Сетчатка глаза болезни штаргардта
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 29 января 2016;
проверки требуют 13 правок.
Болезнь Штаргардта или жёлтопятнистая абиотрофия сетчатки (лат. fundus flavimaculatus), является унаследованной формой ювенильной макулярной дегенерации, которая вызывает прогрессирующее ухудшение зрения, как правило, до точки официальной слепоты. Прогрессирование обычно начинается в возрасте 6-12 лет и замедляется вскоре после быстрого снижения остроты зрения. Несколько генов ассоциированы с этим расстройством. Симптомы обычно развиваются до возраста двадцати лет, и включают волнистое видение, слепые пятна, размытость, нарушение цветового зрения и трудности с адаптацией при тусклом освещении.
Признаки и симптомы[править | править код]
Основным симптомом болезни Штаргардта является снижение остроты зрения от 0.4 до 0.1.[1] Те, у кого болезнь Штаргардта чувствительна к бликам, в пасмурные дни получают некоторое облегчение. Зрение наиболее заметно ухудшается, когда поражена макула (область в центре сетчатки и фокусе зрения), а периферическое зрение затронуто меньше. Симптомы обычно появляются в возрасте до 20 лет. Симптомы включают в себя волнистое видение, слепые пятна, размытость, нарушение цветового зрения и трудности с адаптацией при тусклом освещении.[2][3]
Генетика[править | править код]
Болезнь Штаргардта связана с несколькими разными генами:
- STGD1: наиболее распространенная форма болезни Штаргардта является рецессивная форма, вызванная мутациями в гене ABCA4. Она также может быть связана с геном CNGB3 .
- STGD3: Существует также редкая доминантная форма болезни Штаргардта, вызыванная мутациями в гене ELOVL4.
- STGD4: Связанная с геном PROM1.
Классификация «STGD2» больше не используется.
Патофизиология[править | править код]
Генетический дефект проявляется в визуальном цикле фототрансдукции. Неисправность АТФ-связывающего кассетного транспортера приводит к накоплению токсичного метаболита липофусцина в пигментном эпителии сетчатки глаза.
Форма болезни Штаргардта, которая включает в себя дроссельную схему дистрофии, обусловлена мутацией в гене, который кодирует связанный с мембраной белок, который, в свою очередь, участвует в удлинении очень длинноцепочечных жирных кислот (ELOVL4).
Лечение[править | править код]
Нет доступного лечения для болезни Штаргардта.[1] Многие пациенты используют лупы и, чтобы замедлить развитие болезни, носят солнцезащитные очки.[4]
Прогноз[править | править код]
Долгосрочный прогноз для пациентов с болезнью Штаргардта колеблется в широких пределах.[1]
Болезнь Штаргардта не оказывает никакого влияния на общее состояние здоровья и продолжительность жизни.[5] Некоторые пациенты могут водить машину.
Эпидемиология[править | править код]
Болезнь Штаргардта — наиболее распространенная форма наследственной дегенерации жёлтого пятна несовершеннолетних.[2]
Исследования[править | править код]
22 ноября 2010 года было объявлено, что Advanced Cell Technology[6] получил разрешение от United States Food and Drug Administration немедленно инициировать фазы I/II многоцентрового клинического исследования с использованием клеток сетчатки, полученных из эмбриональных стволовых клеток человека (ЭСК) для лечения пациентов с болезнью Штаргардта.
В сентябре 2011 года ACT объявил о начале очередного этапа лечения для SMD и Dry AMD, так как первый этап оказался безопасным с точки зрения независимого совета экспертов.[7] В марте 2013 года, после лечения и сбора данных о 18 больных, Advanced Cell получил одобрение, чтобы проверить его лечение стволовыми клетками на пациентах с остротой зрения 20/100.[8]
Недавно было обнаружено, что новый препарат может удалить липофусцин из клеток пигментного эпителия сетчатки.[9] Это открывает новую возможность терапии для лечения болезни Штаргардта. Препарат в настоящее время предоставляется как лекарство от орфанного заболевания болезни Штаргардта Европейским агентством по лекарственным средствам.
История[править | править код]
Болезнь была обнаружена в 1909 году Карлом Штаргардтом (нем. Karl Stargardt), офтальмологом в Берлине.[10][11]
В 1997 году было обнаружено, что мутации в гене ABCA4 являются причиной болезни Штаргардта. Мутации вызывают выработку дисфункционального белка, который не может выполнить перенос энергии для фоторецепторных клеток сетчатки. Клетки фоторецепторов вырождаются, что приводит к потере зрения.[2]
Примечания[править | править код]
Источник
Болезнь Штаргардта – наследственное заболевание сетчатки, которое проявляется дистрофическими изменениями ее макулярной зоны и приводит к потере центрального зрения. Дебют заболевания приходится на детский или юношеский возраст. У пациентов отмечаются центральные скотомы и нарушения цветового зрения. Прогрессирование болезни Штаргардта приводит к полной слепоте. Диагностика проводится с помощью офтальмоскопии, флуоресцентной ангиографии и ЭФИ сетчатки. Для лечения применяется инъекционная терапия (витамины, антиоксиданты, ангиопротекторы), физиотерапия, проводятся реваскуляризирующие операции, разрабатывается методика аутологичной тканевой терапии.
Общие сведения
Другое название болезни Штаргардта – ювенильная макулярная дегенерация – отражает суть заболевания: оно начинается в юном (ювенильном) возрасте и характеризуется поражением макулы – рецепторного аппарата зрительного анализатора. Заболевание описал немецкий офтальмолог Карл Штаргардт в начале ХХ века как врожденное поражение макулярной области глаза, которое передавалось по наследству в одной семье. Типичные офтальмоскопические признаки болезни Штаргардта полиморфны: «атрофия хориоидеи», «бычий глаз», «битая (кованая) бронза». Патогенетическое название патологии – «желтопятнистая абиотрофия сетчатки» — отражает изменения в области глазного дна.
В 1997 году генетики обнаружили мутацию гена АВСR, вызывающую нарушение выработки белка, который должен переносить энергию фоторецепторным клеткам. Неполноценность переносчика АТФ приводит к гибели фоторецепторов сетчатки глаз. Различные виды наследственно обусловленной макулярной дистрофии встречаются в 50% случаев патологии глаз. Из них болезнь Штаргардта составляет около 7%. Нозологическая форма диагностируется с частотой 1:10000 и характеризуется прогрессирующим течением. Двусторонняя патология глаз начинается в молодом возрасте (от 6 до 21 года) и приводит к тяжелым последствиям, вплоть до полной потери зрения. Заболевание имеет социальную значимость, потому что приводит к инвалидности в молодом возрасте.
Болезнь Штаргардта
Причины развития болезни Штаргардта
Наследование не зависит от половой принадлежности пациента и родителей. Патология передается преимущественно по аутосомно-рецессивному типу, то есть наследование патологии не связано с полом (аутосомное – связано с неполовыми хромосомами) и не всегда передается будущему поколению (рецессивный путь наследования). По последним данным врачей-генетиков, патология гена может передаваться и по доминантному типу. При доминантном типе наследования дефектов гена – контролера синтеза белка-транспортера АТФ – заболевание протекает легче и нечасто приводит к инвалидности. Большинство рецепторных клеток макулы (верхушки) желтого пятна глазного дна функционируют. У пациентов с доминантным типом наследования болезнь протекает с минимумом проявлений. Больные сохраняют работоспособность и могут даже водить автотранспорт.
Основная причина дегенерации клеток макулы заключается в том, что они страдают от дефицита энергии. Дефект гена приводит к синтезу неполноценного белка, транспортирующего молекулы АТФ через мембрану клеток желтого пятна – центра сетчатки глаза, в котором фокусируется графическое и цветное изображение. В области желтого пятна нет кровеносных сосудов. Питание клеток-колбочек осуществляется за счет белков-переносчиков АТФ из близлежащей сосудистой оболочки (хориоидеи). Белки переносят через мембрану внутрь клеток-колбочек молекулы АТФ.
В нормальных условиях родопсин фоторецепторов поглощает фотон света, трансформируясь в транс-ретиналь и опсин. Затем транс-ретиналь под действием энергии АТФ, которую приносят белки-переносчики, превращается в ретиналь, который соединяется с опсином. Так восстанавливается родопсин. При наследственной мутации гена образуется неполноценный белок-переносчик. В результате нарушается восстановление родопсина и скапливается транс-ретиналь. Он превращается в липофусцин и оказывает прямое токсическое действие на клетки-колбочки.
Классификация болезни Штаргардта
Виды заболевания зависят от распространенности зоны поражения желтого пятна. В офтальмологии различают следующие формы болезни Штаргардта: центральную, перицентральную, центропериферическую (смешанную). При центральной форме поражаются клетки в центре желтого пятна. Это выражается в выпадении центрального зрения. У больного появляется центральная скотома (от гр. «скотос» — темнота). Выпадает из поля зрения центральная зона. Больной видит изображение с темным пятном в точке фиксации взгляда.
Перицентральная форма характеризуется появлением скотомы в стороне от точки фиксации. Человек способен фокусировать взгляд, но отмечает выпадения в одной из сторон от центра поля зрения в виде полумесяца. Со временем скотома приобретает вид темного кольца. Центропериферическая форма начинается с центра и стремительно распространяется к периферии. Темное пятно разрастается и полностью перекрывает поле зрения.
Симптомы болезни Штаргардта
Проявления заболевания начинаются в возрасте 6-7 лет. У всех пациентов, независимо от типа наследования, наблюдаются центральные скотомы. При благоприятном течении скотомы относительные: пациент видит яркие предметы с четкими контурами и не различает объекты со слабой цветовой гаммой. У многих больных отмечается нарушение цветового зрения по типу красно-зеленой дисхромазии, при которой человек видит светло-зеленый цвет как темно-красный. В то же время, некоторые пациенты не отмечают изменения восприятия цветной гаммы.
В начальной фазе заболевания не изменяются границы периферического зрения, при прогрессировании центральные скотомы расширяются, что приводит к полной слепоте. Одновременно с появлением выпадения центрального зрения уменьшается его острота. В завершающей стадии болезни Штаргардта зрительный нерв атрофируется. Человек полностью теряет зрение. Не наблюдается изменений других органов, как в начальной, так и в терминальной стадии заболевания.
Диагностика болезни Штаргардта
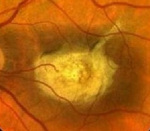
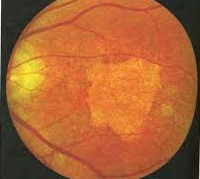
Заболевание начинается в детском возрасте – это один из главных признаков для дифференциальной диагностики. С помощью офтальмоскопии обнаруживается широкое кольцо пониженной пигментации, которое окружает темный центр. Вокруг бледного кольца отмечается следующее кольцо гиперпигментированных клеток. Картина напоминает «бычий глаз» или «кованую бронзу». Фовеолярный рефлекс отрицательный. Макулярное возвышение не определяется. При осмотре желтого пятна отмечаются желтовато-белые пятна разной величины и конфигурации. Со временем границы включений размываются, пятна приобретают серый оттенок либо полностью исчезают.
Во время проведения периметрии при болезни Штангардта отмечаются положительные или отрицательные (пациент их не ощущает) центральные скотомы. При центральной форме заболевания развивается красно-зеленая дейтеранопия. Для периферической формы не характерно нарушение цветового восприятия. Пространственная контрастная чувствительность изменяется по всему диапазону: отсутствует в области высоких частот (в центральном участке до 6-10 градусов) и снижается в области средних частот.
В начальной стадии заболевания отмечается снижение показателей макулярной электрографии при центральной форме дистрофии. При дальнейшем прогрессировании электрические потенциалы не регистрируются. При расположении дистрофии по средней периферической зоне в начальной стадии отмечается нормальная электрография и электроокулография. Затем значения колбочковых и палочковых компонентов элетроретинографии снижаются до субнормальрных. Заболевание протекает бессимптомно – без нарушения остроты зрения и восприятия цвета. Границы поля зрения находятся в пределах нормы. Незначительно снижена темновая адаптация.
С помощью флуоресцентной ангиографии на фоне «бычьего глаза» не обнаруживаются зоны гипофлуоресценции, просматриваются капилляры, «молчащая» или «темная» сосудистая оболочка. В зонах атрофии заметны гиперфлуоресцирующие участки клеток пигментного эпителия сетчатки. Гистологическое исследование в центральной зоне глазного дна определяет повышенное количество пигмента – липофусцина. Отмечается комбинация гипертрофированных и атрофированных клеток пигментного эпителия.
Молекулярно-генетический анализ позволяет заметить мутацию гена до начала проявлений болезни. Чтобы обнаружить замену нуклеотидов, проводится ПЦР в режиме реального времени при использовании нескольких ДНК-зондов – «молекулярных маяков». Дифференциальная диагностика болезни Штаргардта осуществляется с приобретенными лекарственными дистрофиями, пятнами сетчатки Кандори, семейными друзами, ювенильным ретиношизисом, доминантной прогрессирующей фовеальной, колбочковой, колбочно-палочковой и палочко-колбочковой дистрофией.
Лечение и прогноз болезни Штаргардта
Этиологического лечения нет. В качестве общего вспомогательного лечения применяются парабульбарные инъекций таурина и антиоксидантов, введение сосудорасширяющих средств (пентоксифиллин, никотиновая кислота), стероидных препаратов. Проводится витаминотерапия для укрепления сосудов и улучшения кровоснабжения (вит. группы В, А, С, Е). Показаны физиотерапевтические методы лечения: лекарственный электрофорез, ультразвук, лазерстимуляция сетчатки. Применяется методика реваскуляризации сетчатки путем трансплантации в зону желтого пятна пучка мышечных волокон. Разрабатывается патогенетическая регенерационная офтальмологическая технология аутологичной тканевой терапии с помощью стволовых клеток жировой ткани пациента.
Болезнь Штаргардта начинается в раннем возрасте и быстро приводит к инвалидности по зрению. В редких случаях, при доминантном типе наследования, зрение падает медленно. Пациентам рекомендуется наблюдение офтальмолога, прием витаминных комплексов и ношение солнцезащитных очков.
Источник
С Михаилом разговаривать приятно: он умный и начитанный, имеет множество увлечений, а о главном – автогонках – может рассказывать часами. Интеллигентное лицо – очки его украшают. Спокойный, уверенный в себе молодой человек 18 лет от роду. И тем страннее слушать то, что он говорит.
Дистрофия Штаргардта: дорога к слепоте
«Зрение у меня всегда было не очень. Я с детства наблюдался у офтальмолога. Относился к этому спокойно, очки мне не мешали. А в 16 лет начал замечать, что в темноте вижу всё хуже и хуже. К тому же стали выпадать некоторые участки зрения, буквально: здесь вижу, здесь не вижу. Честно говоря, испугался.
Точку поставил визит в военкомат. Медицинская комиссия вынесла вердикт: «абиотрофия сетчатки».
Дальнейшее обследование добавило переживаний. Диагноз звучал как приговор: желтопятнистая дистрофия сетчатки, она же макулодистрофия Штаргардта. Сказали: генетика, и сделать ничего нельзя, заболевание не лечится
Дома с родителями мы перевернул весь Интернет, через знакомых получили консультации нескольких профессоров-офтальмологов, нашли выходы на клиники в Изаиле, Германии, США… Везде, где мы думали, медицина может всё, нам сказали, что надежды на благополучный исход лечения нет.
Вариантов, кроме слепоты, у меня не было.»
«Абиотрофия Штаргардта – это довольно распространённое генетическое заболевание. По статистике она встречается у одного из 20 000 человек. Таким образом, только в России около 7 000 больных, которые по его причине теряют или уже потеряли зрение.
Желтопятнистое глазное дно, другое название этого синдрома, проявляется обычно как раз в подростковом и раннем юношеском возрасте – с 12 до 16 лет. Потеря зрения обычно идет очень резко – в случае Михаила процесс занял всего полгода.
В «УникаМед» Михаил попал в 18 лет, то есть через полтора года после постановки ему диагноза. К этому моменту он практически ничего не видел в темноте, наблюдались скотомы – выпадение участков зрения.
Без коррекции правый глаз видел 20%, левый — 15%. После коррекции оптикой правый глаз — 65%, левый — 55%.
Динамика развития процесса позволяла предположить полную потерю зрения уже к 20 годам».
Дегенерация Штаргардта – не приговор
То, о чём Миша рассказывает дальше, похоже на чудо.
«Мы продолжали искать, и на сайте «УникаМед» прочитали, что синдром Штаргардта они лечат! Поверить было сложно, но мы поехали в Москву.
Уже после первого сеанса регенеративной терапии я стал лучше видеть в темноте, зрение улучшилось. Ощущения такие, будто кто-то наконец помыл грязное лобовое стекло, закрывавшее обзор. Фантастика!
Всего я пока прошел три сеанса – сейчас у меня перерыв. Через 6 месяцев нужно будет пройти еще одну процедуру. Кстати, к автоспорту, в том числе к ночным заездам я уже вернулся!»
«Никаких чудес и никакой фантастики в случае Михаила, конечно же, нет.
Если совсем коротко, то в основе регенеративной терапии – уникальный клеточный аутологичный трансплантат, который стимулирует обновление сетчатки (приставка «ауто» обозначает трансплантат, клетки для которого берутся у самого человека и ему же пересаживаются).
Применение метода показывает положительный эффект практически у всех пациентов. Расширяется поле зрения, улучшается его острота. И если заболевание не является генетическим или сильно запущенным, мы всегда наблюдаем значительное улучшение остроты и качества зрения.
Сложные заболевания, как у Михаила, перестают прогрессировать. Состояние сетчатки и ее питание улучшается – соответственно, значительно улучшается и зрительная функция.
В случае Михаила через три месяца после первого сеанса регенеративной терапии скотомы исчезли, показатели зрения изменились таким образом:
Без оптики: правый глаз — 30%, левый — 25%
С подобранной оптикой: правый глаз — 85%, левый — 75%.
Сейчас, после трех сеансов лечения, Михаил пока не нуждается в дальнейшей терапии, но через 6-8 месяцев он должен снова приехать на осмотр: каким бы волшебным ни казался метод, перепрограммировать гены никто пока не научился, и для поддержания результата лечение нужно периодически повторять.»

Марина Юрьевна, главный врач клиники «УникаМед»
Случай Михаила далеко не единичен: к нам в «УникаМед» обращаются люди, от которых отказались другие клиники. И даже на стадии невидения многие из них благодаря регенеративной терапии восстанавливают зрение.
Как проходит процедура
Для выполнения регенеративной терапии не требуется пребывания в стационаре. Пересадка клеточного материала выполняется амбулаторно в течение одного дня: пациент проводит в клинике 10-12 часов.
Но то, что со стороны кажется чудом, на самом деле – результат кропотливой работы.
 Изготовление трансплантанта начинается с забора костного мозга. Потом его специальным образом подготавливают. Процедура подготовки клеток очень сложная. Она требует специального оборудования, одновременного участия в процессе нескольких классных специалистов по клеточной биологии и точного последовательного выполнения ряда операций.
Изготовление трансплантанта начинается с забора костного мозга. Потом его специальным образом подготавливают. Процедура подготовки клеток очень сложная. Она требует специального оборудования, одновременного участия в процессе нескольких классных специалистов по клеточной биологии и точного последовательного выполнения ряда операций.
Полученный материал по особой технологии вводится пациенту в зависимости от его заболевания и состояния органов зрения.
Вечером, после осмотра офтальмологом, вас выписывают домой до следующей процедуры. Интервал между процедурами определяется индивидуально, но их эффект имеет накопительный характер. И если между первой, второй и третьей процедурой требуется, допустим, три месяца, то между третьей и четвертой может пройти уже полгода. И так далее.
Между процедурами лечение болезни Штаргардта требует регулярного динамического наблюдения офтальмолога, чтобы вовремя «перехватить» возможные потери зрения.
Разумеется, получить эффект легче при лечении заболевания на самой ранней стадии, не дожидаясь потери зрения, полной или частичной. Если замечаете, что зрение становится хуже (особенно в темноте или в сумерках), если сузилось поле зрения, если цвета стали казаться вам менее яркими – найдите время показаться офтальмологу.
Неизлечимых заболеваний становится все меньше – и в клинике «УникаМед» у нас для этого есть все возможности. Регенеративная терапия показывает положительные результаты не только у пациентов с заболеванием Штаргардта, но и в лечении атрофии зрительного нерва, макулодистрофии разной природы, других форм дистрофии сетчатки глаза.
Позвоните и запишитесь на прием по телефону +7 (495) 215-18-19 в Москве.
Источник

