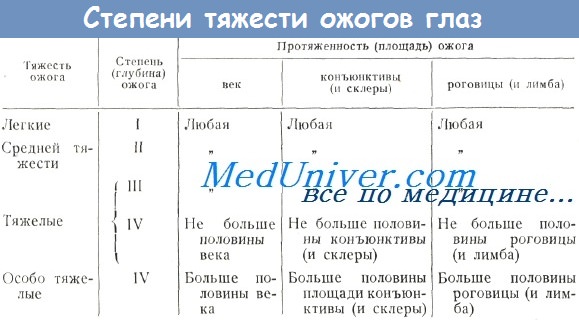
Эндотелиальная дистрофия роговицы фото
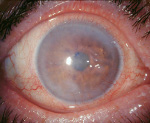
Эндотелиальная дистрофия роговицы – это заболевание органа зрения, причиной которого является отмирание клеток заднего эпителия роговой оболочки. Клинически проявляется снижением остроты зрения в утреннее время, фотофобией, гиперемией, повышенным слезотечением, болевым синдромом. Диагностика эндотелиальной дистрофии роговицы включает в себя проведение наружного осмотра, конфокальной микроскопии, биомикроскопии, пахиметрии, визометрии. Симптоматическая терапия основывается на инстилляции гипертонических солевых растворов. Хирургическая тактика – проведение сквозной или послойной кератопластики.
Общие сведения
Эндотелиальная дистрофия роговицы, или дистрофия Фукса – это патологическое состояние в офтальмологии, характеризующееся нарушением трофики с последующей дегенерацией роговой оболочки. Первое описание первичной эндотелиальной дистрофии роговицы было представлено австрийским ученым Э. Фуксом в начале ХХ века. Исследователь считал, что патология развивается вследствие нарушения регионального кровоснабжения или иннервации, гормонального дисбаланса.
Заболевание может быть первичным или вторичным, ранним или поздним. При раннем варианте эндотелиальную дистрофию роговицы можно диагностировать у детей до 3 лет. Клиника позднего варианта наблюдается у пациентов в возрасте старше 45 лет. Ранние дистрофии с одинаковой частотой встречаются среди мужчин и женщин. Поздняя форма заболевания более распространена среди лиц женского пола.
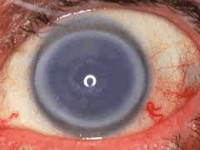
Эндотелиальная дистрофия роговицы
Причины
Первичная эндотелиальная дистрофия роговицы – это генетически детерминированное заболевание. Установлен аутосомно-доминантный тип наследования с неполной или высокой пенетрантностью. При ранней форме возникает мутация гена COL8A2, при поздней – SLC4A11 или ZEB1. В то же время, у 50% пациентов болезнь развивается спорадически.
Реже триггером выступает дисфункция митохондрий эндотелиоцитов, что ведет к их недостаточности. Патологический процесс локализируется во внутреннем слое роговой оболочки, эндотелиоциты которого в последующем не могут делиться и регенерировать. Этиологической роли факторов внешней среды и системных патологий в развитии данного заболевания не установлено.
Наиболее распространённая причина возникновение вторичной эндотелиальной дистрофии роговицы – травматическое повреждение органа зрения. Ятрогенный фактор реализуется при проведении оперативного вмешательства. Хроническое течение кератита при отсутствии своевременного лечения способствует дегенерации роговой оболочки, что обусловлено повреждением эндотелия. При данной патологии воспалительный процесс является не этиологическим фактором, а лишь предпосылкой к развитию эндотелиальной дистрофии роговицы у генетически скомпрометированных лиц.
Патогенез
Компенсаторная гиперфункция эндотелиоцитов при прогрессировании заболевания не может обеспечить выведение избытка жидкости и поддержание прозрачности роговицы. Это связано с пропотеванием водянистой влаги передней камеры глаза через дефекты в эндотелии в строму роговой оболочки. Выраженная отечность приводит к эндотелиальной дистрофии роговицы. При распространении отека на наружный слой возникает буллезная кератопатия. Проведение оперативных вмешательств на роговой оболочке в связи с выраженным истончением эндотелия часто осложняется отеком, что усугубляет деструктивные процессы.
Симптомы дистрофии роговицы
С клинической точки зрения выделяют первичную и вторичную формы дистрофии Фукса. Первичное поражение роговой оболочки является врождённым. Первые проявления ранней дистрофии обнаруживаются при рождении или в раннем детском возрасте, но этот тип заболевания встречается крайне редко. Поздний вариант первичной эндотелиальной дистрофии Фукса чаще развивается у лиц после 45 лет. Для данного типа патологии характерно бинокулярное, но асимметричное течение. Вторичная дистрофия – это приобретённое заболевание, при котором наблюдается монокулярное поражение.
В зависимости от степени тяжести патологии клиника эндотелиальной дистрофии роговицы может характеризоваться латентным течением или проявлениями буллезной кератопатии. Симптомы заболевания медленно прогрессируют, поэтому с момента появления первых признаков до формирования развернутой клинической картины может пройти около 20 лет.
Первая стадия
На первой стадии эндотелиальной дистрофии роговицы морфологические изменения затрагивают только центральные отделы роговой оболочки. При этом появляются специфические коллагеновые образования (гутты) каплевидной, бородавчатой и грибовидной формы. Жалобы отсутствуют. Единственным симптомом заболевания является незначительное снижение остроты зрения в утреннее время.
Вторая стадия
На второй стадии количество эндотелиоцитов уменьшается, развивается отек роговицы, появляются одиночные буллы. Ощущение инородного тела сменяется снижением чувствительности роговой оболочки из-за дегенерации нервных окончаний. Специфические симптомы этой стадии эндотелиальной дистрофии роговицы представлены фотофобией, гиперемией глаз, снижением остроты зрения в утреннее время с последующим восстановлением к вечеру. Это связано с тем, что из-за сомкнутых глаз в период сна должным образом не осуществляется испарение влаги с роговой оболочки, что приводит к депонированию жидкости. Днем испарение влаги способствует уменьшению отечности и возобновлению зрительных функций.
Длительное течение эндотелиальной дистрофии роговицы становится причиной медленно прогрессирующего снижения остроты зрения. При распространении патологического процесса на эпителиальный слой и появлении буллезных изменений пациенты предъявляют жалобы на ощущение инородного тела и повышенную слезоточивость. Болевой синдром, сопровождающийся сильным дискомфортом в области глазницы, развивается при разрыве булл у больных с буллезной кератопатией.
Третья стадия
На третьей стадии вдоль эпителия базальной мембраны синтезируется фиброзная ткань с последующим формированием паннуса. Общее состояние при этом несколько улучшается, но прогрессирование эндотелиальной дистрофии роговицы в дальнейшем приводит к появлению эпителиальных эрозий, язв микробного генеза и васкуляризации центральной части роговой оболочки.
Диагностика
Диагностика эндотелиальной дистрофии роговицы основывается на результатах наружного осмотра и специальных офтальмологических исследований. При наружном осмотре выявляется помутнение роговицы, возможна конъюнктивальная инъекция сосудов. Решающие данные получают с помощью:
- Конфокальной микроскопии роговицы. Является золотым стандартом в диагностике данной патологии. Помимо детального изображения эндотелия, измеряется плотность клеток и их средний диаметр на единицу площади. Степень снижения размера и количества клеточных элементов при эндотелиальной дистрофии роговицы зависит от тяжести заболевания. Также выявляются специфические образования (гутты) в виде капель темного цвета с яркой центральной частью и околоклеточной локализацией. В начале развития диметр гутты меньше эндотелиоцита, в последующем они сливаются и имеют вид крупных пятен.
- Биомикроскопии. При проведении биомикроскопии со щелевой лампой визуализируются локальные зоны дегенерации эндотелиального слоя, отечность. При распространении отека на наружный слой определяются специфические буллы на поверхности роговой оболочки, что указывает на развитие буллезной кератопатии.
- Пахиметрии. Методом пахиметрии определяют толщину роговой оболочки. Дегенеративные процессы при эндотелиальной дистрофии роговицы приводят к ее истончению (менее 0,49 мм), но при появлении отека ее толщина может превышать референсные значения (0,56 мм).
- Визометрии. При помощи визометрии измеряется степень снижения остроты зрения. Для получения достоверного результата и косвенного определения степени выраженности отека пациентам с эндотелиальной дистрофией роговицы рекомендовано проводить исследования в утреннее и вечернее время.
Лечение эндотелиальной дистрофии роговицы
Консервативная тактика
Симптоматическая терапия эндотелиальной дистрофии роговицы включает в себя проведение инстилляций гипертонических солевых растворов с целью уменьшения отечности. Выведение с роговой оболочки избыточной жидкости улучшает остроту зрения. С целью купирования болевого синдрома показан пероральный прием анальгетиков или их инстилляция. Для коррекции остроты зрения можно использовать только мягкие контактные линзы или очки. Также в лечении эндотелиальной дистрофии роговицы применяется роговичный кросс-линкинг, в основе которого лежит фотополимеризация волокон стромы при помощи совместного воздействия фотосенсибилизирующего препарата и ультрафиолетового излучения.
Хирургическое лечение
Тяжелое течение эндотелиальной дистрофии роговицы, сопровождающееся выраженным снижением остроты зрения, сильным истончением роговицы по данным пахиметрии и низкой плотностью клеток на единицу площади по результатам конфокальной микроскопии, является показанием к проведению кератопластики. Сквозной вариант хирургического вмешательства показан при тотальном дистрофическом процессе. Послойная кератопластика рекомендована пациентам в случае повреждения одного или нескольких слоев роговой оболочки. При этом зачастую выполняется трансплантация десцеметовой мембраны совместно с эндотелием.
Прогноз и профилактика
Прогноз при ранней диагностике и лечении для жизни и трудоспособности благоприятный. Отсутствие терапии может привести к полной утрате зрения и инвалидизации пациента. Специфических мер по профилактике эндотелиальной дистрофии роговицы не разработано, поскольку заболевание генетически детерминированное. Неспецифические превентивные меры сводятся к предупреждению травматических повреждений у генетически скомпрометированных лиц, скринингу у новорожденных, своевременной диагностике и лечению офтальмологической патологии. Всем пациентам с установленным диагнозом эндотелиальная дистрофия роговицы необходимо 2 раза в год проходить обследование у офтальмолога.
Источник
Эпителиально-эндотелиальная дистрофия роговой оболочки глаза (кератопатия, дистрофия Фукса) – это заболевание зрительного органа по причине дегенерации клеток заднего эпителия роговицы.
Патология относится к первичным, то есть генетически обусловленным заболеваниям. Болезнь получила свое название по имени австрийского офтальмолога Эрнста Фукса, который описал ее в первые годы ХХ века. Чуть чаще диагностируется у женщин, чем у мужчин. Выделяют два типа дистрофии Фукса:
- ранняя, возникающая сразу же после рождения (встречается очень редко);
- поздняя, развивающуюся после 45 лет.
Симптомы
На ранних этапах развития болезни пациенты говорят о сверхчувствительности к свету, плохом зрении утром — оно улучшается только к вечеру. Это происходит потому, что за ночь жидкость накапливается внутри роговой оболочки, затем днём отек спадает и человек начинает видеть лучше.
На более поздних этапах люди начинают испытывать боль, постоянное ощущение инородного тела внутри глаза.
Причины
В большом числе случаев эта патология носит приобретенный характер, являясь по своей сути вторичной формой дистрофии роговой оболочки. Возникает на базе травм, ранений, а также после операций, проведенных на глаза.
Диагностика
Сначала врач-офтальмолог проводит осмотр больного глаза, собирает подробный анамнез. Далее направит на биомикроскопию и осмотр посредством щелевой лампы. Также у пациента непременно нужно взять пробу жидкости, выделяющейся из глаза.
Важно оценить толщину роговицы, чтобы понять, насколько выражен отек. С этой целью больному проводят ультразвуковую пахиметрию.
Лечение
Выбор терапии лечащий врач осуществляет, основываясь на виде, форме и стадии болезни, месте локализации, особенностях иммунитета человека.
Лечение может включать в себя:
- Кератопротекторные медицинские средства в виде гелей, мазей или капель. Эти медикаменты призваны ускорить регенерацию тканей, улучшить обменные процессы и снять дискомфорт и боль в области глаз. Принцип действия заключается в том, что они покрывают роговицу, защищая ее от негативного влияния и сухости. К данной группе фармсредств относятся «Дефислез», «Визитил», «Актовегин», «Баларпан», «Лакрисин», «Эмоксипин».
- Витаминные комплексы. Хорошо зарекомендовали себя такие средства, как «Витрум вижн», «Лютеин Комплекс», «Оптикс». Для зрения крайне необходимы витамины А, В2, В12, С, В1, Лютеин.
- Антибиотики. Они используются при выраженном отеке роговицы и поражении эпителиального слоя. Бывают в виде мазей или капель. Это может быть «Ципролет», «Тобрекс», «Гентамицин», «Л-оптик»,«Левомицитин», «Флоксал».
- Если эпителиальная дистрофия находится в самом начале своего развития, врач назначает физиотерапию, а именно электрофорез, лазерное облучение. Эти процедуры значительно улучшают качество жизни пациента.
- Кератопластика, или пересадка роговицы. Бывает сквозная либо послойная. Показания к операции: рубцы роговицы, кератоконус, бельмо, тяжелые кератиты. В ходе операции под общим наркозом или местной анестезией удаляют поврежденную роговую оболочку и на ее место ставят донорскую, закрепляя швами. Прогнозы положительные, так как в 95% процедура позволяет серьезно восстановить зрение.
- Кросслинкинг, или фотополимеризация – еще один очень эффективный метод, применяющийся вне зависимости от того, на какой стадии находится болезнь. Этот способ считается малоинвазивным и абсолютно безопасным. Данная процедура инновационна и высокотехнологична. Она позволяет усилить жесткость роговицы, что позволит ей сопротивляться деформации. Между соединительными коллагеновыми волокнами роговицы усиливаются химические связи. В ходе оперирования под микроскопом хирург удаляет верхний слой роговой оболочки, затем чуть более получаса закапывает раствор витамина B2, а после оказывает воздействие лазерным аппаратом. На глаз устанавливается особая контактная линза, которую пациент должен носить 1-2 дня. Далее линза снимается, в течение некоторого времени пациент получает восстановление роговицы, а затем зрения.
К сожалению, лекарственная коррекция эпителиально-эндотелиальной дистрофии роговой оболочки не дает полного излечения этой патологии. Медикаменты лишь снимают дискомфорт и являются дополнением к оперативному вмешательству. При отмене фармацевтики может возникнуть откат на начальное состояние.
Для профилактики повторения проблем с роговицей врачи рекомендуют делать перерывы при работе за компьютером, планшетом, смартфоном или просмотре телевизионных передач.
На зрение положительно влияет зеленый цвет, поэтому переключать внимание нужно именно на предметы данного оттенка. Летом нужно обязательно надевать солнцезащитные очки и избегать попадания лучей на глазную роговицу.
В рацион нужно ввести больше свежих овощей и фруктов. И два раза в год обязательно посещать врача-офтальмолога.
При дистрофии Фукса важно вовремя диагностировать заболевание и своевременно начинать лечение, назначенное специалистом. Одно из самых серьезных осложнений эпителиально-эндотелиальной дистрофии роговицы – потеря зрения.
Больше интересных статей →
Источник
Согласно последней классификации, принятой международным комитетом по классификации роговичных дистрофий (International Committee for Classification of Corneal Dystrophies – IC3D) к группе первичных, генетически детерминированных патологий, или как принято называть в зарубежной литературе – дистрофиям «заднего» типа относятся: дистрофия роговицы Фукса (Fuch’s Endothelial Corneal Dystrophy – FECD), врожденная наследственная эндотелиальная дистрофия (Congenital Hereditary Endothelial Dystrophy – CHED), иридокорнеальный эндотелиальный синдром (Iridocorneal Endothelial Syndrome – ICE), задняя полиморфная дистрофия (Posterior Polymorphous Corneal Dystrophy – PPCD) [198, 199].
Наибольшую распространенность [31, 73] и клиническую значимость среди генетически детерминированных эндотелиальных дистрофий имеет эндотелиальная дистрофия роговицы Фукса, впервые описанная австрийским офтальмологом E. Fuchs в 1902-м году и представленная им под названием «эпителиальная дистрофия роговицы» [74]. В своей работе автор впервые высказал предположение о природе заболевания, связав его с изменениями задних слоев роговицы, в результате которых происходит пропитывание внутриглазной жидкостью стромы роговицы с последующим нарастанием отека эпителия [74, 31]. Предложенный E. Fuchs термин «эпителиальная дистрофия» в настоящее время не используется, так как было доказано, что эпителий роговицы вовлекается в патологический процесс вторично, на поздних стадиях заболевания [65, 185].
В последующем Vogt A., после изобретения в 1911-м году щелевого микроскопа, подробно описал биомикроскопическую картину начальных клинических проявлений заболевания и предложил термин «cornea guttata» для описания характерных эндотелиальных изменений роговицы в виде капель или выпячиваний, которые при увеличении напоминают вид «булыжной мостовой» или «запотелого стекла» [192]. Считается, что cornea guttata служит основным клиническим признаком ДФ и является обязательной находкой при биомикроскопическом исследовании задних слоев роговицы. В то же время немаловажным является тот факт, что cornea guttata может носить посттравматический или поствоспалительный характер, являясь при этом признаком вторичной недостаточности монослоя эндотелиальных клеток [80].
Заболевание встречается в среднем у 4 — 4,5% пациентов старше 50-ти лет [33, 73, 106], имеет неравномерное географическое распространение. Дистрофия роговицы Фукса встречается с большей частотой в странах Европы и США, с меньшей в странах Азии, в частности в Японии [167]. По некоторым данным, женщины страдают ДФ чаще мужчин, приблизительное соотношение составляет 3:1 [31, 33, 58, 106, 122, 166, 196]. Есть данные, что избыточный вес уменьшает вероятность прогрессирования ДФ, а табакокурение – увеличивает [81, 102, 206].
Патогенетические механизмы развития эндотелиальной дистрофии роговицы Фукса локализуются в Десцеметовой мембране (ДМ) и эндотелии. Клетки эндотелия в норме имеют гексагональную форму, являются высокодифференцированными и относятся к долгоживущим элементам. Известно, что плотность эндотелиальных клеток (ПЭК) меняется на протяжении всей жизни, но с разной динамикой. При рождении общее количество клеток эндотелия в глазу человека составляет порядка 1 млн., или 3500-5000 кл/мм² . В первый год жизни ПЭК снижается преимущественно за счет роста роговицы, далее плотность клеток снижается за счет уменьшения их числа. Естественная потеря клеток в возрасте до 14-ти лет составляет 0,6% (0,3 – 1,0%) в год. С возрастом количество клеток эндотелия уменьшается и к 60-ти годам достигает 500 тысяч, или 1400-2500 кл/мм² . Таким образом, имеется физиологическая потеря эндотелиальных клеток (при отсутствии негативных факторов), которая составляет 30-40 клеток ежедневно или 0,5% — 2% в год [8, 26, 101].
Доказанным является факт, что в нормальных условиях клетки эндотелия человека не проявляют способности к пролиферации in vivo [98, 99, 101].
В обычных условиях, т.е. при физиологической регенерации в клетках преобладают процессы восстановления внутриклеточных элементов. В восполнении функции погибших клеток принимают участие соседние за счет изменения формы (полиморфизм) и размеров (полимегетизм). Изучение компенсаторных возможностей клеток эндотелия позволило установить, что минимальное значение ПЭК, при котором возможно поддержание прозрачного состояния роговицы, составляет 300 — 500 кл/мм² [157, 171] (Рис.1).
Как было отмечено, помимо монослоя эндотелиальных клеток, в патологический процесс ДФ вовлекается задняя пограничная мембрана, или Десцеметова мембрана, названная по имени Jean Descemet и представляющая собой базальную мембрану эндотелиального слоя, которая у новорожденного имеет толщину около 3 мкм, у взрослого – 10-12 мкм. ДМ имеет мезодермальное происхождение и, как все базальные мембраны, состоит из коллагена IV и VIII типов, ламинина, фибронектина и протеогликанов, таких как гепаран-сульфат, кератан-сульфат и дерматан-сульфат. При электронной микроскопии в нормальной ДМ определяются 2 слоя: 1) передняя полосатая зона и 2) неполосатая зона [95, 195]. При ДФ ДМ утолщается в 2-4 раза за счет формирования трех новых слоев [78, 95, 195] (рис.2):
3 – задняя полосатая зона;
4 – фибриллярный задний коллагенозный слой (с расположенными фибриллами диаметром 20-30 нм);
5 – фиброклеточный задний коллагенозный слой (содержащий фибробласты).
Морфологическое изучение ДМ при ДФ показало, что средняя ее толщина равняется 21,5 ± 4,5 мкм на периферии и 17,6 ± 3,8 мкм в центре. Cornea guttata имеет место на 75% ДМ, а задний коллагеновый слой — на 15% [87].
Считается, что под влиянием генетических факторов, эндотелиальные клетки приобретают морфологию и функции фибробластов и начинают вырабатывать коллагеновые фибриллы и вещество, аналогичное базальной мембране, приводя к пятислойности ДМ и ее утолщению. Похожие изменения обнаружены у здоровых пожилых людей, как физиологический феномен, так называемые тельца Хассаля-Хенле (Hassal-Henle bodies/warst) – мелкие, округлые, бессимптомные образования со стороны эндотелия, располагающиеся на периферии роговицы [95, 105, 148, 195].
Для систематизации клинических проявлений заболевания В.В. Волковым и М.М. Дроновым (1978) предложена классификация эндотелиально-эпителиальной дистрофии роговицы, также применимая и к первичной ДФ, учитывающая изменения роговицы по глубине поражения ее тканевых слоев, где выделено 5 стадий [7]:
I стадия – эндотелиальная, характеризуется морфологическими изменениями клеток эндотелия, возможен локальный отек и соответственно единичные локальные складки десцеметовой оболочки.
II стадия – стромальная, характеризуется возникновением стойкого отека эндотелия и стромы в результате пропитывания ее внутриглазной жидкостью, множественные складки десцеметовой мембраны.
III стадия – эпителиальная (буллезная), характеризуется возникновением диффузного отека эпителия и булл в результате скопления жидкостью под слоем эпителиальных клеток.
IV стадия – сосудистая (неоваскулярная), характеризуется прорастанием преимущественно глубоких сосудов в задние слои роговицы, вследствие нарушения процессов метаболизма.
V стадия – терминальная (фиброзная), характеризуется формированием стойкого помутнения роговицы, как правило неравномерной плотности вследствие замещения слоев роговицы рубцовой и сосудистой тканью с возможными очаговыми поверхностными изъязвлениями.
Существует другая классификация ДФ, согласно которой выделяют 4 стадии [31, 196]:
I стадия — изменения эндотелия в виде центрально-расположенных единичных или сливных гутт, появляющихся чаще после 40-ка лет. Субъективные жалобы, как правило, отсутствуют.
II стадия — возникновение отека стромы и эпителия роговицы. Больные предъявляют жалобы на туман перед глазами, преимущественно в утреннее время, радужные круги вокруг источников света.
III стадия — образование эпителиальных кист, сливающихся в буллы. При обнажении булл больные предъявляют жалобы на возникновение резких, колющих болей, периодическое чувство инородного тела.
IV стадия — развитие очагов стромального и субэпителиального помутнения, появление новообразованных сосудов. Отмечается уменьшением болевого синдрома и уменьшение буллезности.
За рубежом одной из популярных является классификация ДФ, предложенная Krachmer J. с соавторами (1978) [106]. Она включает 5 стадий, основанных на обнаружении и подсчете гутт на задней поверхности роговицы в оптическом срезе и при ретролюминесценции:
0 стадия — до 11 центрально расположенных гутт на роговицах обоих глаз
I стадия — 12 или более центрально расположенных гутт
II стадия — сливные центральные гутты шириной 1-2 мм
III стадия — сливные центральные гутты шириной 2-5 мм
IV стадия — сливные центральные гутты шириной более 5мм
V стадия — сливные гутты шириной более 5 мм, отек стромы и/или отек эпителия роговицы
Разделение дистрофии Фукса согласно представленным стадиям является наиболее удобным на ранних этапах заболевания. Применение конфокальной микроскопии, фоторегистрации гутт при ретролюминесценции [85] в комплексе с исследованием пахиметрии роговицы в динамике позволяет достоверно установить прогрессирование заболевания на субклиническом уровне.
Источник