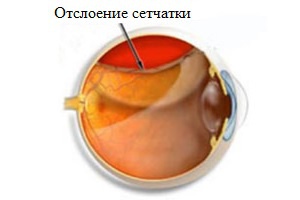
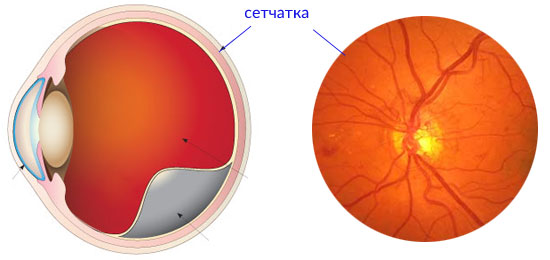
Современные подходы к лечению окклюзий вен сетчатки
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения.
Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным
медицинским работником или студентом медицинского образовательного учреждения.
- Журналы
- Вестник офтальмологии
# 3, 2017
- . Современные подходы и место лазерно…
Авторы:
- С. В. Сдобникова
ФГБНУ «НИИ глазных болезней», ул. Россолимо, 11, A, Б, Москва, Россия, 119021 - К. А. Мирзабекова
ФГБНУ «НИИ глазных болезней», ул. Россолимо, 11, A, Б, Москва, Россия, 119021 - В. К. Сургуч
ФГБНУ «НИИ глазных болезней», ул. Россолимо, 11, A, Б, Москва, Россия, 119021
Журнал:
Вестник офтальмологии. 2017;133(3): 67-74
Просмотрено:
1561
Скачано:
753
Несмотря на появление новых подходов в лечении тромбозов вен сетчатки и посттромботических осложнений, а именно в интравитреальной фармакотерапии и хирургическом лечении, лазерная коагуляция продолжает играть существенную роль в ведении пациентов с данной патологией. Хотя метод лазерной коагуляции используется достаточно давно, сохраняются различные взгляды на показания к его назначению и технику выполнения в конкретных клинических ситуациях. При этом не все представления о лазерной коагуляции при тромбозах основаны на убедительных клинических исследованиях. Цель работы — в обобщенном виде на основании данных литературы представить использование лазеркоагуляции в современном комплексном лечении окклюзий вен сетчатки, а также показать, какие аспекты лечения тромбозов можно считать устоявшимися и обоснованными, а какие остаются предметом обсуждения.
Ключевые слова:
- окклюзии вен сетчатки
- тромбоз центральной вены сетчатки
- лазерная коагуляция
КАК ЦИТИРОВАТЬ:
Сдобникова С.В., Мирзабекова К.А., Сургуч В.К.
. Современные подходы и место лазерной коагуляции в лечении окклюзий вен сетчатки.
Вестник офтальмологии.
2017;133(3):67-74.
https://doi.org/10.17116/oftalma2017133367-74
Список литературы:
- Тульцева С.Н., Астахов Ю.С. Окклюзии вен сетчатки. С.-Петербург: «Издательство Н-Л»; 2010.
- Karia N. Retinal vein occlusion: pathophysiology and treatment options. OPTH. 2010:809. https://doi.org/10.2147/opth.s7631
- Rogers S, McIntosh R, Lim L et al. Natural History of Branch Retinal Vein Occlusion: An Evidence-Based Systematic Review. Ophthalmology. 2010;117(6):1094-1101.e5. https://doi.org/10.1016/j.ophtha.2010.01.058
- Кацнельсон Л.А., Форофонова Т.И., Бунин А.Я. Сосудистые заболевания глаз. М.: Медицина; 1990.
- Танковский В.Э. Тромбозы вен сетчатки. М.; 2000.
- Bynoe L, Hutchins R, Lazarus H, Friedberg M. Retinal Endovascular Surgery For Central Retinal Vein Occlusion. Retina. 2005;25(5):625-632. https://doi.org/10.1097/00006982-200507000-00014
- Сосновский В.В., Сдобникова С.В. Использование тромболитических препаратов при инвазивных методах лечения окклюзий ретинальных сосудов. Вестник офтальмологии. 2007;123(5):51-54.
- Сосновский В.В., Сдобникова С.В., Ревишин А.В., Сургуч В.К., Троицкая Н.А., Сидамонидзе А.Л., Белогуров А.А., Дельвер Э.П., Гурский Я.Г. Tактика хирургического лечения субмакулярных кровоизлияний с использованием рекомбинантной проурокиназы. Вестник офтальмологии. 2009;125(4): 3-8.
- McAllister I, Vijayasekaran S, YuD. Intravitreal Tenecteplase (Metalyse) for Acute Management of Retinal Vein Occlusions. Investigative Opthalmology & Visual Science. 2013;54(7):4910. https://doi.org/10.1167/iovs.13-11967
- Mahmoud T, Peng Y, Proia A, Davidson M, Deramo V, Fekrat S. Recombinant tissue plasminogen activator injected into the vitreous cavity may penetrate the retinal veins of a porcine model of vascular occlusion. British Journal of Ophthalmology. 2006;90(7):911-915. https://doi.org/10.1136/bjo.2005.089037
- Kamei M, Matsumura N, Suzuki M, Sakimoto S, Sakaguchi H, Nishida K. Reperfusion of Large Ischemic Areas Associated With Central Retinal Vein Occlusion. JAMA Ophthalmol. 2014;132(3):361. https://doi.org/10.1001/jamaophthalmol.2013.6334
- Elman M, Raden R, Carrigan A. Intravitreal Injection of Tissue Plasminogen Activator for Central Retinal Vein Occlusion. Retina. 2003;23(3):435. https://doi.org/10.1097/00006982-200306000-00045
- Shahid H. The management of retinal vein occlusion: is interventional ophthalmology the way forward?. British Journal of Ophthalmology. 2006;90(5):627-639. https://doi.org/10.1136/bjo.2005.068668
- Lazo-Langner A, Hawel J, Ageno W, Kovacs M. Low molecular weight heparin for the treatment of retinal vein occlusion: a systematic review and meta-analysis of randomized trials. Haematologica. 2010;95(9):1587-1593. https://doi.org/10.3324/haematol.2010.023614
- Donati G1, Mavrakanas N, Pournaras CJ. Isovolumic hemodilution in the management of the acute phase of central retinal vein occlusion: a pilot study. J Fr Ophtalmol. 2009;32(10):750-756. https://doi.org/ 10.1016/j.jfo.2009.10.010
- Hayreh S, Podhajsky P, Zimmerman M. Natural History of Visual Outcome in Central Retinal Vein Occlusion. Ophthalmology. 2011;118(1):119-133.e2. https://doi.org/10.1016/j.ophtha.2010.04.019
- A Randomized Clinical Trial of Early Panretinal Photocoagulation for Ischermic Central Vein Occlusion. Ophthalmology. 1995;102(10):1434-1444. https://doi.org/10.1016/s0161-6420(95)30848-2
- Natural History and Clinical Management of Central Retinal Vein Occlusion. Archives of Ophthalmology. 1997;115(4):486. https://doi.org/10.1001/archopht.1997.01100150488006
- Coscas G, Loewenstein A, Augustin A et al. Management of Retinal Vein Occlusion — Consensus Document. Ophthalmologica. 2011;226(1):4-28. https://doi.org/10.1159/000327391
- Hayreh S, Zimmerman M. Ocular Neovascularization Associated With Central And Hemicentral Retinal Vein Occlusion. Retina. 2012;32(8):1553-1565. https://doi.org/10.1097/iae.0b013e318246912c
- Lattanzio R, Torres Gimeno A, Battaglia Parodi M, Bandello F. Retinal Vein Occlusion: Current Treatment. Ophthalmologica. 2011;225(3):135-143. https://doi.org/10.1159/000314718
- Chan C, Ip M, Vanveldhuisen P et al. SCORE Study report #11: incidences of neovascular events in eyes with retinal vein occlusion. Ophthalmology. 2011;118(7):1364-1372. https://doi.org/ 10.1016/j.ophtha.2010.11.020
- Hayreh S, Rojas P, Podhajsky P, Montague P, Woolson R. Ocular Neovascularization with Retinal Vascular Occlusion-III. Ophthalmology. 1983;90(5):488-506. https://doi.org/10.1016/s0161-6420(83)34542-5
- Кански Д., Милевски С., Дамато Б., Тэннер В. Заболевания глазного дна. М.: Медпресс-информ; 2009.
- A Randomized Clinical Trial of Early Panretinal Photocoagulation for Ischermic Central Vein Occlusion. Ophthalmology. 1995;102(10):1434-1444. https://doi.org/10.1016/s0161-6420(95)30848-2
- Argon Laser Scatter Photocoagulation for Prevention of Neovascularization and Vitreous Hemorrhage in Branch Vein Occlusion. Archives of Ophthalmology. 1986;104(1):34. https://doi.org/10.1001/archopht.1986.01050130044017
- Argon Laser Photocoagulation for Macular Edema in Branch Vein Occlusion. American Journal of Ophthalmology. 1984;98(3):271-282. https://doi.org/10.1016/0002-9394(84)90316-7
- Early Photocoagulation for Diabetic Retinopathy. Ophthalmology. 1991; 98(5):766-785. https://doi.org/10.1016/s0161-6420(13)38011-7
- Bandello F, Brancato R, Trabuccbi G, Lattanzio R, Malegori A. Diode versus argon-green laser panretinal photocoagulation in proliferative diabetic retinopathy: A randomized study in 44 eyes with a long follow-up time. Graefe’s Arch Clin Exp Ophthalmol. 1993;231(9):491-494. https://doi.org/10.1007/bf00921112
- Bandello F, Brancato R, Lattanzio R, Trabucchi G, Azzolini C, Malegori A. Double frequency Nd:YAG laser vs. argon green laser in the treatment of proliferative diabetic retinopathy: Randomized study with long term follow up. Lasers Surg Med. 1996;19(2):173-176. https://doi.org/10.1002/(sici)1096-9101(1996)19:2<173::aid-lsm8>3.3.co;2-c
- Macarie S, Macarie D. Efficacity of diode laser photocoagulation in retinal neovascularization treatment in diabetic retinopathy. Oftalmologia. 2002;53(2):89-92.
- The Royal College of Ophthalmology Retinal Vein Occlusion (RVO) Guidelines 2015. https://www.rcophth.ac.uk/wp-content/uploads/2015/07/Retinal-Vein-Occlusion-RVO-Guidelines-July-2015.pdf
- Rehak M, Tilgner E, Franke A, Rauscher F, Brosteanu O, Wiedemann P. Early peripheral laser photocoagulation of nonperfused retina improves vision in patients with central retinal vein occlusion (Results of a proof of concept study). Graefes Arch Clin Exp Ophthalmol. 2013;252(5):745-752. https://doi.org/10.1007/s00417-013-2528-8
- Spaide R. Рrospective study of peripheral panretinal photocoagulation of areas of nonperfusion in central retinal vein occlusion. Retina. 2013;33(1):56-62. https://doi.org/10.1097/iae.0b013e3182641875
- Michels R, Gass J. Тhe natural course of retinal branch vein obstruction. Retina. 1991;11(1):12-23. https://doi.org/10.1097/00006982-199111010-00003
- McIntosh R, Rogers S, Lim L et al. Natural History of Central Retinal Vein Occlusion: An Evidence-Based Systematic Review. Ophthalmology. 2010;117(6):1113-1123.e15. https://doi.org/10.1016/j.ophtha.2010.01.060
- Bloom S. Laser Surgery Of The Posterior Segment. Philadelphia: Lippincott; 1991.
- Akduman L, Olk R. Diode Laser (810 nm) versus Argon Green (514 nm) Modified Grid Photocoagulation for Diffuse Diabetic Macular Edema. Ophthalmology. 1997;104(9):1433-1441. https://doi.org/10.1016/s0161-6420(97)30119-5
- Browning D, Antoszyk A. The effect of the surgeon and the laser wavelength on the response to focal photocoagulation for diabetic macular edema. Ophthalmology. 1999;106(2):243-248. https://doi.org/10.1016/s0161-6420(99)90063-5
- Saeed M, Parmar D, McHugh D. Frequency-doubled Nd:YAG laser for the treatment of exudative diabetic maculopathy. Eye. 2001;15(6):712-718. https://doi.org/10.1038/eye.2001.235
- Lee CM, Olk RJ, Akduman L. Combined modified grid and panretinal photocoagulation for diffuse diabetic macular edema and proliferative diabetic retinopathy. Ophthalmic Surg Lasers. 2000;31(4):292-300.
- Parodi M, Spasse S, Iacono P, Di Stefano G, Canziani T, Ravalico G. Subthreshold Grid Laser Treatment of Macular Edema Secondary to Branch Retinal Vein Occlusion with Micropulse Infrared (810 Nanometer) Diode Laser. Ophthalmology. 2006;113(12):2237-2242. https://doi.org/10.1016/j.ophtha.2006.05.056
- Akduman L, Olk RJ. Subthresold (invisible) modified grid diode laser photocoagulation in diffuse diabetic macular edema. Ophthalmic Surg Lasers. 1999;9:706-714.
- Brown DM, Heier JS, Clark WL, Boyer DS, Vitti R, Berliner AJ, Zeitz O, Sandbrink R, Zhu X, Haller JA. Intravitreal aflibercept injection for macular edema secondary to central retinal vein occlusion: 1-year results from the phase 3 COPERNICUS study. Am J Ophthalmol. 2013;155(3):429-437.e7. https://doi.org/ 10.1016/j.ajo.2012.09.026
- Varma R, Bressler N, Suñer I et al. Improved Vision-Related Function after Ranibizumab for Macular Edema after Retinal Vein Occlusion. Ophthalmology. 2012;119(10):2108-2118. https://doi.org/10.1016/j.ophtha.2012.05.017
- Epstein D, Algvere P, von Wendt G, Seregard S, Kvanta A. Benefit from Bevacizumab for Macular Edema in Central Retinal Vein Occlusion: Twelve-Month Results of a Prospective, Randomized Study. Ophthalmology. 2012;119(12):2587-2591. https://doi.org/10.1016/j.ophtha.2012.06.037
- Wroblewski J, Wells J, Adamis A et al. Pegaptanib Sodium for Macular Edema Secondary to Central Retinal Vein Occlusion. Archives of Ophthalmology. 2009;127(4):374-80. https://doi.org/10.1001/archophthalmol.2009.14
- Shah N, Shah U. Long-term effect of early intervention with single intravitreal injection of bevacizumab followed by panretinal and macular grid photocoagulation in central retinal vein occlusion (CRVO) with macular edema: A pilot study. Eye. 2011;25(2):239-244. https://doi.org/10.1038/eye.2010.225
- Donati S, Barosi P, Bianchi M, Al Oum M, Azzolini C. Combined intravitreal bevacizumab and grid laser photocoagulation for macular edema secondary to branch retinal vein occlusion. EJO. 2011;22(4):607-614. https://doi.org/10.5301/ejo.5000085
- Algvere P, Epstein D, von Wendt G, Seregard S, Kvanta A. Intravitreal bevacizumab in central retinal vein occlusion: 18-month results of a prospective clinical trial. EJO. 2011;21(6):789-795. https://doi.org/10.5301/ejo.2011.6522
- Funk M, Kriechbaum K, Prager F et al. Intraocular Concentrations of Growth Factors and Cytokines in Retinal Vein Occlusion and the Effect of Therapy with Bevacizumab. Investigative Opthalmology & Visual Science. 2009;50(3):1025. https://doi.org/10.1167/iovs.08-2510
- Stahl A, Struebin I, Hansen L, et al. Bevacizumab in central retinal vein occlusion: a retrospective analysis after 2 years of treatment. European Journal of Ophthalmology. 2010;20(1):180-185.
- Campochiaro P, Heier J, Feiner L et al. Ranibizumab for Macular Edema following Branch Retinal Vein Occlusion. Ophthalmology. 2010;117(6):1102-1112.e1. https://doi.org/10.1016/j.ophtha.2010.02.021
- Brown DM. Clinical implications of the BRAVO and CRUISE trials. Retina Today. 2010;5:38-40.
- Haller J, Dugel P, Weinberg D, Chou C, Whitcup S. Evaluation Of The Safety And Performance Of An Applicator For A Novel Intravitreal Dexamethasone Drug Delivery System For The Treatment Of Macular Edema. Retina. 2009;29(1):46-51. https://doi.org/10.1097/iae.0b013e318188c814
- Scott I, VanVeldhuisen P, Oden N et al. SCORE Study Report 1: Baseline Associations between Central Retinal Thickness and Visual Acuity in Patients with Retinal Vein Occlusion. Ophthalmology. 2009;116(3):504-512. https://doi.org/10.1016/j.ophtha.2008.10.017
- Haller J, Bandello F, Belfort R et al. Randomized, Sham-Controlled Trial of Dexamethasone Intravitreal Implant in Patients with Macular Edema Due to Retinal Vein Occlusion. Ophthalmology. 2010;117(6):1134-1146.e3. https://doi.org/10.1016/j.ophtha.2010.03.032
- Moraczewski A, Lee R, Palmberg P, Rosenfeld P, Feuer W. Outcomes of treatment of neovascular glaucoma with intravitreal bevacizumab. British Journal of Ophthalmology. 2008;93(5):589-593. https://doi.org/10.1136/bjo.2008.151472
- Kofoed P, Munch I, Larsen M. Profound retinal ischaemia after ranibizumab administration in an eye with ocular ischaemic syndrome. Acta Ophthalmologica. 2009;88(7):808-810. https://doi.org/10.1111/j.1755-3768.2009.01612.x
- Quaggin S. Turning a blind eye to anti-VEGF toxicities. Journal of Clinical Investigation. 2012;122(11):3849-3851. https://doi.org/10.1172/jci65509
- Dınc E, Yıldırım O, Necat Yılmaz S et al. Intravitreal bevacizumab effects on VEGF levels in distant organs: an experimental study. Cutaneous and Ocular Toxicology. 2013;33(4):275-282. https://doi.org/10.3109/15569527.2013.855227
- Matsuyama K, Ogata N, Matsuoka M, Wada M, Takahashi K, Nishimura T. Plasma levels of vascular endothelial growth factor and pigment epithelium-derived factor before and after intravitreal injection of bevacizumab. British Journal of Ophthalmology. 2010;94(9):1215-1218. https://doi.org/10.1136/bjo.2008.156810
- Papadopoulou D, Mendrinos E, Mangioris G, Donati G, Pournaras C. Intravitreal Ranibizumab May Induce Retinal Arteriolar Vasoconstriction in Patients with Neovascular Age-related Macular Degeneration. Ophthalmology. 2009;116(9):1755-1761. https://doi.org/10.1016/j.ophtha.2009.03.017
- Mete A, SaygiÌ O, Mete A, Bayram M, BekiÌ N. Effects of intravitreal bevacizumab (Avastin) therapy on retrobulbar blood flow parameters in patients with neovascular age-related macular degeneration. J Clin Ultrasound. 2009:NA-NA. https://doi.org/10.1002/jcu.20650
- Nishijima K, Ng Y, Zhong L et al. Vascular Endothelial Growth Factor-A Is a Survival Factor for Retinal Neurons and a Critical Neuroprotectant during the Adaptive Response to Ischemic Injury. The American Journal of Pathology. 2007;171(1):53-67. https://doi.org/10.2353/ajpath.2007.061237
- Adelman R, Parnes A, Michalewska Z, Parolini B, Boscher C, Ducournau D. Strategy for the Management of Diabetic Macular Edema: The European Vitreo-Retinal Society Macular Edema Study. BioMed Research International. 2015;2015:1-9. https://doi.org/10.1155/2015/352487
- Park D, Kim I. Long-Term Effects Of Vitrectomy And Internal Limiting Membrane Peeling For Macular Edema Secondary To Central Retinal Vein Occlusion And Hemiretinal Vein Occlusion. Retina. 2010;30(1):117-124. https://doi.org/10.1097/Iae.0b013e3181bced68
- Raszewska-Steglinska M, Gozdek P, Cisiecki S, Michalewska Z, Michalewski J, Nawrocki J. Pars plana vitrectomy with ILM peeling for macular edema secondary to retinal vein occlusion. Eur J Ophthalmol. 2009; 19(6):1055-1062.
- Kumagai K, Furukawa M, Ogino N, Larson E, Uemura A. Long-Term Visual Outcomes After Vitrectomy For Macular Edema With Foveal Hemorrhage In Branch Retinal Vein Occlusion. Retina. 2007;27(5):584-588. https://doi.org/10.1097/01.iae.0000249576.98520.25
- DeCroos F, Shuler R, Stinnett S, Fekrat S. Pars Plana Vitrectomy, Internal Limiting Membrane Peeling, and Panretinal Endophotocoagulation for Macular Edema Secondary to Central Retinal Vein Occlusion. American Journal of Ophthalmology. 2009;147(4):627-633.e1. https://doi.org/10.1016/j.ajo.2008.10.024
- Arai M, Yamamoto S, Mitamura Y, Sato E, Sugawara T, Mizunoya S. Efficacy of Vitrectomy and Internal Limiting Membrane Removal for Macular Edema Associated with Branch Retinal Vein Occlusion. Ophthalmologica. 2009;223(3):172-176. https://doi.org/10.1159/000197113
Источник
Обзор посвящен возможностям использования фибринолитиков в лечении окклюзии центральной вены сетчатки и ее ветвей. В настоящее время с этой целью наиболее часто используют тканевой активатор плазминогена и проурокиназу. Представлены результаты клинических исследований, свидетельствующие о высоком уровне эффективности и безопасности применения данной группы препаратов.
В настоящее время патология сетчатки, приводящая к стойкому снижению зрения, слабовидению и инвалидности, является актуальной медико-социальной проблемой. Окклюзии центральной вены сетчатки (ЦВС) и ее ветвей являются одной из ведущих причин стойкого снижения зрения. Они занимают второе место после диабетической ретинопатии по частоте встречаемости среди сосудистой патологии сетчатки, приводящей к снижению зрительных функций [1]. По данным K.A. Ponto at al. (2015), распространенность острых нарушений кровообращения в венозном русле сетчатки среди людей в возрасте 35–74 лет составляет 4,0 на 1000 человек. Частота встречаемости окклюзий ЦВС составляет 0,8 случая на 1000, тогда как распространенность окклюзии ветвей ЦВС – 3,2 на 1000 [2]. При этом, согласно исследованию С.Н. Тульцевой, проведенному в 2009 г. в Северо-Западном регионе, в 59% случаев данное заболевание встречается у лиц старше 60 лет, в 39% – в возрастной группе 41–60 лет и только в 2% случаев – у лиц моложе 40 лет. Следует, однако, отметить тенденцию к определенному «омоложению» заболевания: в аналогичном исследовании, проведенном С.Н. Тульцевой в том же регионе в 2000 г., распределение пациентов по возрасту составляло 74%, 25% и 1% соответственно [3]. Данные о заболеваемости в зависимости от пола противоречивы. Так, R. Klein et al. (2000) указывают на отсутствие «полового предпочтения» у данного заболевания, в то время как исследования С.Н. Тульцевой (2010) свидетельствуют о преобладании женщин (60–66%), а данные K.A. Ponto еt al. (2015) – о столь же заметном преобладании мужчин (63%) [2–5].
В отличие от артериальных окклюзий [6] расстройства венозного кровообращения сетчатки вследствие присущих венам анатомо-физиологических особенностей обусловлены в основном тромботическим процессом [7]. Тромбоз центральной вены сетчатки сходен по характеру своего развития с венозным тромбозом другой локализации [8]. Причинами его являются повреждения стенки сосуда и стаз крови, происходящие на фоне дисбаланса свертывающей и противосвертывающей систем крови [3, 9]. Значительную роль в патогенезе данных патологических изменений играют местные факторы. В области сосудистых аркад, а также за решетчатой пластинкой склеры артериальные и венозные сосуды имеют общую адвентицию. В случае атеросклероза стенки артериолы, а также повышенного артериального давления происходит компрессия вены в области артериовенозного перекреста, приводящая к сужению ее просвета и замедлению тока крови. Также возможны возникновение турбулентного тока крови и повреждение эндотелия с последующим формированием тромба [3].
Процесс тромбообразования последовательно проходит три стадии. Первая заключается в прилипании (адгезии) тромбоцитов непосредственно к поврежденному эндотелию или к волокнам коллагена, которые выступают в просвет сосуда после повреждения его эндотелия. На второй стадии происходят скопление (агрегация) кровяных пластинок у места повреждения стенки сосуда и выделение ими ряда биологически активных веществ, в т. ч. сосудосуживающих. В результате просвет пораженного сосуда сужается и перекрывается массой тромбоцитов [10]. Следует отметить, что при лечебном воздействии на первых двух стадиях процесс тромбообразования может быть обратимым [11].
На третьей стадии тромбообразования достаточную силу набирают коагуляционные процессы, в результате которых образуется фибрин, который опутывает тромбоциты, лейкоциты и эритроциты [10]. Затем происходит ретракция кровяного сгустка, и формирование тромба завершается. Третья стадия в химическом отношении уже является необратимой [11]. Через 7–14 дней в тромб начинают внедряться фибробласты, эндотелиальные и воспалительные клетки. В итоге происходит организация тромба – замещение его васкуляризированной соединительной тканью. Мигрировавшие эндотелиальные клетки в это время формируют коллатерали, которые способствуют частичному восстановлению кровотока. Этот процесс занимает от 3 до 8 мес. [9–11].
Растворение внутрисосудистых тромбов происходит под действием плазмина, который катализирует протеолитическую деградацию фибрина с образованием растворимых продуктов, что приводит к восстановлению кровотока. Плазмин образуется в результате активации его предшественника плазминогена под действием ряда биологически активных веществ. Различают два пути активации плазминогена: внутренний и внешний. Внутренний механизм осуществляется благодаря плазменным активаторам и активаторам форменных элементов крови. Активация плазминогена по внешнему пути осуществляется за счет тканевого активатора плазминогена (tРА), поступающего из эндотелия сосудов, а также урокиназы, синтезируемой фибробластами, моноцитами/макрофагами и эндотелиальными клетками (рис. 1) [12, 13].
В настоящее время имеется большое количество отечественных и зарубежных исследований, посвященных патогенетическому лечению тромбозов ЦВС и ее ветвей при помощи фибринолитиков [4, 14–22]. Основной целью применения препаратов данной группы служит лизис тромба, приведшего к окклюзии ЦВС в стволе зрительного нерва или в области решетчатой пластинки склеры, либо ветви ЦВС в области артериовенозного перекреста, что является важнейшим условием восстановления ретинального кровотока. Даже в случаях развития необратимых изменений в сетчатке быстрое восстановление проходимости ЦВС за счет лизиса тромба может предотвратить дальнейшее снижение зрительных функций и развитие осложнений тромбоза [17, 23].
Исходя из патофизиологии развития тромбоза применение препаратов с целью тромболизиса может быть эффективным только в первые 7–14 дней после острого нарушения кровообращения в венозном русле, что подтверждается данными отечественных и зарубежных исследований [3, 9, 14, 24–26]. Вместе с тем фибринолитики при интраокулярном применении даже на поздних сроках после тромбоза в бассейне ЦВС в части случаев способны индуцировать отслойку задней гиалоидной мембраны, что, в свою очередь, способствует уменьшению отека сетчатки и улучшению зрительных функций [22, 27–30].
В зарубежных исследованиях в лечении окклюзий ЦВС и ее ветвей наиболее часто используют препараты уже упомянутого выше тканевого активатора плазминогена (tРА) при разных способах их введения; tРА активируется при связывании с фибрином и индуцирует превращение плазминогена в плазмин, который и расщепляет фибриновый сгусток [13]. Ряд исследований свидетельствуют о высоком уровне эффективности и безопасности этого препарата в лечении тромбозов ЦВС [14, 19–22, 31]. Недостатком tРА при его интраокулярном введении является большой молекулярный вес (70 кДа), что несколько замедляет его трансретинальное проникновение [17]. Кроме того, имеются данные и о его токсическом воздействии на сетчатку, притом усиливающемся при наличии тромбоза ЦВС [32–34].
В практике отечественных офтальмологов при остром нарушении кровоснабжения в венозном русле сетчатки чаще используют препарат рекомбинантной проурокиназы человека [4, 15–18]. Проурокиназа обладает рядом преимуществ по сравнению с препаратами tPA. Так, при применении проурокиназы наблюдается низкий риск ретромбозов (до 5%). К тому же препарат не индуцирует гиперкоагуляцию [35–37]. Кроме того, обладая более низким по сравнению с tPA молекулярным весом (54 кДа), при местном интраокулярном введении проурокиназа быстрее проникает в венозную систему сетчатки [17]. Однако ввиду отсутствия полноценных контролируемых исследований вопрос сравнительной эффективности этих двух фибринолитиков до сих пор остается открытым.
Вместе с тем при системном применении проурокиназа обладает (по сравнению с tPA) и рядом недостатков. Так, было показано, что в терапевтических концентрациях в плазме проурокиназа индуцирует системный фибринолиз, что значительно повышает риск кровотечений [35]. Кроме того, имеются данные и о том, что внутривенное введение больших доз нативной немодифицированной проурокиназы может повлиять на вероятность активизации и метастазирования опухолей [38–41]. Однако перечисленные нежелательные эффекты проурокиназы проявляются, по всей видимости, только при ее системном применении и достижении терапевтической или более высокой концентрации в плазме крови. Что касается местного применения проурокиназы в офтальмологии, то сведений о подобных эффектах как в литературе, так и в наших клинических наблюдениях пока не обнаружено.
Важно отметить, что в препарате рекомбинантной проурокиназы человека используется не природная проурокиназа, а фермент, относящийся к классу модифицированных проурокиназ с измененным N-концевым рецептор-связывающим доменом [28]. Имеются сведения о том, что эти модифицированные протеазы, в отличие от их природной формы, не связываются с урокиназными рецепторами на поверхности клеток и, следовательно, не участвуют в процессах миграции и ремоделирования тканей, в т. ч. в активизации процесса метастазирования опухолей [28, 38].
Многочисленные отечественные и зарубежные исследования посвящены применению фибринолитиков при тромбозах ЦВС с использованием различных путей введения [4, 9, 15–17, 25, 42–44].
Так, ряд исследований был посвящен анализу эффективности и безопасности системного введения таким больным различных препаратов рассматриваемой группы, в частности, фибринолизина, стрептокиназы, tPA и др. [9, 25, 42–44]. Исследователи отметили повышение остроты зрения пораженного глаза в течение нескольких месяцев, что свидетельствует об эффективности системного применения фибринолитиков. Однако данная методика так и не получила широкого распространения вследствие высокой вероятности развития системных геморрагических осложнений.
В то же время в большинстве современных исследований предпочтение закономерно отдается местному применению фибринолитиков, позволяющему добиться высокой концентрации препарата в зоне локализации тромботического процесса при минимальном риске развития системных побочных эффектов.
В отечественной офтальмологии, как известно, наиболее распространенными методами инъекционного введения ферментов являются субконъюнктивальный, пара- и ретробульбарный [4, 7]. Их преимущество состоит в малой травматичности и высокой доступности для практикующего врача, в т. ч. и в амбулаторном звене офтальмологической помощи. Однако необходимость преодоления ферментом барьера в виде фиброзной капсулы глаза служит причиной недостаточной эффективности рассматриваемых методов и обусловливает необходимость разработки и внедрения в практику альтернативных способов введения ферментных препаратов. При этом особого внимания заслуживают ряд методов подведения лекарственного вещества максимально близко к зоне локализации тромба в венозном русле сетчатки: интравитреальные инъекции, канюлирование ретинальной вены, а также суб- и эпиретинальное его введение [17].
В частности, С.В. Сдобниковой с соавт. (2007) предложен способ лечения тромбоза ЦВС [17], заключающийся в проведении витрэктомии (в т. ч. с пилингом внутренней пограничной мембраны) совместно с канюлированием ретинальной вены. Эта методика позволяет под визуальным контролем ввести тромболитический препарат максимально близко к месту окклюзии, что обеспечивает высокую концентрацию препарата непосредственно в зоне формирования тромба. Кроме того, в ходе этого вмешательства осуществляется механическое воздействие на тромб турбулентным током раствора фибринолитика, что также может привести к его смещению в проксимальном направлении [17]. К недостаткам метода относятся его относительная техническая сложность, а также потребность в дорогостоящем специальном оборудовании (микроманипулятор и микроинжектор) для обеспечения дозированной инфузии препарата. Велик также и риск достаточно серьезных осложнений такой операции: развития гемофтальма в ходе сквозной перфорации сосуда, а также повреждения и отслойки сетчатки [17, 45–49].
Достаточно оригинальным способом интраокулярного введения фибринолитического препарата также является его субретинальная инъекция, осуществляемая из витреальной полости после витрэктомии в сочетании с газожидкостным обменом [17, 30, 50]. Фибринолитик вводят в перипапиллярную область, где таким путем создается депо препарата. В дальнейшем трансневрально и с остаточным кровотоком через ретинальные капилляры происходит постепенное проникновение тромболитика к месту окклюзии. Данный способ введения препарата позволяет достичь его высокой концентрации в зоне тромбоза, однако все же обладает рядом недостатков. К ним, в частности, относятся риск механического повреждения нейроэпителия и нервных волокон в перипапиллярной области при отслаивании сетчатки вводимым препаратом и повышение вероятности проявления ретинотоксического эффекта последнего.
Несколько менее инвазивна методика, включающая проведение субтотальной витрэктомии, выполнение стандартной процедуры газожидкостного обмена и эпиретинальное введение фибринолитика [17, 51–53]. Однако и этот метод оказался не лишенным недостатков, одним из которых явилась большая вероятность проявления токсического эффекта фибринолитика за счет его воздействия в высокой концентрации на макулярную и перипапиллярную области сетчатки [17]. Также в ходе проведения рассматриваемых исследований в ряде случаев были отмечены такие свойственные витреальным хирургическим вмешательствам осложнения, как гемофтальм и формирование эпиретинальных мембран [52, 53].
Также описан способ суперселективного введения раствора фибринолитика в arteria ophthalmica. Процедура проводилась под местной анестезией в отделении нейрорадиологии специалистом по катетеризации интракраниальных сосудов. Техника манипуляции заключается в следующем. Через бедренную артерию проводится катетеризация внутренней сонной артерии катетером диаметром 5 Fr, после чего выполняется ангиография для локализации места изгиба arteria carotis interna. Затем катетер перемещают в проксимальную экстракраниальную часть внутренней сонной артерии. Далее микрокатетер диаметром 1,8 Fr или 1,5 Fr проводят в устье arteria ophthalmica и вновь выполняют ангиографию, чтобы удостовериться в правильности положения микрокатетера, после чего осуществляют медленную инфузию раствора фибринолитика в течение 40 мин. Вся процедура занимает около 1 ч, а после ее завершения пациенту показан строгий постельный режим в течение 12–24 ч. Помимо очевидной технической сложности данной процедуры следует отметить, что в послеоперационном периоде у части пациентов отмечались местные геморрагические осложнения в виде интраретинальных кровоизлияний и гемофтальма [54].
В силу рассмотренных обстоятельств упомянутые методы доставки фибринолитических препаратов к месту локализации тромба так и не получили широкого практического применения.
В настоящее время при лечении окклюзий ЦВС и ее ветвей из методов внутриглазного введения препарата наиболее часто используется техника интравитреальной инъекции фибринолитика (500 МЕ проурокиназы или 50 мкг tPA) через плоскую часть цилиарного тела. В ходе манипуляции на первом этапе проводят эпибульбарную анестезию и закапывают 5–10% раствор поливидон-йода. Затем инъекционную иглу диаметром 30G или даже тоньше вводят внутрь глаза перпендикулярно склере на отдалении 3,5–4 мм от лимба между зонами прикрепления вертикальной и горизонтальной прямых мышц и инъецируют раствор препарата в стекловидное тело [55]. При использовании этого пути введения препарат диффундирует через внутреннюю пограничную мембрану сетчатки и проникает в венозную систему через капилляры, поврежденные при тромбозе в результате нарушения гематоретинального барьера. Далее, с остаточным венозным кровотоком, препарат достигает места окклюзии ЦВС или ее ветви и вызывает лизис находящегося там тромба. Достоинствами данного метода являются его техническая простота и относительно небольшая травматичность [17, 55, 56]. Однако имеются сведения, что интравитреальное введение фибринолитика может все же привести к развитию геморрагических осложнений и способствовать усилению макулярного отека за счет лизиса мелких вторичных тромбов на уровне ретинальных капилляров с последующим повышением венозного давления (при сохранении окклюзии ЦВС) и усилением экссудации [17]. Кроме того, при любой интравитреальной инъекции существует риск повреждения хрусталика, а также развития эндофтальмита и отслойки сетчатки. Тем не менее описанные осложнения встречаются достаточно редко, и, к тому же, большинство из них может быть предотвращено. В частности, частота развития эндофтальмита после интравитреальных инъекций различных препаратов сегодня не превышает 0,05% [55, 57]. При этом целый ряд отечественных и зарубежных исследователей отмечают высокую эффективность и относительную безопасность данного метода лечения [4, 14–16, 18–23, 56].
В целом необходимо отметить, что применение фибринолитических препаратов в терапии тромбозов ЦВС и ее ветвей является патогенетически оправданным. Многочисленные отечественные и зарубежные исследования свидетельствуют об эффективности и высоком профиле безопасности данной группы лекарственных средств, прежде всего tPA и проурокиназы, при их местном внутриглазном введении. Наиболее эффективным является применение данных препаратов в течение первых 7–14 дней от момента сосудистой катастрофы за счет полного или частичного тромболизиса, однако и в более поздние сроки их использование также может быть оправданно в целях индуцирования отслойки задней гиалоидной мембраны и последующего уменьшения отека сетчатки.
Сведения об авторах: Баранов Андрей Юрьевич – врач-офтальмолог; Бржеский Владимир Всеволодович – д.м.н., профессор. ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России. 194100, Санкт-Петербург, ул. Литовская, 2. Контактная информация: Баранов Андрей Юрьевич, e-mail: homeandrey@rambler.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 05.09.2017.
About the authors: Andrei Yu. Baranov – ophthalmologist; Vladimir V. Brzhesky — professor. Saint Petersburg State Medical Pediatric University. 2, Lithuanian Str., Saint Petersburg, 194100, Russian Federation. Contact information: Andrei Yu. Baranov, e-mail: homeandrey@rambler.ru. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 05.09.2017.
Источник