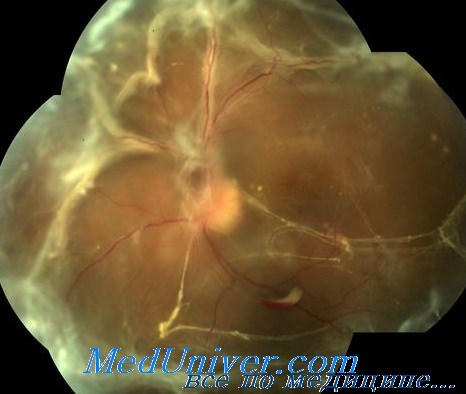
Пвр это отслойка сетчатки
Что такое пролиферативная витреоретинопатия (ПВР)? Причины, механизмы развитияПролиферативная витреоретинопатия (ПВР) можно рассматривать как репаративный или рубцовый процесс. Вследствие механического повреждения тканей, таких как ПЭС, происходит миграция, сморщивание и умеренная пролиферация клеток. Дефект ВПМ может возникнуть в результате воздействия СТ, образования разрывов сетчатки или проведения диссекции мембраны. Затем происходит миграция и умеренная пролиферация глиальных клеток, а также контракция сетчатки, подобно репарации дефекта между ВПМ и сетчаткой. По такому механизму происходит «заживление» разрывов сетчатки, что будет подробно описано в главах, посвященных хирургическому лечению макулярных отверстий и выполнению рети-нотомии во время субмакулярных хирургических вмешательств. Аналогично тому, что происходит при отслойке сетчатки от ПЭС, клетки ПЭС мигрируют на поверхность сетчатки и заднюю поверхность стекловидное тело (СТ). При наличии воспалительного процесса моноциты из капилляров радужной оболочки и цилиарного тела могут мигрировать к поверхности сетчатки, пролиферировать и оседать на ней. Глиальные клетки, клетки ПЭС и моноциты мигрируют вдоль нормальных анатомических структур и новообразованных тканей, при этом происходит сокращение их внутриклеточного матрикса, что приводит к образованию тангенциальных тракций на сетчатку. Результаты проведенных исследований показывают, что во время заживления в микроканальцах во множестве клеток одновременно развивается процесс, аналогичный гладкомышечному сокращению. В миофибробластах имеются закрытые углубления, в которых располагаются специальные рецепторы к коллагену, фибрину и эластину. Эти углубления содержат фибронектин, который позволяет клеткам присоединяться к коллагеновым волокнам. Факторы роста (ТФР-b и др.), металлопротеиназы, фибронектин и рецепторы коллагена, эластина и фибрина участвуют в патогенезе миграции и сокращения; пролиферация (митотическая активность) имеет гораздо меньшее значение. Этот процесс можно рассматривать как гипоцеллюлярное периретинальное рубцевание, аналогичное гипоцеллюлярному сокращению СТ. Пролиферативная витреоретинопатия (ПВР) является не совсем корректным термином, так как при ее наличии присутствует минимальная митотическая активность и антиметаболиты для ее лечения неэффективны, по сути пролиферативная витреоретинопатия (ПВР) аналогична образованию келоидных рубцов. Чтобы подчеркнуть гипоцеллюлярный характер данного процесса, авторы статьи предлагают исключить определение «пролиферативная» из названия «пролиферативная витреоретинопатия». Как и при формировании келоидных рубцов, пролиферативная витреоретинопатия (ПВР) является следствием чрезмерной репарации или избыточного рубцевания. Процесс рубцевания биологически идентичен процессу заживления; он в основном характеризуется функциональными свойствами. Пролиферативную витреоретинопатию (ПВР) следует рассматривать как гипоцеллюлярное взаимодействие между различными типами клеток и внеклеточным матриксом. В патогенезе участвуют клетки ПЭС, глиальные клетки и клетки воспаления.
Лучшее понимание патогенеза данного процесса позволяет выбрать более эффективную стратегию лечения; чрезмерная лазерная коагуляция сетчатки стимулирует развитие пролиферативной витреоретинопатии (ПВР), короткий интервал между хирургическими вмешательствами также является распространенной причиной ее развития. Большая продолжительность хирургического вмешательства, обширная лазерная коагуляция сетчатки, травмы радужки (ирис-ретракторами), комбинация факоэмульсификации с имплантацией ИОЛ, а также чрезмерный пилинг ЭРМ на периферии сетчатки вместо выполнения ретинэктомии могут стать причиной ятрогенной пролиферативной витреоретинопатии (ПВР). В отличие от хирургического лечения онкологической патологии или дренирования абсцесса, целью оперативного лечения при витреоретинальных вмешательствах является минимальное повреждение, а не удаление всех патологических тканей. Хирург, оперирующий пролиферативную витреоретинопатию (ПВР), должен мыслить как пластический хирург, а не как хирург-онколог. Тангенциальное сокращение клеток происходит до образования коллагена, продукцию которого можно рассматривать как позднюю фазу стабилизации. Образование базальной мембраны и коллагена можно рассматривать как восстановление мембраны Бруха или ВПМ, подобно повторению процесса, происходящего при эмбриональном развитии. Пролиферативная витреоретинопатия (ПВР) может выглядеть, как изолированные звездчатые складки, фиксированные складки сетчатки, субретинальные изменения или ЭММ. Пролиферативная витреоретинопатия (ПВР) может быть более обширной, что дает основания описывать ее не использующимся в настоящее время термином «массивная периретинальная пролиферация». Если пролиферация глиальных клеток или клеток ПЭС распространяется на смежное заднее основание стекловидного тела, процесс можно описывать устаревшим термином «массивное сокращение СТ». В настоящее время нет доказательств роли гиалоцитов в патогенезе ПВР. Знание анатомии играет важнейшую роль в адекватном выполнении хирургического вмешательства. При центральной витрэктомии на самом деле производится устранение слияния заднего основания стекловидного тела и переднего основания стекловидного тела во фронтальной плоскости, а не сферическая центральная витрэктомия. Важно напомнить, что основание стекловидного тела не объемное и не может быть «срезано», как утверждают некоторые хирурги, оно является зоной соединения периферической части СТ и сетчатки. Часто хирурги заявляют, что они выполняют диссекцию основания СТ, но в данном случае это не так, хотя на самом деле важно выполнить так называемое иссечение периферической части СТ в непосредственной близости от поверхности сетчатки. Круговые коллагеновые волокна СТ укорачиваются из-за гипоцеллюлярного сокращения, подтягивая экватор внутрь; эти волокна, прилежащие к основанию СТ, редко поддаются удалению методом пилинга. Коллагеновые волокна СТ, ориентированные в переднезаднем направлении, смежные с основанием СТ, также укорачиваются из-за гипоцеллюлярного сокращения, вызывая тракцию передней петли (так ее первым описал S.Charles), резекция этого компонента передней ПВР имеет большое значение для уменьшения передних тракций экваториальной области сетчатки. ЭММ всегда находятся кзади от заднего края основания стекловидного тела; «пилинг периферических ПВР-мембран» также является некорректным термином. Рубцы в субретинальном пространстве могут возникать во многих случаях, как описано выше. Пластинчатая конфигурация может привести к образованию субретинальной мембраны в виде перевернутой звезды. Субретинальная полосчатая (нитевидная) пролиферация формируется, вероятно, в виде тяжей клеток ПЭС вдоль нитей фибрина, которые затем сокращаются, что приводит к созданию обширной дендритной конфигурации. Если эти тяжи расположены по окружности на уровне средних слоев сетчатки, может возникать кольцевая конфигурация субретинального рубца, которая приведет к отслойке сетчатки в виде замкнутого конуса. — Также рекомендуем «Операбельность пролиферативной витреоретинопатии (ПВР). Выбор метода операции» Оглавление темы «Операции при патологии сетчатки»:
|
Источник
Захаров В.Д., Курцхалидзе К.Д.
Отслойка сетчатки (ОС) была и остается тяжелым заболеванием глаза, при котором трудно предсказать эффективность лечения, особенно когда это касается тяжелых отслоек сетчатки с наличием пролиферативной витреоретинопатии (ПВР). Современное развитие витреоретинальной хирургии позволило расширить показания к хирургическому лечению тяжелых форм ОС, в том числе считавшихся ранее неоперабельными. К этой категории ОС можно отнести ОС, при которых происходит фиброзное перерождение ткани сетчатки с образованием субретинальных и эпиретинальных мембран при наличии плотной фиксации патологическими сращениями с измененным стекловидным телом (СТ), что в конечном итоге препятствует ее прилеганию [2, 3].
На сегодняшний день основополагающим моментом в лечении этой тяжелой патологии глаза является тщательное освобождение сетчатки от сращений с пролиферативной тканью, особенно в области периферии глазного дна. К сожалению, это не всегда представляется возможным в силу выраженности изменений витреоретинальных структур из-за исходного тяжелого состояния глаза, предшествующих операций, наличия сопутствующей патологии и др. Все это заставляет искать новые способы хирургии тяжелых отслоек сетчатки. В связи с этим представляются перспективными способы хирургического лечения данной патологии с применением ретинотомии и ретинэктомии [1, 2, 5, 7, 8, 10, 11]. Тяжелые ОС, осложненные выраженной ПВР, часто требуют использования ретинотомии и ретинэктомии, что позволяет мобилизовать сетчатку и добиться ее анатомического прилегания. Однако, несмотря на положительные стороны ретинотомии и ретинэктомии, в ряде случаев само вмешательство провоцирует прогрессирование передней пролиферативной витреоретинопатии (ППВР) [6]. Несмотря на то, что в ближайшие дни после операции анатомический результат хирургии был положительный, в дальнейшем во многих случаях отмечали рецидив или развитие пролиферативного ответа с локализацией в области базального витреума (БВ). Развитие и прогрессирование пролиферативного процесса после ретинотомий в области БВ и цилиарного тела (ЦТ) приводит к отслойке ЦТ и, как следствие, к стойкой гипотонии глаза как в случаях нахождения силиконового масла (СМ) в полости глаза, так и в случаях после его удаления [3, 9, 11, 13, 14], что в конечном итоге ведет к субатрофии глаза. Таким образом, становится понятным, что сохранение пролиферативной активности вызывает риск повторной отслойки сетчатки.
Одним из дополнительных средств в комплексном хирургическом лечении тяжелых отслоек сетчатки с использованием круговой ретинотомии и ретинэктомии для профилактики репролиферации, которая является основной причиной рецидивов отслойки сетчатки, может быть применение техники малых разрезов 25G [4, 12]. В настоящее время при использовании инструментов 25G не требуются предварительные разрезы конъюнктивы, склеры, а используются троакары с надетыми на них специальными полиамидными трубками длиной 3,6 мм — «портами» для прокола склеры через конъюнктиву в плоской части цилиарного тела. Внутренний и наружный диаметр «портов» равен 0,57 мм и 0,62 мм, используемая при этом инфузионная канюля имеет диаметр 0,37 мм и 0,56 мм. Троакары затем удаляются, а в местах проколов склеры остаются «порты», которые обеспечивают доступ в витреальную полость. Арсенал инструментов 25G, имеющийся на вооружении витреоретинальных хирургов на сегодняшний день, а также взаимозаменяемость «портов» позволяют проводить витрэктомию при самых тяжелых патологиях сетчатки и стекловидного тела.
Технические трудности при витрэктомии на глазах с ПВР при регматогенных отслойках сетчатки преодолимы, и полученный опыт позволяет сказать, что витрэктомия 25G возможна во всех сложных случаях, где ранее применялась витрэктомия 20G.
Цель работы — повысить эффективность хирургического лечения отслоек сетчатки, требующих применения круговой ретинотомии и ретинэктомии.
Материал и методы
Прооперированы 43 пациента (43 глаза) с отслойками сетчатки, осложненными ПВР С-А тип 4, тип 5 (рис. 1). Все больные были разделены на две группы: в 1-й группе — 27 пациентов (27 глаз), которым проводилось хирургическое лечение с проведением круговой ретинотомии по стандартной методике с использованием инструментов 20G калибра; во 2-й группе — 16 пациентов (16 глаз), которым проводилось хирургическое лечение с проведением круговой ретинотомии по предлагаемой методике с применением инструментов 25G калибра по бесшовной технологии. Средний возраст пациентов составил 53 и 44 года соответственно. Основной причиной отслойки сетчатки в обеих группах являлась миопия, данные представлены в табл. 1.
Давность отслойки сетчатки в среднем составила от 3 до 6 мес. в группе с 20G и от 7 до 9 мес. — в группе с 25G (табл. 2).
Наиболее частой сопутствующей патологией была миопия в обеих группах, данные представлены в табл. 3. Предшествующие хирургические вмешательства указаны в табл. 4. Дооперационная острота зрения пациентов представлена в табл. 5, дооперационное поле зрения — в табл. 6, дооперационное ВГД — в табл. 7.
У всех больных, по данным УБМ, диагностирована ППВР. Всем пациентам выполняли полный набор исследований (острота зрения, кераторефрактометрия, тонометрия, тонография, периметрия, биомикроскопия, непрямая офтальмоскопия, биомикроофтальмоскопия, эхобиометрия, В-сканирование, ультразвуковая биомикроскопия, оптическая когерентная томография, электрофизиологические исследования сетчатки и зрительного нерва).
Техника хирургического вмешательства.
Одним из ключевых моментов в лечении пациентов с применением техники 25G (2 группа) было наличие артифакии или афакии, т.к. проведение круговой ретинотомии и ретинэктомии с тщательным удалением пролиферативной ткани на периферии на факичном глазу невозможно без повреждения хрусталика. Поэтому при наличии факичных глаз сначала проводили факоэмульсификацию катаракты с имплантацией ИОЛ (операции проводились как одномоментно, так и раздельно с эндовитреальным вмешательством), либо удаление хрусталика с капсульным мешком без имплантации ИОЛ при наличии миопии высокой степени.
Это касалось и тех случаев, когда хрусталик был прозрачный. Через три трансконъюнктивальных прокола в области плоской части цилиарного тела инструментами 25G калибра под углом 30O по отношению к склере, по направлению к лимбу с предварительным смещением конъюнктивы, устанавливаются полиамидные трубки-«порты» в нижнеенаружном сегменте глазного яблока (место для ирригацинной канюли) и на 9-10 и 2-3 ч, через которые в полость глаза вводят световод и витреотом (рис. 2).
Далее выполняли витрэктомию с последующим контрастированием стекловидного тела и задней гиалоидной мембраны (ЗГМ) кортикостероидами с обязательной отсепаровкой ЗГМ на максимально возможном протяжении. Удаление передних отделов стекловидного тела, передней гиалоидной мембраны (ПГМ), шварт, пролиферативной ткани на крайней периферии проводили с использованием склерокомпресии. Затем удаляли эпиретинальные мембраны с поверхности сетчатки, используя ретинальный шпатель. Следующим этапом по окружности, на границе прикрепления ЗГМ к сетчатке осуществляли эндокоагуляцию сосудов диатермокоагулятором, продолжая ее в радиальном направлении на 12, 3, 6, 9 ч (рис. 3). Затем проводили круговую ретинотомию по линии диатермокоагулятов витреотомом, сначала в круговом направлении (рис. 4), затем в радиальном (рис. 5).
Длина радиальных разрезов зависит от степени фиброзных изменений сетчатки и достигает уровня границы перехода фиброзно-измененной ткани сетчатки в неизмененную, в среднем достигая от 1 до 3 мм. Далее полностью удаляли остатки сетчатки с пролиферативной тканью на периферии, затем дополнительно использовали кортикостероиды для контрастирования задней поверхности сетчатки, удаляли субретинальную пролиферативную ткань. Далее вводили перфторорганическое соединение с целью расправления сетчатки. Выполняли эндолазеркоагуляцию сетчатки по краю ретинотомии в 2 ряда, затем еще 1 ряд эндолазеркоагулятов центральнее линии диатермокоагулятов (рис. 6). Затем после дополнительного введения перфторорганического соединения проводили обмен ПФОС на силикон.
При тампонаде применяли силиконовое масло 1300 сSt. Далее производили удаление «портов» без наложения швов. Во всех случаях удалось добиться интраоперационного прилегания сетчатки. Через 1,5-3 мес. СМ удаляли. В 1-й группе витрэктомия и все дальнейшие этапы операции проводятся через разрезы 20G калибра. После проведения витрэктомии выполняется круговая ретинотомия максимально периферично, производится «сбривание» стекловидного тела на максимально возможном протяжении к периферии сетчатки. В качестве тампонирующего средства применялось СМ 5700 сSt или 1000 сSt.
Результаты и обсуждение
Осложнения, возникшие в ходе операции, представлены в табл. 8. Как видно из этой таблицы, наиболее частым осложнением были геморрагии из ретинальных сосудов. В структуре интраоперационных осложнений меньший процент геморрагий и ятрогенных разрывов обусловлен более контролируемой витрэктомией при использовании инструментов 25G калибра. Складки сетчатки и транслокация макулы были обусловлены субретинальным фиброзом. Что касается осложнений в раннем послеоперационном периоде, то такие осложнения, как воспаление и геморрагии меньше встречались в группе с 25G за счет меньшего травмирования тканей глаза. Формирование разрезов при использовании системы 20G несет в себе повышенный риск развития геморрагий из сосудистой оболочки как на стадии формирования разрезов, так и во время наложения герметизирующих швов. Послеоперационная гипотония, связанная с гипофункцией цилиарного тела в ответ на операционную травму, чаще наблюдалась в группе с 20G (табл. 9).
Повышение ВГД в группе с 25G носило транзиторный характер и после применения гипотезивных капель в течение 1-3 дней нормализовалось. После соответствующей терапии осложнения удалось устранить на всех глазах, однако сроки лечения в группе с 20G были больше в среднем на 3-7 дней. В позднем послеоперационном периоде отмечается меньшее количество рецидивов и фиброза в группе с 25G (табл. 10). Срок наблюдений составил от 1 до 20 мес. По поводу рецидивов отслойки сетчатки проводилось повторное хирургическое лечение, с удалением ЭРМ и повторной тампонадой силиконовым маслом. Сроки силиконовой тампонады составили от 1 до 6 мес. в группе с 25G и от 1 до 19 мес. — в группе с 20G. Больший срок силиконовой тампонады связан с наличием эпиретинального фиброза и с большим риском развития отслойки сетчатки. Удаление силикона проводилось 10 пациентам (37 % случаев) в группе 20G, из них у 2 развился рецидив отслойки сетчатки; в группе с 25G удаление силикона проводилось 8 пациентам (50%), из них у 2 развился рецидив отслойки сетчатки, по поводу чего в обеих группах проводилось повторное хирургическое вмешательство с повторным введением силиконового масла. Причиной рецидивов в группе с 25G в одном случае был эпиретинальный фиброз, а в другом случае — новый разрыв; в группе 20G в одном случае был субретинальный фиброз, а в другом случае — новый разрыв.
Острота зрения с коррекцией составила от 0,02 до 0,1 в группе с 25G и от 0,002 до 0,1 — в группе с 20G в зависимости от исходного состояния и длительности отслойки сетчатки. Данные представлены в табл. 11.
Результаты исследования показывают, что ВГД было в среднем на уровне 15,1 мм рт.ст. на этапе силиконовой тампонады и 14,3 мм рт.ст. – после удаления силикона в группе с 20G. В группе с 25G ВГД было в среднем на уровне 17,9 мм рт.ст. на этапе силиконовой тампонады и 15,2 мм рт.ст. — после удаления силикона (рис. 7).
Использование витрэктомической системы 25G значительно снижает операционную травму при витреоретинальных вмешательствах, что привело к уменьшению воспаления в послеоперационном периоде и, как следствие, к уменьшению выраженности репролиферации. Как известно, пролиферация является конечной стадией любого воспаления, тем самым уменьшая интраоперационную травму и выраженность воспаления, мы уменьшаем тяжесть и агрессивность ПВР в послеоперационном периоде.
Тщательное удаление остатков ЗГМ на крайней периферии, удаление остатков периферических отделов сетчатки при ретинэктомии, участков пролиферативной ткани на периферии глазного дна являются патогенетически обоснованными при хирургии тяжелых отслоек сетчатки, осложненных ПВР. Уменьшая суммарную площадь остова для формирования и развития ПВР, мы тем самым уменьшаем массивность и плотность репролиферативной ткани. Концепция микроинвазивной и трансконьюнктивальной бесшовной хирургии имеет потенциал для увеличения эффективности при разной витреоретинальной патологии. Эта методика ускоряет послеоперационное восстановление и улучшает результаты, упрощая хирургическую процедуру, уменьшает интраоперационную травму и послеоперационную воспалительную реакцию, сокращая затраченное рабочее время хирурга и период выздоровления пациента.
Выводы
1. Применение круговой ретинотомии и ретинэктомии в лечении отслоек сетчатки, осложненных ПВР, позволяет в полной мере добиться мобилизации, адаптации и фиксации сетчатки.
2. Применение микроинвазивных методик в лечении отслоек сетчатки, осложненных ПВР, позволяет уменьшить интраоперационную травму, снижает выраженность воспалительной реакции, что в конечном итоге уменьшает количество рецидивов и улучшает качество лечения этой тяжелой категории пациентов.
3. Имеющийся на сегодняшний день набор инструментов 25G обеспечивает проведение всех этапов операции в необходимом объеме у пациентов с отслойкой сетчатки осложненной ПВР.
Поступила 14.07.08
Источник