Оптическая когерентная томография сетчатки oct
 Метод оптической когерентной томографии (optical coherence tomography, сокращенно ОСТ (eng.) или ОКТ (рус.)) представляет собой современное высокоточное неинвазивное исследование различных структур глаза. ОСТ является бесконтактным методом, позволяющим специалисту визуализировать ткани глаза с очень высоким разрешением (1 — 15 микрон), точность которого сравнима с микроскопическим исследованием.
Метод оптической когерентной томографии (optical coherence tomography, сокращенно ОСТ (eng.) или ОКТ (рус.)) представляет собой современное высокоточное неинвазивное исследование различных структур глаза. ОСТ является бесконтактным методом, позволяющим специалисту визуализировать ткани глаза с очень высоким разрешением (1 — 15 микрон), точность которого сравнима с микроскопическим исследованием.
Теоретические основы метода ОСТ были разработаны в 1995 году американским офтальмологом К. Пулафито, и уже в 1996 – 1997 годах компания Carl Zeiss Meditec внедрила в клиническую практику первый прибор для оптической когерентной томографии. Сегодня устройства для ОСТ применяют для диагностики различных заболеваний глазного дна и переднего отрезка глаза
Показания к ОСТ
Метод оптической когерентной томографии позволяет:
- визуализировать морфологические изменения сетчатки и слоя нервных волокон, а также и оценить их толщину;
- оценить состояние диска зрительного нерва;
- осмотреть структуры переднего отрезка глаза и их взаимное пространственное расположение.
Метод может применяться в офтальмологии для диагностики множества патологий заднего отдела глаза, таких как:
- дегенеративные изменения сетчатки (врожденные и приобретенные, ВМД)
- кистоидный макулярный отек и макулярный разрыв
- отслойка сетчатки
- эпиретинальная мембрана
- изменения диска зрительного нерва (аномалии, отек, атрофия)
- диабетическая ретинопатия
- тромбоз центральной вены сетчатки
- пролиферативная витреоретинопатия.
Что касается патологий переднего отдела глаза, ОСТ может применяться:
- для оценки угла передней камеры глаза и работы дренажных систем у пациентов с глаукомой
- в случае глубоких кератитов и язв роговой оболочки глаза
- во время осмотра роговицы в ходе подготовки и после выполнения лазерной коррекции зрения и кератопластики
- для контроля у пациентов с факичными ИОЛ или интрастромальными кольцами.
Видео нашего специалиста
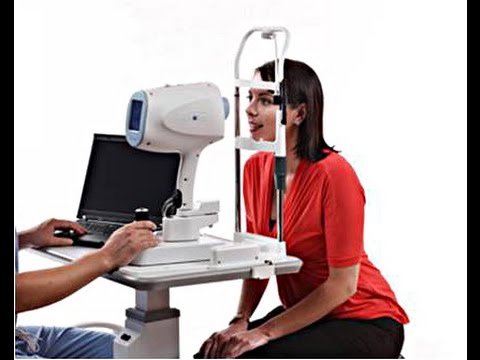
Как проходит исследование
 Пациенту предлагают зафиксировать взгляд обследуемым глазом на специальной метке, после чего врач выполняет ряд сканирований и отбирает наиболее информативное изображение, позволяющее оценить состояние органа зрения. Диагностика полностью безболезненна и занимает минимум времени.
Пациенту предлагают зафиксировать взгляд обследуемым глазом на специальной метке, после чего врач выполняет ряд сканирований и отбирает наиболее информативное изображение, позволяющее оценить состояние органа зрения. Диагностика полностью безболезненна и занимает минимум времени.
Для оценки результатов применяют сравнение с нормативной базой данных, находящейся в памяти аппарата для когерентной томографии. В «Московской Глазной Клинике» используется современный высокотехнологичный оптический когерентный томограф OPTOVUE RTVue100, производства США, позволяющий провести исследование быстро и с максимальной точностью.
Цены на обследование
Стоимость проведения оптической когерентной томографии макулярной области составляет 2000 рублей (за 1 глаз), ОСТ диска зрительного нерва – 2000 рублей, ОСТ роговицы – 1000 рублей. Цены на другие медицинские услуги в МГК можно посмотреть здесь.
Все интересующие Вас вопросы можно задать специалистам по телефонам 8 800 777-38-81 и 8 (499) 322-36-36 или онлайн, воспользовавшись соответствующей формой на сайте.

Принцип метода ОСТ
Метод основывается на различии в отражении световых волн разными тканями организма в зависимости от их структуры. Для визуализации тканей сетчатки применяют низкокогерентные световые лучи с длиной волны 830 нм, для диагностики патологий переднего отрезка глаза — лучи с длиной волны 1310 нм. Специальный прибор, интерферометр Майкельсона, измеряет такие показатели как время задержки отраженных лучей и их интенсивность после прохождения через различные структуры глаза. В ходе исследования луч света разделяется на два пучка: один пучок следует к специальному зеркалу (он является контрольным), другой направляется в исследуемую область. После отражения лучей они улавливаются фотодетектором, который формирует интерференционное изображение. Для получения объемного изображения исследование выполняется в продольном и поперечном направлениях.
После анализа данного изображения с помощью установленного программного обеспечения, прибор выдает результаты исследования в виде псевдоизображения структур глаза. При этом участки, имеющие высокую степень отражения световых лучей, на изображении имеют оттенки красного цвета, а зоны с низкой степенью отражения световых лучей окрашиваются в холодные цвета, вплоть до черного.
Известно, что слой пигментного эпителия и нервных волокон обладает более высокой светоотражающей способностью, в то же время ядерный и плексиформный слои сетчатой оболочки глаза характеризуются средней светоотражательной способностью. Стекловидное тело на томограмме в норме окрашивается в черный цвет, т.к. данная структура глаза оптически прозрачна. Проведение исследования затрудняется в случае отека роговой оболочки глаза, при наличии кровоизлияний или помутнений оптических сред.
Источник
Оптическая когерентная томография (ОКТ или OCT)
Это получение и оценка изображений срезов тканей переднего и заднего отрезков глаза, включая роговицу, сетчатку, слои нервных волокон сетчатки, слой ганглиозных клеток, макулярную область и головку зрительного нерва. Данный метод высокоточной компьютерной томограммы органа зрения для диагностики сложных и скрытых для визуализации заболеваний глаза применяется около 20 лет, но в последние годы метод ОКТ стал золотым стандартом офтальмологического обследования Пациентов с патологией сетчатки и зрительного нерва.
В нашей клинике для исследования применяется новая высокоточная компьютерная система CIRRUS HD-OCT (Carl Zeiss Meditec, Германия), которая позволяет получать и анализировать томограммы структур глаза в поперечной и трехмерных проекциях при помощи спектральной оптической когерентной томографии (СОКТ). СОКТ – это новый вид неинвазивной низкокогерентной интерферометрии, создающей томограммы высокой разрешающей способности без контакта с глазами. Аббревиатура HD-OCT означает «оптическая когерентная томография высокой четкости» (High-Definition Optical Coherence Tomography).

Данный метод исследования благодаря своей точности позволяет провести диагностику на ранних стадиях и назначить своевременное и адекватное лечение таких серьезных заболеваний глаза, как:
- Глаукома (заболевание зрительной системы, сопровождающееся повышением внутриглазного давления и атрофией зрительного нерва)
- ВМД (возрастная макулярная дегенерация)
- Макулярный разрыв
- Кистозный макулярный отек
- Диабетическая ретинопатия.
Преимущества системы CIRRUS HD-OCT:
- Поперечное и трехмерное спектральное сканирование
- Быстрота исследований
- Нет необходимости расширять зрачок
- Автоматическая система наведения
- Авто контроль за качеством снимков
- Моментальная диагностика и дифференциальная диагностика заболеваний
- Контроль динамики лечения
Перечень изменений структур глаза, диагностируемых на ОСТ
Элементарные изменения контуров сетчатки:
- Изменение профиля центральной ямки
- Пре- и эпиретинальные мембраны
- Макулярные разрывы
- Ламеллярные разрывы
- Песевдоразрывы
- Друзы и атрофия пигментного эпителия
- Задняя стафилома при миопии
Полости сетчатки и сосудистой оболочки:
- Серозные отслойки сетчатки
- Отслойки пигментного эпителия
- Отек (кистозный, локальный, диффузный)
- Микро- и микроаневризмы
- Нормальные и патологические сосуды

Плотные образования и отложения:
- Кровоизлияния
- Экссудаты (твердые и ватообразные)
- Субретинальные отложения (пигмент, липофусцин)
- Неоваскулярные мембраны
Изменение толщины слоев сетчатки:
- Атрофия и дистрофия слоев сетчатки
- Окклюзия артерий
- Глаукома
- Атрофия зрительного нерва
- Меланомы, невусы
Изменения сосудистой оболочки:
- Возрастные изменения
- Центральные серозные хориоретинопатии
- Воспаления
- Близорукость
- Опухоли (меланомы, гемангиомы, остеомы, невусы)
Диагностика и лечение глаукомы
Данные исследований ОСТ позволяют офтальмологу выявить глаукому на самых ранних стадиях, когда зрение и поля зрения еще не изменены, но появляются скрытые нарушения в слоях ганглиозных клеток, которые страдают при глаукоме самыми первыми. Иногда глаукома может протекать на фоне низкого давления и без клинических симптомов. Применяя компьютерное исследования структур зрительного нерва и сетчатки, офтальмолог получает возможность оценивать и контролировать эффективность назначенного лечения, выявить причину и характер повышения внутриглазного давления.

CIRRUS включает в себя широкий набор диагностических средств, совместное использование которых позволяет фиксировать и оценивать дефекты и признаки ухудшения состояния зрительного нерва, характерные для начальных и развитых стадий заболевания. Отдельные и комбинированные отчеты упрощают процесс оценки и сокращают время принятия решений:
- Анализ ганглионарных клеток значительно расширяет возможности диагностики глаукомы и позволяет вам выявлять даже незначительные изменения макулы, не представленные в области диска зрительного нерва.
- Центрирование измерений толщины ганглионарных клеток осуществляется автоматически с помощью функции FoveaFinder™. Измерения сравниваются с нормативными данными на суперпиксельных картах отклонений.
- Кубический анализ использования данных позволяет вам проводить диагностический анализ, результаты которого вы можете использовать для оценки течения глаукомного процесса.
- Функция AutoCenter™ после получения скана автоматически центрирует измерительную окружность вокруг диска зрительного нерва. Размещение окружности не зависит от оператора.
- Собственные алгоритмы компании ZEISS позволяют точно измерять толщину слоя нервных волокон сетчатки и параметры диска зрительного нерва, включая нейроретинальное кольцо, с учетом наклоненных дисков, разрывов ретинального пигментного эпителия и прочих опасных патологий.
Источник
1. Huang D., Swanson E.A., Lin C.P. et al. Optical coherence tomography // Science. 1991. Vol. 254. № 5035. P. 1178–1181.
2. Swanson E.A., Izatt J.A., Hee M.R. et al. In-vivo retinal imaging by optical coherence tomography // Opt Lett. 1993. Vol. 18. № 21. P. 1864–1866.
3. Fercher A.F., Hitzenberger C.K., Drexler W., Kamp G., Sattmann H. In-Vivo optical coherence tomography // Am J Ophthalmol. 1993. Vol. 116. № 1. P. 113–115.
4. Izatt J.A., Hee M.R., Swanson E.A., Lin C.P., Huang D., Schuman J.S., Puliafito C.A., Fujimoto J.G. Micrometer-scale resolution imaging of the anterior eye in vivo with optical coherence tomography // Arch Ophthalmol. 1994. Vol. 112. № 12. P. 1584–1589.
5. Puliafito C.A., Hee M.R., Lin C.P., Reichel E., Schuman J.S., Duker J.S., Izatt J.A., Swanson E.A., Fujimoto J.G. Imaging of macular diseases with optical coherence tomography // Ophthalmology. 1995. Vol. 102. № 2. P. 217–229.
6. Schuman J.S., Hee M.R., Arya A.V., Pedut-Kloizman T., Puliafito C.A., Fujimoto J.G., Swanson E.A. Optical coherence tomography: a new tool for glaucoma diagnosis // Curr Opin Ophthalmol. 1995. Vol. 6. № 2. P. 89–95.
7. Schuman J.S., Hee M.R., Puliafito C.A., Wong C., Pedut-Kloizman T., Lin C.P., Hertzmark E., Izatt .JA., Swanson E.A., Fujimoto J.G. Quantification of nerve fiber layer thickness in normal and glaucomatous eyes using optical coherence tomography // Arch Ophthalmol. 1995. Vol. 113. № 5. P. 586–596.
8. Hee M.R., Puliafito C.A., Wong C., Duker J.S., Reichel E., Schuman J.S., Swanson E.A., Fujimoto J.G. Optical coherence tomography of macular holes // Ophthalmology. 1995 Vol. 102. № 5. P. 748–756.
9. Hee M.R., Puliafito C.A., Wong C., Reichel E., Duker J.S., Schuman J.S., Swanson E.A., Fujimoto J.G. Optical coherence tomography of central serous chorioretinopathy // Am J Ophthalmol.1995. Vol. 120. № 1. P. 65–74.
10. Hee M.R., Puliafito C.A., Wong C., Duker J.S., Reichel E., Rutledge B., Schuman J.S., Swanson E.A., Fujimoto J.G. Quantitative assessment of macular edema with optical coherence tomography // Arch Ophthalmol. 1995. Vol. 113. № 8. P. 1019–1029.
11. Висковатых А.В., Пожар В.Э., Пустовойт В.И. Разработка оптического когерентного томографа для офтальмологии на быстроперестраиваемых акустооптических фильтрах // Сборник материалов III Евразийского конгресса по медицинской физике и инженерии «Медицинская физика – 2010». 2010. Т. 4. C. 68–70. М., 2010 [Viskovatykh A.V. Pozhar V.E., Pustovoyt V.I. The development of optical coherence tomography for ophthalmology at the acoustooptical filters // Collection of materials of the 3rd Eurasian Congress on Medical Physics and Engineering «Medical Physics 2010». 2010. № 4. P. 68–70 (in Russian)].
12. Drexler W., Morgner U., Ghanta R.K., Kartner F.X., Schuman J.S., Fujimoto J.G. Ultrahigh-resolution ophthalmic optical coherence tomography // Nat Med. 2001. Vol. 7. № 4. P. 502–507.
13. Drexler W., Sattmann H., Hermann B. et al. Enhanced visualization of macular pathology with the use of ultrahigh-resolution optical coherence tomography // Arch Ophthalmol. 2003. Vol. 121. P. 695–706.
14. Ko T.H., Fujimoto J.G., Schuman J.S. et al. Comparison of ultrahigh and standard resolution optical coherence tomography for imaging of macular pathology // Arch Ophthalmol. 2004. Vol. 111. P. 2033–2043.
15. Ko T.H., Adler D.C., Fujimoto J.G. et al. Ultrahigh resolution optical coherence tomography imaging with a broadband superluminescent diode light source // Opt Express. 2004. Vol. 12. P. 2112–2119.
16. Fercher A.F., Hitzenberger C.K., Kamp G., El-Zaiat S.Y. Measurement of intraocular distances by backscattering spectral interfereometry // Opt Commun. 1995. Vol. 117. P. 43–48.
17. Choma M.A., Sarunic M.V., Yang C.H., Izatt J.A. Sensitivity advantage of swept source and Fourier domain optical coherence tomography // Opt Express. 2003. Vol. 11. № 18. P. 2183–2189.
18. Астахов Ю.С., Белехова С.Г. Оптическая когерентная томография: как все начиналось и современные диагностические возможности методики // Офтальмологические ведомости. 2014. Т. 7. № 2. C. 60–68. [Astakhov Yu.S., Belekhova S.G. Optical coherence tomography: how it all began and advanced diagnostic capabilities technique // Oftalmologicheskie vedomosti. 2014. № 7 (2). P. 60–68 (in Russian)].
19. Свирин А.В., Кийко Ю.И., Обруч Б.В., Богомолов А.В. Спектральная когерентная оптическая томография: принципы и возможности метода // Клиническая офтальмология. 2009. Т. 10. № 2. C. 50–53 [Svirin A.V., Kiyko Yu.I., Obruch B.V., Bogomolov A.V. Spectral optic coherent tomography: principles and possibilities (Literary review) // Clinical Ophthalmology. 2009. № 10 (2). P. 50–53 (in Russian)].
20. Kiernan D.F., Hariprasad S.M., Chin E.K., Kiernan C.L, Rago J., Mieler W.F. Prospective comparison of cirrus and stratus оptical coherence tomography for quantifying retinal thickness // Am J Ophthalmol. 2009. Vol. 147. № 2. P. 267–275.
21. Wang R.K. Signal degradation by multiple scattering in optical coherence tomography of dense tissue: a monte carlo study towards optical clearing of biotissues // Phys Med Biol. 2002. Vol. 47. № 13. P. 2281–2299.
22. Povazay B., Bizheva K., Hermann B. et al. Enhanced visualization of choroidal vessels using ultrahigh resolution ophthalmic OCT at 1050 nm // Opt Express. 2003. Vol. 11. № 17. P. 1980–1986.
23. Spaide R.F., Koizumi H., Pozzoni M.C. et al. Enhanced depth imaging spectral-domain optical coherence tomography // Am J Ophthalmol. 2008. Vol. 146. P. 496–500.
24. Margolis R., Spaide R.F. A pilot study of enhanced depth imaging optical coherence tomography of the choroid in normal eyes // Am J Ophthalmol. 2009. Vol. 147. P. 811–815.
25. Ho J., Castro D.P., Castro L.C., Chen Y., Liu J., Mattox C., Krishnan C., Fujimoto J.G., Schuman J.S., Duker J.S. Clinical assessment of mirror artifacts in spectral-domain optical coherence tomography // Invest Ophthalmol Vis Sci. 2010. Vol. 51. № 7. P. 3714–3720.
26. Anand R. Enhanced depth optical coherence tomographyiImaging — a review // Delhi J Ophthalmol. 2014. Vol. 24. № 3. P. 181–187.
27. Rahman W., Chen F.K., Yeoh J. et al. Repeatability of manual subfoveal choroidal thickness measurements in healthy subjects using the technique of enhanced depth imaging optical coherence tomography // Invest Ophthalmol Vis Sci. 2011. Vol. 52. № 5. P. 2267–2271.
28. Park S.C., Brumm J., Furlanetto R.L., Netto C., Liu Y., Tello C., Liebmann J.M., Ritch R. Lamina cribrosa depth in different stages of glaucoma // Invest Ophthalmol Vis Sci. 2015. Vol. 56. № 3. P. 2059–2064.
29. Park S.C., Hsu A.T., Su D., Simonson J.L., Al-Jumayli M., Liu Y., Liebmann J.M., Ritch R. Factors associated with focal lamina cribrosa defects in glaucoma // Invest Ophthalmol Vis Sci. 2013. Vol. 54. № 13. P. 8401–8407.
30. Faridi O.S., Park S.C., Kabadi R., Su D., De Moraes C.G., Liebmann J.M., Ritch R. Effect of focal lamina cribrosa defect on glaucomatous visual field progression // Ophthalmology. 2014 Vol. 121. № 8. P. 1524–1530.
31. Potsaid B., Baumann B., Huang D., Barry S., Cable A.E., Schuman J.S., Duker J.S., Fujimoto J.G. Ultrahigh speed 1050nm swept source / Fourier domain OCT retinal and anterior segment imaging at 100,000 to 400,000 axial scans per second // Opt Express 2010. Vol. 18. № 19. P. 20029–20048.
32. Adhi M., Liu J.J., Qavi A.H., Grulkowski I., Fujimoto J.G., Duker J.S. Enhanced visualization of the choroido-scleral interface using swept-source OCT // Ophthalmic Surg Lasers Imaging Retina. 2013. Vol. 44. P. 40–42.
33. Mansouri K., Medeiros F.A., Marchase N. et al. Assessment of choroidal thickness and volume during the water drinking test by swept-source optical coherence tomography // Ophthalmology. 2013. Vol. 120. № 12. P. 2508–2516.
34. Mansouri K., Nuyen B., Weinreb R.N. Improved visualization of deep ocular structures in glaucoma using high penetration optical coherence tomography // Expert Rev Med Devices. 2013. Vol. 10. № 5. P. 621–628.
35. Takayama K., Hangai M., Kimura Y. et al. Three-dimensional imaging of lamina cribrosa defects in glaucoma using sweptsource optical coherence tomography // Invest Ophthalmol Vis Sci. 2013. Vol. 54. № 7. P. 4798–4807.
36. Park H.Y., Shin H.Y., Park C.K. Imaging the posterior segment of the eye using swept-source optical coherence tomography in myopic glaucoma eyes: comparison with enhanced-depth imaging // Am J Ophthalmol. 2014. Vol. 157. № 3. P. 550–557.
37. Michalewska Z., Michalewski J., Adelman R.A., Zawislak E., Nawrocki J. Choroidal thickness measured with swept source optical coherence tomography before and after vitrectomy with internal limiting membrane peeling for idiopathic epiretinal membranes // Retina. 2015. Vol. 35. № 3. P. 487–491.
38. Lopilly Park H.Y., Lee N.Y., Choi J.A., Park C.K. Measurement of scleral thickness using swept-source optical coherence tomography in patients with open-angle glaucoma and myopia // Am J Ophthalmol. 2014. Vol. 157. № 4. P. 876–884.
39. Omodaka K., Horii T., Takahashi S., Kikawa T., Matsumoto A., Shiga Y., Maruyama K., Yuasa T., Akiba M., Nakazawa T. 3D Evaluation of the Lamina Cribrosa with Swept-Source Optical Coherence Tomography in Normal Tension Glaucoma // PLoS One. 2015 Apr 15. Vol. 10 (4). e0122347.
40. Mansouri K., Nuyen B., Weinreb R. Improved visualization of deep ocular structures in glaucoma using high penetration optical coherence tomography // Expert Rev Med Devices. 2013. Vol. 10. № 5. P. 621–628.
41. Binder S. Optical coherence tomography/ophthalmology: Intraoperative OCT improves ophthalmic surgery // BioOpticsWorld. 2015. Vol. 2. P. 14–17.
42. Zhang Z.E., Povazay B., Laufer J., Aneesh A., Hofer B., Pedley B., Glittenberg C., Treeby B., Cox B., Beard P., Drexler W. Multimodal photoacoustic and optical coherence tomography scanner using an all optical detection scheme for 3D morphological skin imaging // Biomed Opt Express. 2011. Vol. 2. № 8. P. 2202–2215.
43. Morgner U., Drexler W., Ka..rtner F. X., Li X. D., Pitris C., Ippen E. P., and Fujimoto J. G. Spectroscopic optical coherence tomography // Opt Lett. 2000. Vol. 25. № 2. P. 111–113.
44. Leitgeb R., Wojtkowski M., Kowalczyk A., Hitzenberger C. K., Sticker M., Ferche A. F. Spectral measurement of absorption by spectroscopic frequency-domain optical coherence tomography // Opt Lett. 2000. Vol. 25. № 11. P. 820–822.
45. Pircher M., Hitzenberger C.K., Schmidt-Erfurth U. Polarization sensitive optical coherence tomography in the human eye // Progress in Retinal and Eye Research. 2011. Vol. 30. № 6. P. 431–451.
46. Geitzinger E., Pircher M., Geitzenauer W., Ahlers C., Baumann B., Michels S., Schmidt-Erfurth U., Hitzenberger C.K. Retinal pigment epithelium segmentation by polarization sensitive optical coherence tomography // Opt Express. 2008. Vol. 16. P. 16410–16422.
47. Pircher M., Goetzinger E., Leitgeb R., Hitzenberger C.K. Transversal phase resolved polarization sensitive optical coherence tomography // Phys Med Biol. 2004. Vol. 49. P. 1257–1263.
48. Mansouri K., Nuyen B., N Weinreb R. Improved visualization of deep ocular structures in glaucoma using high penetration optical coherence tomography // Expert Rev Med Devices. 2013. Vol. 10. № 5. P. 621–628.
49. Geitzinger E., Pircher M., Hitzenberger C.K. High speed spectral domain polarization sensitive optical coherence tomography of the human retina // Opt Express. 2005. Vol. 13. P. 10217–10229.
50. Ahlers C., Gotzinger E., Pircher M., Golbaz I., Prager F., Schutze C., Baumann B., Hitzenberger C.K., Schmidt-Erfurth U. Imaging of the retinal pigment epithelium in age-related macular degeneration using polarization-sensitive optical coherence tomography // Invest Ophthalmol Vis Sci. 2010. Vol. 51. P. 2149–2157.
51. Geitzinger E., Baumann B., Pircher M., Hitzenberger C.K. Polarization maintaining fiber based ultra-high resolution spectral domain polarization sensitive optical coherence tomography // Opt Express. 2009. Vol. 17. P. 22704–22717.
52. Lammer J., Bolz M., Baumann B., Geitzinger E., Pircher M., Hitzenberger C., Schmidt-Erfurth U. 2010. Automated Detection and Quantification of Hard Exudates in Diabetic Macular Edema Using Polarization Sensitive Optical Coherence Tomography // ARVO abstract 4660/D935.
53. Schmitt J. OCT elastography: imaging microscopic deformation and strain of tissue // Opt Express. 1998. Vol. 3. № 6. P. 199–211.
54. Ford M.R., Roy A.S., Rollins A.M. and Dupps W.J.Jr. Serial biomechanical comparison of edematous,normal, and collagen crosslinked human donor corneas using optical coherence elastography // J Cataract Refract Surg. 2014. Vol. 40. № 6. P. 1041–1047.
55. Leitgeb R., Schmetterer L.F., Wojtkowski M., Hitzenberger C.K., Sticker M., Fercher A.F. Flow velocity measurements by frequency domain short coherence interferometry. Proc. SPIE. 2002. P. 16–21.
56. Wang Y., Bower B.A., Izatt J.A., Tan O., Huang D. In vivo total retinal blood flow measurement by Fourier domain Doppler optical coherence tomography // J Biomed Opt. 2007. Vol. 12. P. 412–415.
57. Wang R. K., Ma Z., Real-time flow imaging by removing texture pattern artifacts in spectral-domain optical Doppler tomography // Opt. Lett. 2006. Vol. 31. № 20. P. 3001–3003.
58. Wang R. K., Lee A. Doppler optical micro-angiography for volumetric imaging of vascular perfusion in vivo // Opt Express. 2009. Vol. 17. № 11. P. 8926–8940.
59. Wang Y., Bower B. A., Izatt J. A., Tan O., Huang D. Retinal blood flow measurement by circumpapillary Fourier domain Doppler optical coherence tomography // J Biomed Opt. 2008. Vol. 13. № 6. P. 640–643.
60. Wang Y., Fawzi A., Tan O., Gil-Flamer J., Huang D. Retinal blood flow detection in diabetic patients by Doppler Fourier domain optical coherence tomography // Opt Express. 2009. Vol. 17. № 5. P. 4061–4073.
61. Jia Y., Tan O., Tokayer J., Potsaid B., Wang Y., Liu J.J., Kraus M.F., Subhash H., Fujimoto J.G., Hornegger J., Huang D. Split-spectrum amplitude-decorrelation angiography with optical coherence tomography // Opt Express. 2012. Vol. 20. № 4. P. 4710–4725.
62. Jia Y., Wei E., Wang X., Zhang X., Morrison J.C., Parikh M., Lombardi L.H., Gattey D.M., Armour R.L., Edmunds B., Kraus M.F., Fujimoto J.G., Huang D. Optical coherence tomography angiography of optic disc perfusion in glaucoma // Ophthalmology. 2014. Vol. 121. № 7. P. 1322–1332.
63. Bizheva K., Pflug R., Hermann B., Povazay B., Sattmann H., Anger E., Reitsamer H., Popov S., Tylor J.R., Unterhuber A., Qui P., Ahnlet P.K., Drexler W. Optophysiology: depth resolved probing of retinal physiology with functional ultrahigh resolution optical coherence tomography // PNAS (Proceedings of the National Academy of Sciences of America ). 2006. Vol. 103. № 13. P. 5066–5071.
64. Tumlinson A.R., Hermann B., Hofer B., Považay B., Margrain T.H., Binns A.M., Drexler W., Techniques for extraction of depth-resolved in vivo human retinal intrinsic optical signals with optical coherence tomography // Jpn. J. Ophthalmol. 2009. Vol. 53. P. 315–326.
Источник
Возможности современной офтальмологии значительно расширены в сравнении с методами диагностики и лечения заболеваний органов зрения еще каких-то пятьдесят лет назад. Сегодня для постановки точного диагноза, выявления малейших изменений в структурах глаза применяются сложные, высокотехнологичные аппараты и методики. Оптическая когерентная томография (ОКТ), выполняемая с помощью специального сканнера – один из таких методов. Что это такое, кому и когда нужно проводить подобное обследование, как правильно к нему подготовиться, существуют ли противопоказания и возможны ли осложнения – ответы на все эти вопросы ниже.
Преимущества и особенности
Оптическая когерентная томография сетчатки и других элементов глаза – это инновационное офтальмологическое исследование, при котором визуализируются в высоком качестве разрешения поверхностные и глубинные структуры органов зрения. Этот метод является сравнительно новым, не проинформированные пациенты относятся к нему с предубеждением. И совершенно напрасно, так как на сегодняшний день ОКТ считается лучшим, что существует в диагностической офтальмологии.

Выполнение ОКТ занимает всего лишь несколько секунд, а результаты будут подготовлены максимум через час после обследования – можно заехать в клинику на обеденном перерыве, выполнить ОКТ, сразу же получить диагноз и в тот же день начать лечение
К основным преимуществам ОКТ можно отнести:
- возможность исследовать одновременно оба глаза;
- скорость процедуры и оперативность получения точных результатов для постановки диагноза;
- за один сеанс врач получает четкое представление о состоянии макулы, зрительного нерва, сетчатки, роговицы, артерий и капилляров глаза на микроскопическом уровне;
- ткани элементов глаза можно досконально изучить без биопсии;
- разрешающие способности ОКТ во много раз превышают показатели обычной компьютерной томографии или УЗИ – обнаруживаются повреждения тканей размером не более 4 микрон, патологические изменения на самых ранних стадиях;
- не требуется вводить внутривенно контрастные окрашивающие вещества;
- процедура относится к неинвазивным, потому почти не имеет противопоказаний, не требует специальной подготовки и восстановительного периода.
При проведении когерентной томографии пациент не получает никакого радиационного облучения, что также является большим преимуществом с учетом того, какому вредному воздействию внешних факторов и без этого подвергается каждый современный человек.
В чем суть процедуры
Если через организм человека пропустить световые волны, они будут отражаться от различных органов по-разному. Время задержки световых волн и время их прохождения через элементы глаза, интенсивность отражения замеряют с помощью специальных приборов при проведении томографии. Затем они переносятся на экран, после чего проводятся расшифровка и анализ полученных данных.
Окт сетчатки глаза – абсолютно безопасный и безболезненный метод, поскольку приборы не контактируют с органами зрения, ничего не вводится подкожно или внутрь глазных структур. Но при этом он обеспечивает куда более высокую информативность, чем стандартные КТ или МРТ.

Вот так выглядит изображение на мониторе компьютера, полученное путем сканирования при ОКТ, для его расшифровки потребуются особые познания и навыки специалиста
Именно в способе расшифровки получаемого отражения кроется главная особенность ОКТ. Дело в том, что волны света движутся с очень высокой скоростью, что не позволяет напрямую замерить необходимые показатели. Для этих целей используется специальный прибор – интерферометр Мейкельсона. Он разделяет световую волну на два луча, затем один луч пропускается через глазные структуры, которые необходимо исследовать. А другой направляется на зеркальную поверхность.
Если требуется выполнить обследование сетчатки и макулярной зоны глаза, применяется низкокогерентный инфракрасный луч длиной 830 нм. Если же нужно сделать ОКТ передней камеры глаза, будет нужна волна длиной 1310 нм.
Оба луча соединяются и попадают в фотодетектор. Там они преображаются в интерференционную картинку, которая затем анализируется компьютерной программой и выводится на монитор в виде псевдоизображения. Что же оно покажет? Участки с высокой степенью отражения будут окрашены в более теплые оттенки, а те, которые отражают световые волны слабо, выглядят на картинке почти черными. «Теплыми» на картинке отображаются нервные волокна и пигментный эпителий. Ядерные и плексиформные прослойки сетчатки обладают средней степенью отражаемости. А стекловидное тело выглядит черным, так как оно практически прозрачное и хорошо пропускает световые волны, почти не отражая их.
Для получения полноценной, информативной картинки необходимо пропустить световые волны через глазное яблоко в двух направлениях: поперечном и продольном. Искажения получаемого изображения могут возникать, если роговица отечна, имеют место помутнения стекловидного тела, кровоизлияния, инородные частички.

Одной процедуры продолжительностью менее минуты достаточно, чтобы без инвазивного вмешательства получить максимально полную информацию о состоянии глазных структур, выявить развивающиеся патологии, их формы и стадии
Что можно сделать с помощью оптической томографии:
- Определить толщину глазных структур.
- Установить размеры диска зрительного нерва.
- Выявить и оценить изменения структуры сетчатки и нервных волокон.
- Оценить состояние элементов переднего участка глазного яблока.
Таким образом, при проведении ОКТ врач-офтальмолог получает возможность за один сеанс изучить все составляющие глаза. Но наиболее информативным и точным получается исследование сетчатки. На сегодняшний день оптическая когерентная томография – самый оптимальный и информативный способ оценки состояния макулярной зоны органов зрения.
Показания к проведению
Оптическую томографию в принципе можно назначать каждому пациенту, обратившемуся к офтальмологу с какими-либо жалобами. Но в отдельных случаях без этой процедуры не обойтись, она заменяет КТ и МРТ и даже опережает их по информативности. Показаниями к проведению ОКТ являются такие симптомы и жалобы пациентов:
- «Мушки», паутинки, молнии и вспышки перед глазами.
- Помутнение зрительной картинки.
- Неожиданное и резкое снижение зрения в одном или обоих глазах.
- Сильная боль в органах зрения.
- Значительное повышение внутриглазного давления при глаукоме или по другим причинам.
- Экзофтальм – выпячивание глазного яблока из орбиты самопроизвольно или после травмы.

Глаукома, повышение внутриглазного давления, изменения диска зрительного нерва, подозрения на отслойку сетчатки, а также подготовка к хирургическим вмешательствам на глазах – все это показания к проведению оптической когерентной томографии
Если предстоит коррекция зрения с использованием лазера, то подобное исследование проводят до операции и после нее, чтобы точно определить угол передней камеры глаза и оценить степень дренажа внутриглазной жидкости (если диагностирована глаукома). Также ОКТ необходима при проведении кератопластики, вживления интрастромальных колец или интраокулярных линз.
Что можно определить и обнаружить с помощью когерентной томографии:
- изменения внутриглазного давления;
- врожденные или приобретенные дегенеративные изменения тканей сетчатки;
- злокачественные и доброкачественные новообразования в структурах глаза;
- симптомы и степень выраженности диабетической ретинопатии;
- различные патологии диска зрительного нерва;
- полиферативную витреоретинопатию;
- эпиретинальную мембрану;
- тромбы коронарных артерий или центральной вены глаза и другие сосудистые изменения;
- разрывы или отслойку макулы;
- макулярный отек, сопровождающийся формированием кист;
- язвы роговицы;
- глубоко проникающий кератит;
- прогрессирующая близорукость.
Благодаря такому диагностическому исследованию можно выявить даже незначительные изменения и аномалии органов зрения, правильно поставить диагноз, определить степень поражений и оптимальный метод лечения. ОКТ на самом деле помогает сохранить или восстановить зрительные функции пациента. А поскольку процедура совершенно безопасна и безболезненна, часто ее выполняют в профилактических целях при заболеваниях, которые могут осложняться патологиями со стороны глаз – при сахарном диабете, гипертонической болезни, нарушениях мозгового кровообращения, после травм или хирургического вмешательства.
Когда нельзя проводить ОКТ
Наличие кардиостимулятора и других имплантов, состояния, при которых пациент не может фокусировать взгляд, находится в бессознательном состоянии или не способен контролировать свои эмоции и движения, большинство диагностических исследований не проводится. В случае с когерентной томографией все иначе. Процедуру такого рода можно проводить при спутанности сознания и нестабильном психоэмоциональном состоянии пациента.

В отличие от МРТ и КТ, которые хотя информативны, но имеют ряд противопоказаний, ОКТ можно применять для обследования детей без всяких опасений – ребенок не испугается процедуры и не получит никаких осложнений
Главное и фактически единственное препятствие к выполнению ОКТ – это одновременное проведение других диагностических исследований. В день, на который назначена ОКТ, применять какие-либо другие диагностические методы обследования органов зрения нельзя. Если же пациент уже подвергался другим процедурам, то ОКТ переносят на другой день.
Также помехой к получению четкого, информативного изображения может стать близорукость высокой степени или сильное помутнение роговицы и других элементов глазного яблока. В этом случае световые волны будут плохо отражаться и давать искаженное изображение.
Техника выполнения ОКТ
Сразу же нужно сказать, что оптическую когерентную томографию в районных поликлиниках обычно не проводят, так как офтальмологические кабинеты не располагают необходимым оборудованием. Сделать ОКТ можно только в специализированных частных медицинских учреждениях. В крупных городах не составит труда найти заслуживающий доверия офтальмологический кабинет, располагающий ОКТ-сканнером. о проведении процедуры желательно договориться заблаговременно, стоимость когерентной томографии для одного глаза начинается от 800 рублей.
Никакой подготовки к проведению ОКТ не требуется, нужен только функционирующий ОКТ-сканнер и сам пациент. Обследуемого попросят сесть на стул и сфокусировать взгляд на указанной отметке. Если глаз, структуру которого нужно исследовать, не способен сфокусироваться, то взгляд фиксируется насколько возможно другим, здоровым глазом. Находиться в неподвижном состоянии требуется не более двух минут – этого достаточно, чтобы пропустить пучки инфракрасного излучения через глазное яблоко.
В течение этого периода делается несколько снимков в разных плоскостях, после чего медицинский сотрудник отбирает самые четкие и качественные. Их компьютерная система сверяет с имеющейся базой данных, составленной на основании обследований других пациентов. Представлена база различными таблицами и схемами. Чем меньше будет обнаружено совпадений, тем выше вероятность, что структуры глаза обследуемого пациента патологически изменены. Поскольку все аналитические действия и преобразования полученных данных выполняются компьютерными программами в автоматическом режиме, на получение результатов уйдет не более получаса.
ОКТ-сканнер производит идеально точные измерения, обрабатывает их быстро и качественно. Но для постановки корректного диагноза необходимо еще правильно расшифровать полученные результаты. А это требует высокого профессионализма и глубоких познаний в области гистологии сетчатки и хориоидеи врача-офтальмолога. По этой причине расшифровка результатов исследований и постановка диагноза проводятся несколькими специалистами.
Резюме: большинство офтальмологических заболеваний крайне сложно распознать и диагностировать на ранних стадиях, тем более – установить реальную степень поражения глазных структур. При подозрительных симптомах стандартно назначается офтальмоскопия, но этого метода недостаточно, чтобы получить максимально точную картину о состоянии глаз. Более полную информацию дают компьютерная томография и магнитно-резонансная томография, но эти диагностические мероприятия имеют ряд противопоказаний. Оптическая когерентная томография совершенно безопасна и безвредна, ее можно выполнять даже в тех случаях, когда другие методы обследования органов зрения противопоказаны. На сегодняшний день это единственный неинвазивный способ получить максимально полную информацию о состоянии глаз. Единственная сложность, которая может возникнуть – не все офтальмологические кабинеты располагают необходимой для проведения процедуры аппаратурой.
Источник


