Неоваскуляризация сетчатки и диска зрительного нерва при
Пролиферативная диабетическая ретинопатия является наиболее тяжёлым глазным осложнением при сахарном диабете, возникающим в результате утраты нормального кровоснабжения сетчатки с последующим развитием пролиферативной неоваскулярной ткани на глазном дне. Развитие неоваскулярной ткани отражает нарушение баланса между ингибиторами и стимуляторами ангиогенеза в сетчатке и стекловидном теле. Считается, что в этом процессе участвует множество локальных химических медиаторов (цитокинов).
Важные клинические признаки. Неоваскуляризация на диске зрительного нерва (НВД, NVD)
Неоваскуляризацию, развивающуюся на поверхности диска зрительного нерва или на расстоянии не более одного диаметра диска от диска зрительного нерва, определяют как неоваскуляризация диска зрительного нерва (рис. 3-15, 3-16, 3-17, А-Г; рис. 3-19, А-Г). НВД легко спутать с шунтирующими сосудами на диске зрительного нерва (например, после тромбоза вены сетчатки). Неоваскуляризация диска обычно имеет вид кружевной сети неправильных сосудов, которые могут быть приподняты над поверхностью диска. Необходимо отличать истинную НВД от гиперемированного отёчного диска при диабетической папиллопатии. Неоваскуляризация сетчатки Этот термин используют для описания неоваскуляризации любой локализации на глазном дне, кроме диска зрительного нерва (НВД) (рис. 3-18, 3-19).

Рис. 3-15. Неоваскуляризация диска зрительного нерва. Неоваскуляризация диска зрительного нерва средней тяжести по определению DRS. (Diabetic Retinopathy Study Group.)

Рис. 3-16. Значительно проминирующая неоваскуляризация диска зрительного нерва.

Рис. 3-17. А. Пролиферативная диабетическая ретинопатия с макулярным отёком, твёрдыми экссудатами и неоваскуляризацией диска зрительного нерва. Б. Вид средней периферии в нижнем квадранте с несколькими геморрагиями и тусклой картиной глазного дна, В. Флюоресцентная ангиография подтверждает наличие неоваскуляризации диска зрительного нерва и выявляет выраженную окклюзию крупных и мелких ретинальных сосудов. Г. При флюоресцентной ангиографии в нижнем отделе глазного дна выявляют выраженную окклюзию капилляров и ишемическое прокрашивание стенок крупных сосудов (стрелка).

Рис. 3-18. А. Участки неоваскуляризации сетчатки (NVE). Обратите внимание на тусклый вид глазного дна по периферии от неоваскуляризации сетчатки. Б. При внутривенной флюоресцентной ангиографии в макуле определяют микроаневризмы с минимальными ишемическими изменениями. В. Гиперфлюоресценция очагов неоваскуляризации сетчатки. Г. Выраженное нарушение капиллярной перфузии к периферии от очагов неоваскуляризации сетчатки.

Рис. 3-19. А. Пролиферативная диабетическая ретинопатия с неоваскуляризацией диска зрительного нерва и неоваскуляризацией сетчатки (стрелки). Б. При внутривенной флюоресцентной ангиографии выявляют гиперфлюоресценцию неоваскуляризации диска зрительного нерва и неоваскуляризации сетчатки. Показано неравномерное капиллярное русло в центре макулы (увеличенное изображение). В. Выраженная гиперфлюоресценция участков неоваскуляризации сетчатки с неперфузируемой сетчаткой на периферии. Г. В поздней фазе наблюдается гиперфлюоресценция вследствие экстравазации красителя из неоваскуляризации диска зрительного нерва и неоваскуляризации сетчатки, а также вследствие макулярного отёка.
Неоваскуляризация сетчатки при пролиферативной диабетической ретинопатии чаще развивается в заднем полюсе глаза или на средней периферии, хотя возможно и появление неоваскуляризации сетчатки на крайней периферии сетчатки. Как правило, неоваскуляризация сетчатки возникает на границе перфузируемой и неперфузируемой сетчатки, что хорошо выявляется с помощью флюоресцентной ангиографии. Неоваскуляризация радужки Появление неоваскуляризация радужки является крайне неблагоприятным признаком (рис. 3-20). Вовлечение в патологический процесс угла передней камеры может повлечь за собой развитие неоваскулярной глаукомы (НВГ, NVG), привести к слепоте и появлению болей в глазу.

Рис. 3-20. В гониоскопическом зеркале видна неоваскуляризация радужной оболочки при пролиферативной диабетической ретинопатии.
С.Э. Аветисова, В.К. Сургуча
Опубликовал Константин Моканов
Источник
Эпидемиология
Сахарный диабет является одним из наиболее распространённых заболеваний. По последним статистическим данным, эта патология выявлена у 5% неотобранного населения мира, а диабетическая ретинопатия занимает первое место среди причин слепоты и слабовидения (Международный конгресс по эпидемиологии сахарного диабета. Лондон, 1990 г.)
Этиология и патогенез
В развитии диабетической ретинопатии важное значение имеют возраст начала сахарного диабета и его длительность. У пациентов с началом диабета до 30 лет частота ретинопатии возрастает от 50% после 10-12 лет от начала диабета до 75% и более после 20 лет. Если сахарный диабет диагностируется в более позднем возрасте, ретинопатия может развиваться гораздо быстрее и наблюдается в 75-80% случаев уже через 7-8 лет.
Ключевым фактором в развитии диабетической ретинопатии является недостаточность инсулина, вызывающая накопление интерцеллюлярного сорбитола и фруктозы, что способствует повышению осмотического давления, развитию внутриклеточного отёка, утолщению эндотелия капилляров и сужению их просвета. Повышение уровня протеинов в плазме увеличивает агрегацию форменных элементов крови и тормозит фибринолиз, обусловливая микротромбообразование, гибель перицитов и эндотелиальных клеток в ретинальных капиллярах, что нарушает проницаемость сосудистой стенки и приводит к межклеточному отёку тканей сетчатки. Нарушение перфузии в парафовеальных сосудах создаёт условия для развития экссудативной макулопатии. Прогрессирующая облитерация ретинальных капилляров становится причиной ишемии сетчатки, сопровождающейся выработкой вазоформативного фактора, способствующего развитию неоваскуляризации как начала пролиферативных изменений на глазном дне.
Диагностика
Основными методами диагностики считаются офтальмоскопия и ФАГД. Офтальмоскопия при диабетической ретинопатии выявляет многообразные патологические изменения на глазном дне. Для систематизации этих проявлений с учётом предшествующих классификаций (F.L’Esperanse, 1975; L.Weng, H.Little, 1977), в 1984 г. проф. Л.А. Кацнельсон разработал классификацию диабетической ретинопатии, позволяющую выделить 2 основные формы заболевания.
Классификация диабетической ретинопатии
- Препролиферативная форма.
- васкулярная фаза;
- экссудативная фаза (с отёком макулы, без отёка макулы);
- геморрагическая или экссудативно-геморрагическая фаза.
- Пролиферативная форма.
- с неоваскуляризацией;
- с глиозом I, II, III, IV стадии;
- с тракционной отслойкой сетчатки.
Подразумевается, что каждая последующая фаза содержит элементы предыдущей.
Клиника
Характерным признаком васкулярной фазы препролиферативной диабетической ретинопатии считается появление микроаневризм. Они обычно развиваются в зонах локальной капиллярной окклюзии и представляют собой мешотчатые выросты стенок капилляров. Кроме того, на этой стадии наблюдается увеличение калибра ретинальных вен — флебопатия и расширение аваскулярной зоны, свидетельствующее о начавшейся облитерации парафовеальных капилляров (рис. 4-1, 4-2, 4-3, 4-4).
Экссудативная фаза (рис. 4-4, 4-5, 4-6, 4-7, 4-8, 4-9, 4-10, 4-11, 4-12, 4-13, 4-14, 4-15, 4-16) диагностируется тогда, когда есть твёрдый и мягкий экссудат и относительно небольшая геморрагическая активность. Твёрдый экссудат содержит липидный выпот. Мягкий, или ватообразный, экссудат сопровождает процессы ишемии сетчатки и возникает в зонах микроваскулярной окклюзии. Сосудистые изменения усугубляются; появляются шунтированные сосуды, муфты, редупликации, телеангиэктазии. На более позднем этапе возникает обструкция прекапиллярных артериол и капилляров, объединяемая термином «интраретинальная микроангиопатия». В центральной зоне появляется отёк макулярной области, длительное существование которого приводит к развитию кистовидной дистрофии.
Геморрагическая фаза (рис. 4-17, 4-18) чаще встречается при юношеском диабете. Она отличается злокачественным течением и более быстрым переходом в пролиферативную форму. В клинической картине на первый план выступают множественные кровоизлияния в виде пятен, полос, языков пламени. Создаётся опасность прорыва внутренней пограничной мембраны и распространения кровоизлияний в эпиретинальное пространство и стекловидное тело. Отмечаются выраженные изменения ретинальных вен с множеством констрикций, напоминающих связку сосисок. Нарушается проницаемость сосудистой стенки (рис. 4-19, 4-20). Появление ишемических зон сетчатки, определяемых в основном при флюоресцентной ангиографии (рис. 4-21, см. рис. 4-25), говорит о прогрессировании заболевания и скором переходе процесса в пролиферативную форму с неоваскуляризацией и разрастанием глиозной ткани (рис. 4-22, 4-23, 4-24, 4-25, 4-26, 4-27, 4-28, 4-29, 4-30, 4-31, 4-32, 4-33, 4-34). В зависимости от распространённости глиозной ткани выделяют 4 степени глиоза:
- I степень — участки глиоза в заднем полюсе или средней части вдоль сосудистых аркад, не захватывающие диск зрительного нерва;
- II степень — глиоз диска зрительного нерва;
- III степень — глиоз диска зрительного нерва и в области сосудистых аркад;
- IV степень — циркулярные полосы глиоза, захватывающие диск, сосудистые аркады и темпоральные межаркадные зоны сетчатки.
Глиальная ткань может пролиферировать в стекловидное тело, вызывая тракцию и отслойку сетчатки.
Лечение
В терапии диабетической ретинопатии имеют значение режим питания и нормализация углеводного обмена (инсулин, пероральные сахароснижающие препараты). К настоящему времени сложилось мнение, что консервативное лечение диабетических изменений глазного дна малоэффективно. Наиболее целесообразно длительное назначение ангиопротекторов (доксиум, диваскан, предиан).
Методом выбора при диабетической ретинопатии является своевременная и адекватная лазерная коагуляция сетчатки.
При развитии фиброваскулярной ткани в центральной зоне возможно её хирургическое удаление с эндолазерной коагуляцией.
Осложнения
Гемофтальм, тракционная отслойка сетчатки и вторичная неоваскулярная глаукома — наиболее частые осложнения диабетической ретинопатии, лечение которых требует, как правило, хирургического вмешательства.
При рецидивирующем гемофтальме проводится витрэктомия или витрэктомия с транссклеральной криокоагуляцией сетчатки.
Тракционная отслойка сетчатки, сочетающаяся с очень грубой патологией глазного дна, практически инкурабельна.
В менее тяжёлых случаях проводят швартотомию и циркляж силиконовой лентой.
Развитие вторичной неоваскулярной глаукомы в начальной стадии требует дегидратационной терапии (диакарб, фуросемид), курсов субконьюнктивальных инъекций дексазона и инстилляций b-блокаторов (тимолол, арутимол, окупрес). При появлении выраженного стойкого болевого синдрома рекомендуется криопексия цилиарного тела.
Литература
- Кацнельсон Л.А. Клинические формы диабетической ретинопатии / / Вестник офтальмологии. — 1989. — № 5. — С. 43-47.
- Кацнельсон Л.А., Форофонова Т.И., Бунин А.Я. Сосудистые заболевания глаз. — М.: Медицинна, 1990. — С. 43-82.
- Little H. diabetic retinopathy. — New York: Thieme, 1983. — 396 р.
- Francis A.L’Esperance Jr.Ophthalmic lasers. Photocoagulation, photoradiation and surgery.- St.Louis-Toronto-London, — 1983.
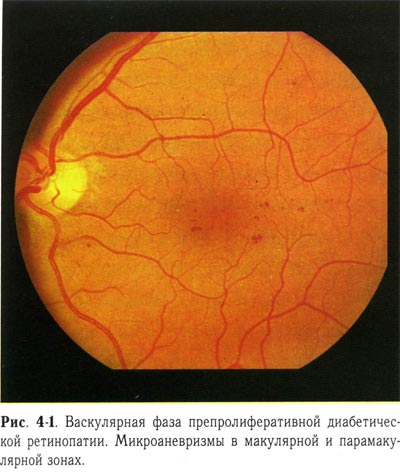 | Васкулярная фаза препролиферативной диабетической ретинопатии. Микроаневризмы в макулярной и парамакулярной зонах |
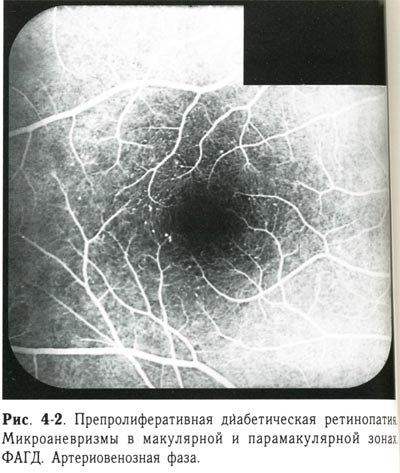 | Препролиферативная диабетическая ретинопатия. Микроаневризмы в макулярной и парамакулярной зонах. ФАГД. Артериовенозная фаза. |
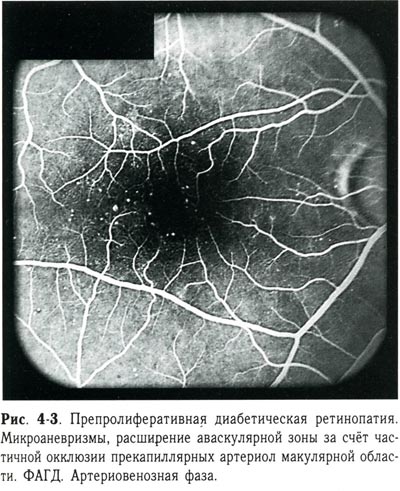 | Препролиферативная диабетическая ретинопатия. Микроаневризмы, расширение аваскулярной зоны за счет частичной окклюзии прекапиллярных артериол макулярной области ФАГД. Артериовенозная фаза. |
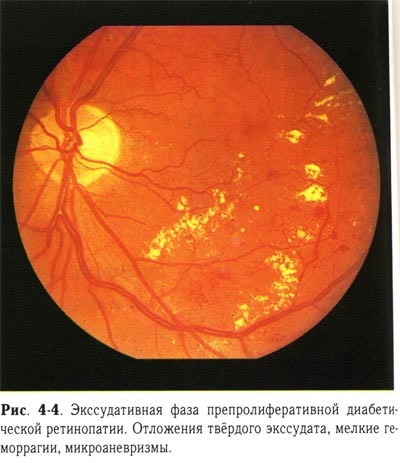 | Экссудативная фаза препролиферативной диабетической ретинопатии. Отложение твердого экссудата, мелкие геморрагии, микроаневризмы. |
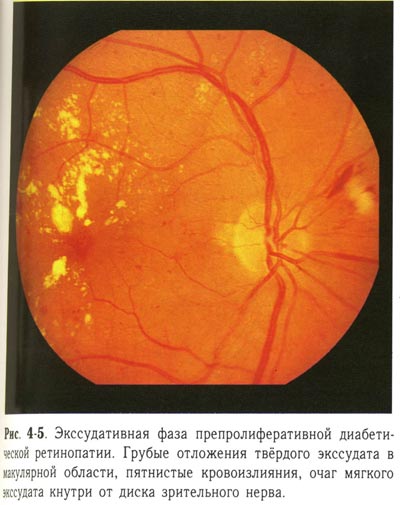 | Экссудативная фаза препролиферативной диабетической ретинопатии. Грубые отложения твердого экссудата в макулярной области, пятнистые кровоизлияния, очаг мягкого экссудата кнутри от ДЗН. |
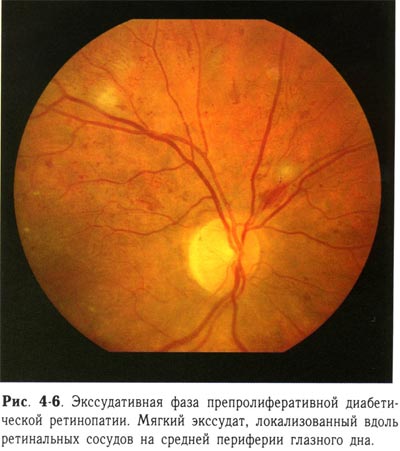 | Экссудативная фаза препролиферативной диабетической ретинопатии. Мягкий экссудат, локализованный вдоль ретинальных сосудов на средней периферии глазного дна. |
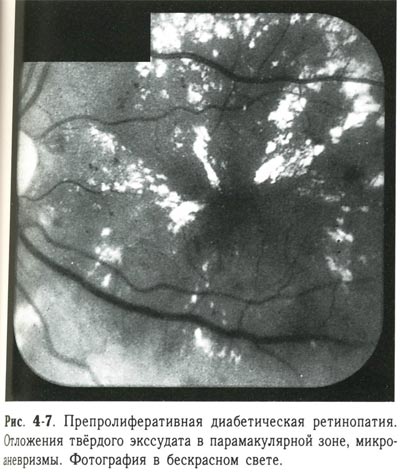 | Препролиферативная диабетическая ретинопатия. Отложения твердого экссудата в парамакулярной зоне, микроаневризмы. Фотография в бескрасном свете. |
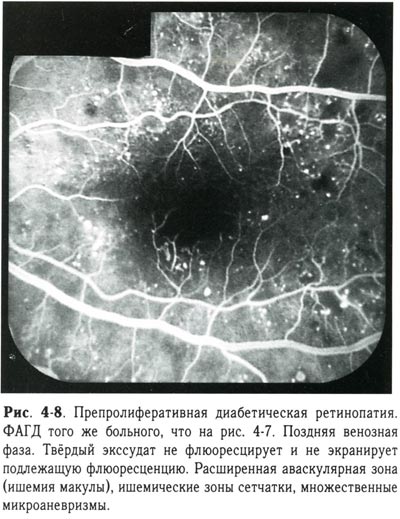 | Препролиферативная диабетическая ретинопатия. ФАГД того же больного, что и предыдущий снимок. Поздняя венозная фаза. Твердый экссудат не флюоресцирует и не экранирует подлежащую флюоресценцию. Расширенная аваскулярная зона (ишемия макулы), ишемические зоны сетчатки, множественные микроаневризмы. |
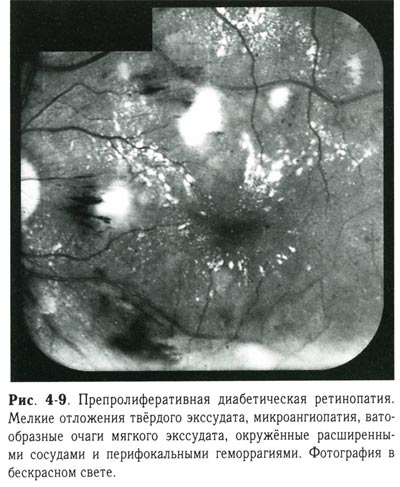 | Препролиферативная диабетическая ретинопатия. Мелкие отложения твердого экссудата, микроангиопатия, ватообразные очаги мягкого экссудата, окруженные расширенными сосудами и перифокальными геморрагиями. Фотография в бескрасном свете. |
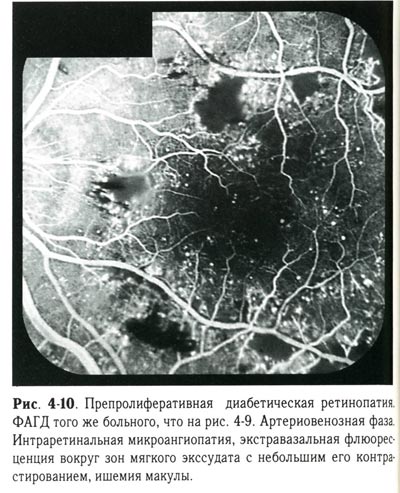 | Препролиферативная диабетическая ретинопатия. ФАГД того же больного, что и предыдущий снимок. Артериовенозная фаза. Интраретинальная микроангиопатия, экстравазальная флюоресценция вокруг зон мягкого экссудата с небольшим его контрастированием, ишемия макулы. |
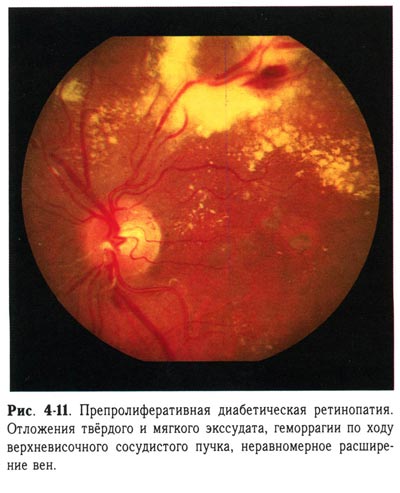 | Препролиферативная диабетическая ретинопатия. Отложения твердого и мягкого экссудата, геморрагии по ходу верхневисочного сосудистого пучка, неравномерное расширение вен. |
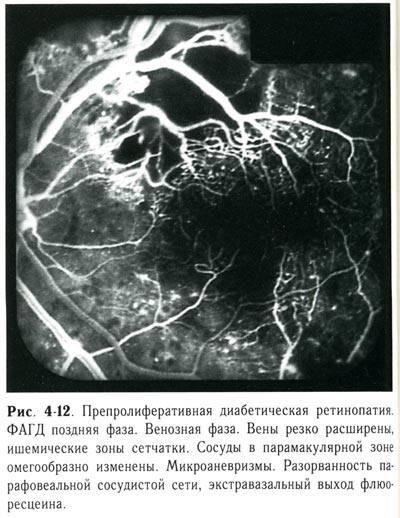 | Препролиферативная диабетическая ретинопатия. ФАГД поздняя фаза. Венозная фаза. Вены резко расширены, ишемические зоны сетчатки. Сосуды в парамакулярной зоне омегообразно изменены. Микроаневризмы. Разорванность парафовеальной сосудистой сети, экстравазальный выход флюоресцеина. |
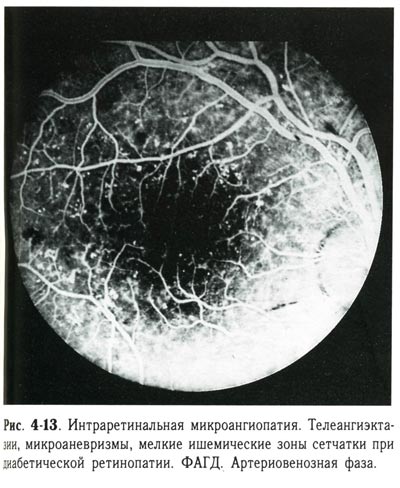 | Интраретинальная микроангиопатия. Телеангиэктазии, микроаневризмы, мелкие ишемические зоны сетчатки при диабетической ретинопатии. ФАГД. Артериовенозная фаза. |
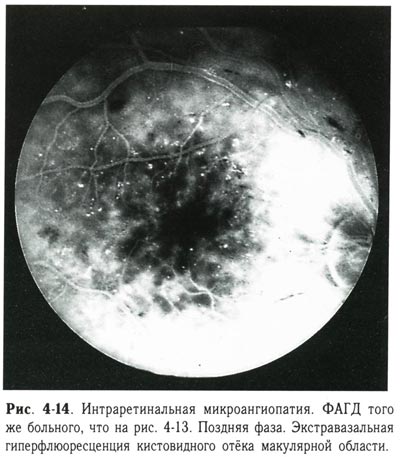 | Интраретинальная микроангиопатия. ФАГД того же больного, что и на предыдущем снимке. Поздняя фаза. Экстравазальная гиперфлюоресценция кистовидного отека макулярной области. |
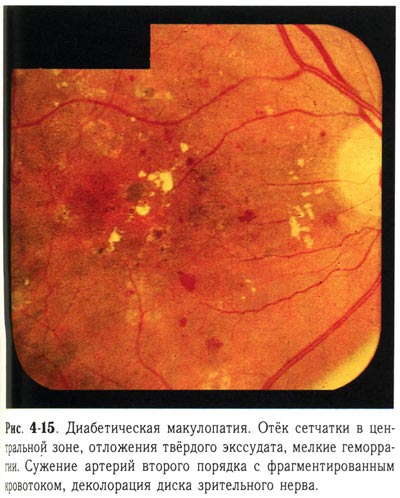 | Диабетическая макулопатия. Отек сетчатки в центральной зоне, отложения твердого экссудата, мелкие геморрагии. Сужение артерий второго порядка с фрагментированным кровотоком, деколорация ДЗН. |
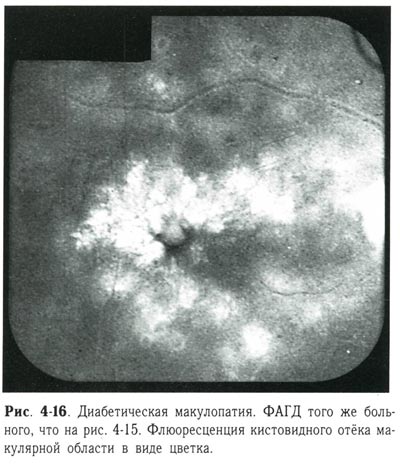 | Диабетическая макулопатия. ФАГД того же больного, что и на предыдущем снимке. Флюоресценция кистовидного отека макулярной области в виде цветка |
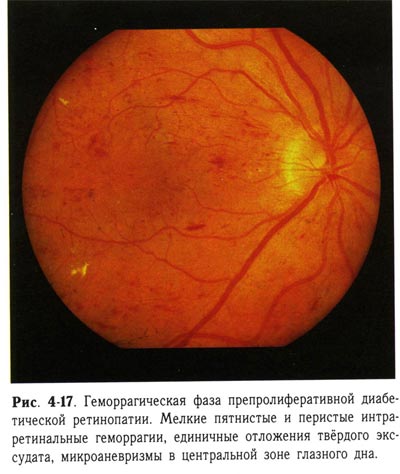 | Геморрагическая фаза препролиферативной диабетической ретинопатии. Мелкие пятнистые и перистые интраретинальные геморрагии, единичные отложения твердого экссудата, микроаневризмы в центральной зоне глазного дна. |
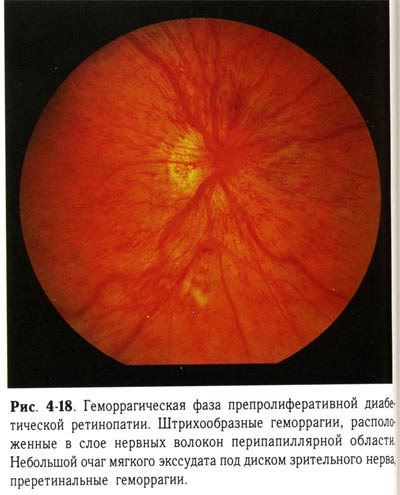 | Геморрагическая фаза препролиферативной диабетической ретинопатии. Штрихообразные геморрагии, расположенные в слое нервных волокон перипапиллярной области. Небольшой очаг мягкого экссудата под ДЗН, преретинальные геморрагии. |
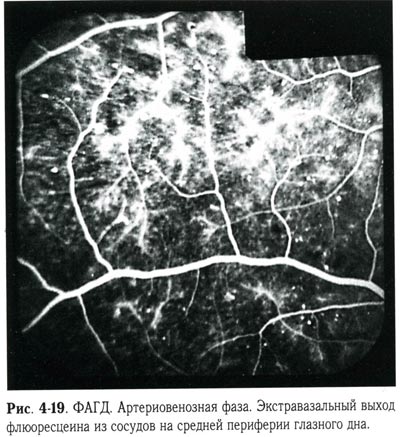 | ФАГД. Артериовенозная фаза. Экстравазальный выход флюоресцеина из сосудов на средней периферии глазного дна. |
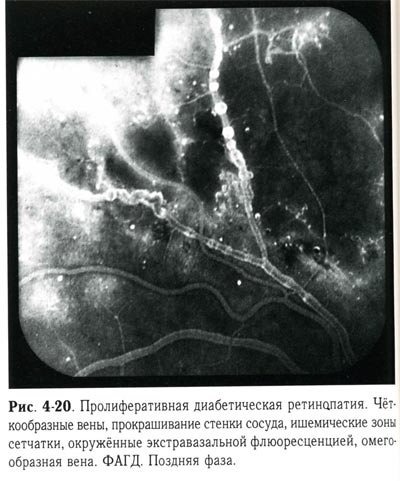 | Пролиферативная диабетическая ретинопатия. Четкообразные вены, прокрашивание стенки сосуда, ишемические зоны сетчатки, окруженные экстравазальной флюоресценцией, омегообразная вена. ФАГД. Поздняя фаза. |
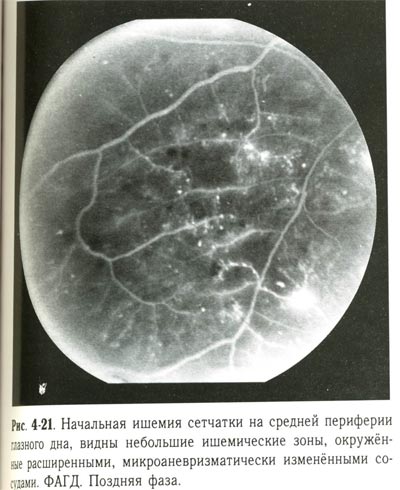 | Начальная ишемия сетчатки на средней периферии глазного дна, видны небольшие ишемические зоны, окруженные расширенными, микроаневризматически измененными сосудами. ФАГД. Поздняя фаза. |
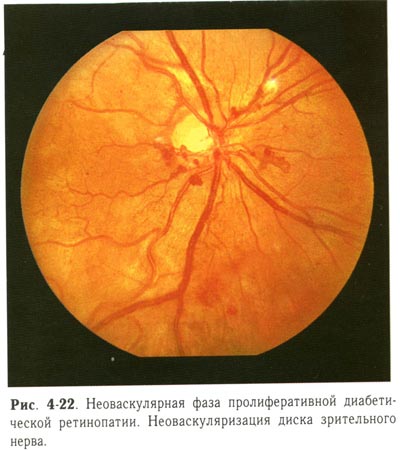 | Неоваскулярная фаза пролиферативной диабетической ретинопатии. Неоваскуляризация диска зрительного нерва. |
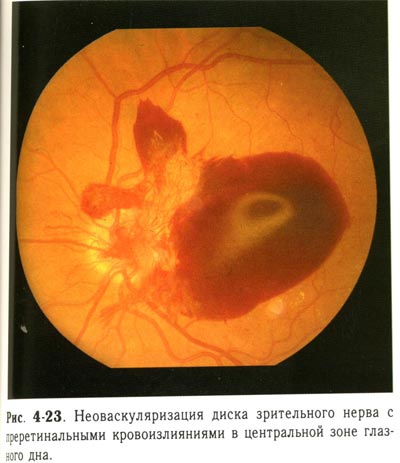 | Неоваскуляризация диска зрительного нерва с преретинальными кровоизлияниями в центральной зоне глазного дна. |
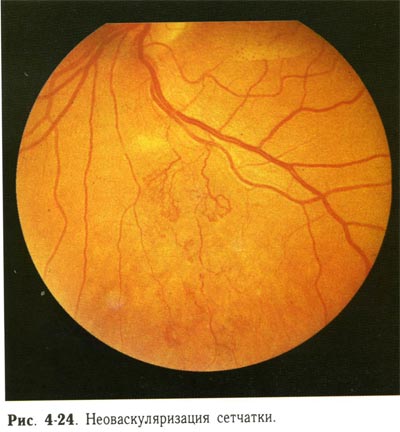 | Неоваскуляризация сетчатки. |
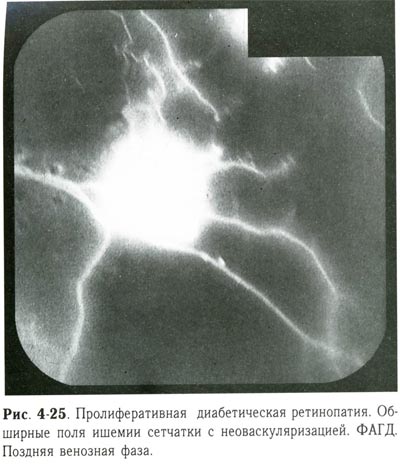 | Пролиферативная диабетическая ретинопатия. Обширные поля ишемии сетчатки с неоваскуляризацией. ФАГД. Поздняя венозная фаза. |
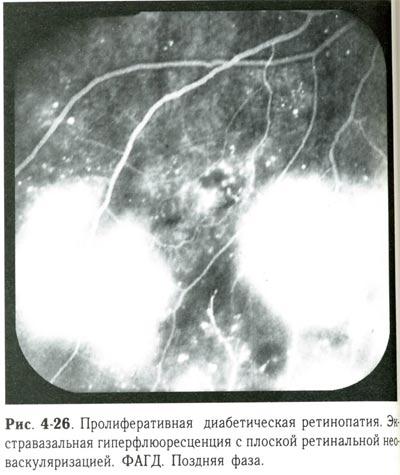 | Пролиферативная диабетическая ретинопатия. Экстравазальная гиперфлюоресценция с плоской ретинальной неоваскуляризацией. ФАГД. Поздняя фаза. |
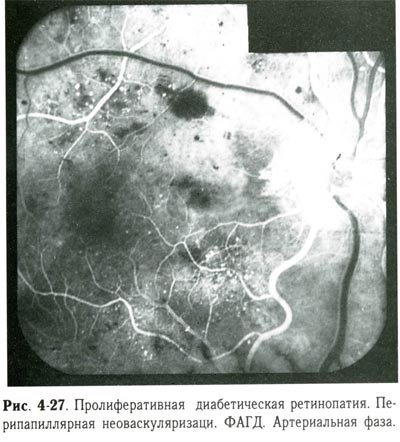 | Пролиферативная диабетическая ретинопатия. Перипапиллярная неоваскуляризация. ФАГД. Артериальная фаза. |
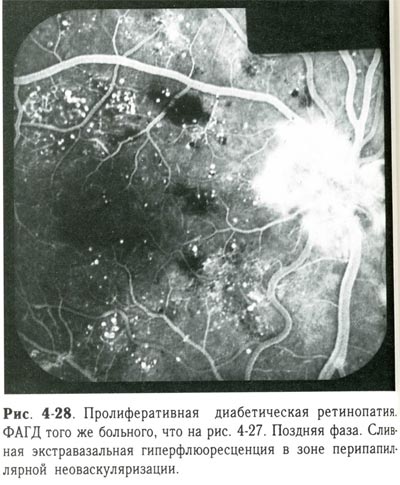 | Пролиферативная диабетическая ретинопатия. ФАГД того же больного, что и на предыдущем снимке. Поздняя фаза. Сливная экстравазальная гиперфлюоресценция в зоне перипапиллярной неоваскуляризации |
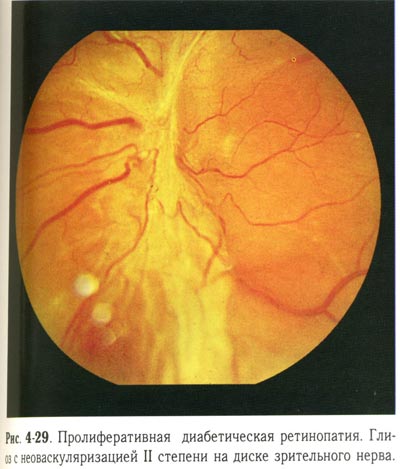 | Пролиферативная диабетическая ретинопатия. Глиоз с неоваскуляризацией второй степени на ДЗН. |
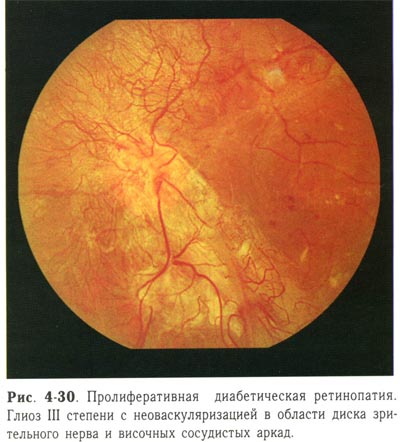 | Пролиферативная диабетическая ретинопатия. Глиоз третьей степени с неоваскуляризацией в области ДЗН и височных сосудистых аркад. |
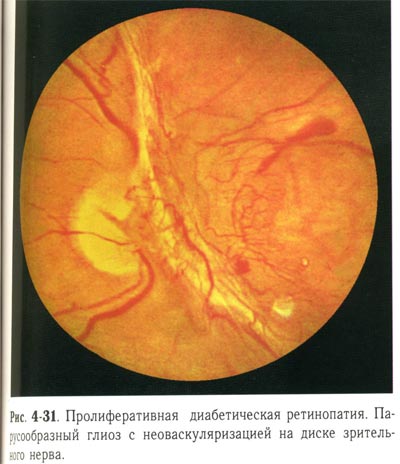 | Пролиферативная диабетическая ретинопатия. Парусообразный глиоз с неоваскуляризацией на ДЗН. |
 | Пролиферативная диабетическая ретинопатия. Начальный глиоз диска зрительного нерва с неоваскуляризацией. |
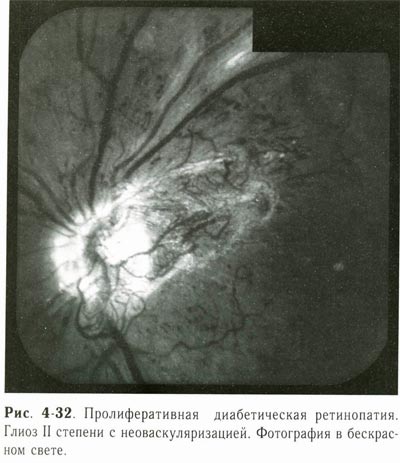
 | Пролиферативная диабетическая ретинопатия. Глиоз второй степени с неоваскуляризацией. Фотография в бескрасном свете. |
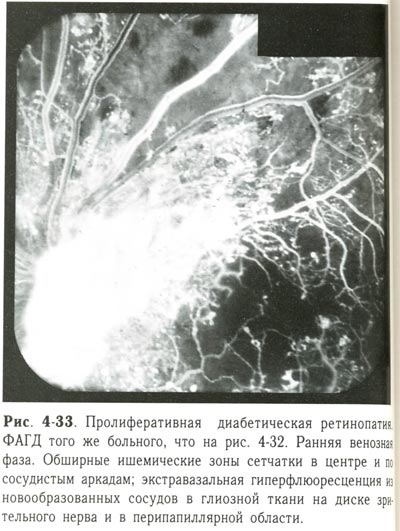 | Пролиферативная диабетическая ретинопатия. ФАГД того же больного, что и на предыдущем снимке. Ранняя венозная фаза. Обширные ишемические зоны сетчатки в центре и по сосудистым аркадам; экстравазальная гиперфлюоресценция из новообразованных сосудов в глиозной ткани на диске зрительного нерва и в перипапиллярной области. |
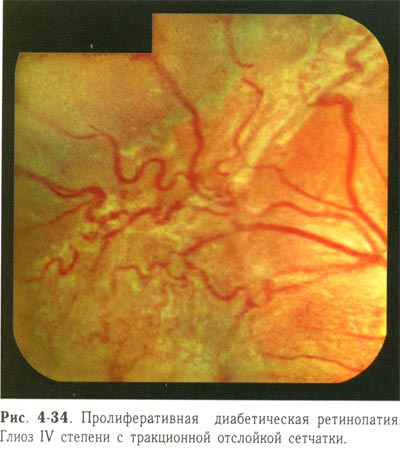 | Пролиферативная диабетическая ретинопатия. Глиоз четвертой степени с тракционной отслойкой сетчатки. |
К содержанию атласа патологии глазного дна
Источник
Тищенко О.Е.
1Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Пролиферативные заболевания сетчатки являются одной из причин слепоты и слабовидения во всем мире, самыми распространенными из которых являются пролиферативная диабетическая ретинопатия (ПДР) и экссудативная форма возрастной макулярной дегенерации (ВМД).
Для определения новых стратегических направлений в лечении офтальмологических заболеваний, связанных с развитием неоваскуляризции, необходимо иметь четкое представление о механизмах развития патологического ангиогенеза. Регуляция процессов формирования новообразованных сосудов, с точки зрения современных представлений, осуществляется благодаря наличию системы, связанных между собой, стимулирующих и ингибирующих факторов. Нарушение баланса в этой системе — между ангиогенными и антиангиогенными факторами приводит к развитию патологического ангиогенеза [37].
В настоящее время известно большое количество ангиогенных или, как их еще принято называть, — вазопролиферативных факторов, которые прямо или опосредованно влияют на ангиогенез. К ним относятся кислый и основной фактор роста фибробластов (aFGF, bFGF), инсулиноподобный фактор роста, фактор роста гепатоцитов (HGF), трансформирующий фактор роста b (TGF-b). Ключевым фактором ангиогенеза в норме и патологии, благодаря его биологическим свойствам, принято считать эндотелиальный сосудистый фактор роста (Vascular Endothelial Growth Factor-VEGF) [13].
VEGF принадлежит к семейству пептидных факторов. В настоящее время идентифицировано 8 его изоформ, отличающихся по количеству образующих аминокислот; наиболее распространенной из, которых, является изоформа VEGF-165.
Экспрессируется VEGF в хориоидее и сетчатке — перицитах и эндотелиоцитах, клетках пигментного эпителия и клетках Мюллера, ганглионарных клетках и глиальных [26].
Основным стимулом к повышению его экспрессии является гипоксия [36]. Кроме того, установлено, что усиливают продукцию VEGF некоторые противовоспалительные цитокины (IL-1 и IL-6) и ростовые факторы (Epidermal Growth Factor, Transforming Growth Factor).
Основные биологические эффекты VEGF проявляются при его взаимодействии с двумя основными видами рецепторов — VEGFR1 и VEGFR2, расположенных преимущественно на эндотелиоцитах и клетках Мюллера. Активация рецепторов VEGFR2 в процессах ангиогенеза играет ключевую роль, так как приводит к повышению сосудистой проницаемости [14].
За счет взаимодействия с рецепторами VEGF индуцирует комплекс механизмов формирования сосудов, который включает в себя пролиферацию эндотелиоцитов, их миграцию и индукцию синтеза металлопротеиназ — ферментов, необходимых для инвазии новообразованных сосудов в окружающие ткани [42].
В связи с тем, что VEGF играет роль одного из ведущих факторов в развитии патологической неоваскуляризации, целесообразно было предположить, что возможность ингибировать его действие — это возможность предотвратить развитие патологического ангиогенеза и, связанной с ним офтальмопатологии.
В настоящее время с этой целью используются несколько лекарственных препаратов — пегаптаниб (Макуджен) — селективный ингибитор VEGF-165, ранибизумаб (Луцентис) и бевацизумаб (Авастин) — блокаторы всех изоформ VEGF.
Пегаптаниб (Макуджен) по химической структуре представляет собой аптамер, связывающий изоформу VEGF-165. На основании проведения ряда клинических исследований пациентов с ВМД и субретинальной неоваскулярной мембраной (СНМ) субфовеолярной локализации было установлено, что данный препарат по эффективности не уступает ФДТ, при его применении наблюдается стабилизация и повышение зрительных функций [15].
Ранибизумаб (Луцентис) представляет собой Fab-фрагмент полноразмерного рекомбинантного моноклонального антитела ко всем изоформам VEGF. Эффективность данного препарата была доказана также при ВМД с СНМ всех типов с субфовеолярной локализацией [22].
Бевацизумаб (Авастин) — полноразмерное рекомбинантное моноклональное антитело ко всем изоформам VEGF.
Проведено большое количество научно-клинических исследований, посвященных его применению при ВМД со всеми типами хориоидальной неоваскуляризации с субфовеолярной локализацией [3, 35]. Обобщенные результаты свидетельствуют о том, что при его применении также наблюдается стабилизация (в 52,8-56% случаев) и повышение остроты зрения (в 30,4-43% случаев).
Положительный эффект, по результатам исследований ряда авторов, был получен и при применении бевацизумаба при ПДР. Наблюдался значительный и быстрый регресс новообразованных сосудов при его интравитреальном введении [2].
Высокая эффективность и относительно невысокая цена бевацизумаба, по сравнению с аналогичными препаратами (пегаптаниб, ранибизумаб) и ФДТ является основанием для проведения в настоящее время дальнейших широкомасштабных экспериментальных и клинических исследований, посвященных его применению в офтальмологии. В связи с тем, что в официальном перечне показаний для его применения отсутствуют офтальмологические заболевания (применяется «off-label») требуется проведение целого ряда дополнительных научно-исследовательских мероприятий.
Однако, несмотря на высокую эффективность, препараты, блокирующие сосудистый эндотелиальный фактор роста, особенно все его изоформы, продолжают вызывать некоторые опасения. Возможными осложнениями при применении бевацизумаба являются — артериальная гипертензия, острое (инфаркт миокарда, инсульт) и хроническое нарушение кровообращения (хроническая сердечная недостаточность, ишемия сосудов головного мозга), тромбоз глубоких вен [46]. В связи с этим при применении бевацизумаба авторы исключали из своих исследований пациентов с некомпенсированной артериальной гипертензией, инфарктом миокарда в анамнезе и нарушением функции сосудов головного мозга [3]. В результате проведения крупных клинических исследований (VISION, MARINA, ANCHOR, FOCUS) было уставлено, что при ВМД пегаптаниб (селективный блокатор VEGF-165) менее эффективен, чем ранибизумаб (блокирует все изоформы VEGF), но риск нежелательных осложнений при его применении значительно меньше. Сообщается об увеличении частоты сердечно-сосудистых нарушений, острых нарушений кровообращения головного мозга и кровотечений, по сравнению с группой плацебо, при применении ранибизумаба, однако, полученные различия не были статистически значимы.
Ряд авторов сообщает о некоторых других нежелательных эффектах данной группы препаратов. VEGF принимает участие в обеспечении жизнедеятельности хориокапилляров [24]; при интравитриальном введении бевацизумаба и, соответственно, снижении уровня его содержания наблюдались случаи атрофии хориокапилляриса у пациентов. Кроме этого VEGF в условиях ишемии сетчатки обладает нейропротективным действием [28]. Отсутствие этого эффекта в результате его блокады может привести к дальнейшему прогрессированию нейрональных повреждений [23].
В эксперименте при интравитреальном введении бевацизумаба, по результатам электронной микроскопии, было выявлено митохондриальное разрушение во внутреннем сегменте фоторецепторов и усиление апоптоза [18].
Накопленный клинический опыт свидетельствует о высокой эффективности анти-VEGF-препаратов в лечении заболеваний, сопровождающихся неоваскуляризацией и патологической проницаемостью сосудов. Однако, учитывая необходимость длительного лечения данной патологии, требуется проведение дополнительных экспериментальных и клинических исследований, которые позволят определить не только положительные, но ивозможные отрицательные побочные эффекты.
Поэтому изучение и разработка новых подходов в подавлении нежелательных патологических эффектов VEGF и одновременное сохранение нейропротективных и нейротрофических свойств может стать значимым прорывом в лечении данных заболеваний.
Большие надежды возлагаются на фактор пигментного эпителия (Pigment Epithelium-Derived Factor-PEDF), который является мощным эндогенным ингибитором ангиогенеза и обладает нейротрофическими и нейропротективными свойствами.
Впервые PEDF был обнаружен в культуральной среде человеческих клеток пигментного эпителия сетчатки, как белок с нейротрофической активностью. Было установлено, что PEDF является индуктором нейрональной дифференцировки клеток в культуре клеток ретинобластомы и авторы делают вывод о том, что PEDF играет важную роль в развитии и дифференцировке нервной ткани сетчатки [43].
В следующей работе установлено, что PEDF — белок с молекулярной массой 50 kDa и синтезируется в эмбриональных клетках ретинального пигментного эпителия. Ген PEDF в эмбриональных человеческих клетках является активным уже в 17 недель, что свидетельствует о вовлечении PEDF в развитие нервной ткани на ранних этапах [44].
Анализ последовательности ДНК показал, что молекула PEDF родственна серпиновому семейству сериновых протеаз [38].
Далее фактор пигментного эпителия был обнаружен в фоторецепторах и ретинальном пигментном эпителии, из которого он секретируется в интерфоторецепторный матрикс. PEDF локализуется во внутренних слоях сетчатки, хориоидее, цилиарном теле, в роговичном эпителии и эндотелии, в водянистой влаге, в высоких концентрациях содержится в стекловидном теле [5].
В связи с тем, что PEDF проявляет нейротрофическую активность в культуре опухолевых клеток (ретинобластома), возникло предположение, что это свойство должно проявляться и в отношении нейронов без патологии. В связи с этим было проведено исследование свойств рекомбинантного PEDF в культурах нормальных мозжечковых гранулярных клетках. Авторами было установлено, что PEDF значительно увеличивает клеточную жизнеспособность, не оказывая влияния на митотическую активность [41].
При более детальных исследованиях было установлено, что гибель клеток в культуре мозжечковых гранулярных клеток является естественным апоптозом, а PEDF является мощным ингибитором, как естественного, так и вызванного апоптоза [1].
Влияние PEDF не ограничивается только мозговыми нейронами. Было выявлено, что PEDF способствует дифференцировке и выживанию развивающихся спинных моторных нейронов [17]. В другой работе было установлено, что в органотипической культуре на модели моторной нейрональной дегенерации, в присутствии PEDF сохраняется морфологическая структура и общее количество нейронов [7].
PEDF обладает достаточно выраженными нейротрофическими свойствами, как при хроническом, так и при остром нейротоксическом повреждении; активно защищает мозжечковые гранулярные клетки при глутаматном токсическом повреждении [40], поддерживает клеточную жизнеспособность за счет уменьшения апоптоза, вызванного перекисью водорода, в культуре крысиных ретинальных нейронов [9].
При наследственной ретинальной дегенерации сетчатки у мышей, характеризующейся гибелью фоторецепторов, PEDF также проявил свойства ингибитора апоптоза, тем самым, увеличив выживаемость фоторецепторов [11].
Анализ активности PEDF на модели повреждения фоторецепторов, связанной с потерей пигментного эпителия (эмбриональная культура сетчатки лягушек без пигментного эпителия) показал, что PEDF при отсутствии пигментного эпителия поддерживает нормальное развитие фоторецепторов и экспрессию опсина [19].
При интравитреальном введении PEDF крысам с последующим воздействием повреждающих уровней освещенности, было установлено, что он обладает защитным действием на фоторецепторы от светового повреждения [10]. В культуре крысиных ретинальных ганглиозных клеток при глутаматном повреждении PEDF предохранял данные клетки от гибели [34].
При проведении клинических исследований было выявлено снижение уровня содержания PEDF в тканях глаза у пациентов с глаукомой [31] и миопией высокой степени, особенно с хориоретинальной дистрофией [29]. Авторы предполагают, что это может быть связано с гибелью при этой патологии ганглиозных клеток и клеток пигментного эпителия сетчатки, которые синтезируют PEDF.
В настоящее время PEDF представляет собой большой интерес для офтальмологов, не столько как фактор с нейротрофическими и нейропротективными свойствами, сколько, как один из главных эндогенных ингибиторов ангиогенеза [4]. Он обладает мощной антиангиогенной активностью, ингибирует миграцию и пролиферацию эндотелиальных клеток, которые играют основную роль в развитии патологической васкуляризации.
Выявлено, что PEDF поддерживает антиангиогенные свойства стекловидного тела и роговицы. В сетчатке физиологическое действие PEDF регулируется концентрацией кисл


