Лазеркоагуляция сетчатки у недоношенных
Володин П.Л., Яблокова И.А., Узунян Д.Г.
Актуальность.
На современном этапе развития отрасли здравоохранения проблема ретинопатии недоношенных остается актуальной, а поиск новых технологий в диагностике и лечении такой особой группы пациентов, как недоношенные дети, – необходимым и востребованным. За 2015 г. только в Московской области родилось почти 4 тыс. недоношенных детей, из них более 200 младенцев – с экстремально низкой массой тела (ЭНМТ) при рождении, у которых риск развития ретинопатии наиболее высок и чаще наблюдается неблагоприятный тип течения заболевания [2].
В то же время остаются нерешенными вопросы своевременного выявления и направления детей с прогрессирующей ретинопатией недоношенных, требующих незамедлительного лечения, что зачастую связано с нехваткой квалифицированных кадров, тяжелым соматическим состоянием недоношенных детей в первые месяцы жизни, трудоемкостью осмотра периферии глазного дна [3-5].
В связи с этим частота первичного выявления детей с тяжелыми постпороговыми стадиями активной ретинопатии недоношенных остается достаточно высокой, что требует разработки и модификации тактики лечения пациентов из этой группы.
Цель.
Разработать тактику ведения детей с тяжелыми стадиями активной ретинопатии недоношенных.
Материал и методы.
Под нашим наблюдением находилось 197 детей с активными стадиями ретинопатии недоношенных, из них 132 детям потребовалось лазерное лечение. В 48 случаях (96 глаз) была выявлена тяжелая постпороговая стадия активной ретинопатии недоношенных (наличие высокого вала с экстраретинальной пролиферацией протяженностью 6 и более непрерывных или 9 и более суммарных часовых меридианов в сочетании с «плюс-болезнью»).
Анализ гестационного возраста и массы тела при рождении в данной группе пациентов представлен в табл.
Средний гестационный возраст составил 29,1±2,3 недели, масса тела при рождении – 1050±280 г. Средний возраст на момент операции – 36,3±1,5 недели.
Учитывая характер течения заболевания и риск прогрессирования процесса с развитием тракционной отслойки сетчатки при проведении коагуляции в стандартном объеме, нами предложена модифицированная методика коагуляции тяжелых постпороговых стадий активной ретинопатии недоношенных [1].
Модификация методики заключалась в расширении объема коагуляции с нанесением лазерных аппликаций центральнее вала и оптимизации параметров лазерного излучения.
Для уточнения стадии и степени активности процесса детям из группы наблюдения проводились бинокулярная офтальмоскопия, цифровая ретиноскопия и флуоресцентная ангиография (ФАГ на широкоугольной педиатрической ретинальной камере «Retcam-3»), В-сканирование и ультразвуковая биомикроскопия (УБМ).
Предварительно все дети были осмотрены педиатром и анестезиологом, получено письменное информированное согласие родителей на проведение ряда обследований под масочным севофлюрановым наркозом.
Проведенное комплексное обследование подтвердило наличие высокой активности процесса (по данным ФАГ) у большинства детей с 3 постпороговой стадией. В одном случае методом ультразвуковой биомикроскопии выявлена локальная периферическая отслойка сетчатки в 3-й зоне, у одного ребенка активности процесса не выявлено, наблюдался частичный самопроизвольный регресс, в дальнейшем в анализ данные пациенты не вошли (48-2=46 детей).
Все пациенты с подтвержденной активной постпороговой ретинопатией недоношенных разделены на 2 группы.
В основную группу вошли 24 пациента, лазеркоагуляция которым проводилась в паттерновом режиме по модифицированной методике одномоментно.
В группу контроля были включены 22 ребенка. Лазеркоагуляция в этой группе проводилась в 2 этапа, первым этапом проведена стандартная лазеркоагуляция аваскулярных зон сетчатки на сканирующем полуавтоматическом офтальмокоагуляторе Паскаль (рис. 1). Вторым этапом проводилась дополнительная лазеркоагуляция васкулярной сетчатки перед валом экстраретинальной пролиферации в случае прогрессирования процесса.
Все пациенты были сопоставимы по возрасту на момент операции, массе тела при рождении, гестационному сроку и степени выраженности клинических проявлений.
Результаты.
В основной группе после применения модифицированной методики лазеркоагуляции у всех 24 пациентов (48 глаз – 100%) достигнута стабилизация и регресс заболевания через 2 недели после операции. При осмотре через 3 мес. выявлено полное исчезновение признаков экстраретинальной пролиферации, сепарация витреоретинальных тяжей в зоне вала пролиферации, рост концевых сосудов между лазеркоагулятами.
В группе контроля в 10 случаях (10 глаз, 5 детей – 23%) после проведения лазеркоагуляции сетчатки в стандартном объёме при осмотре через 2 недели после операции стабилизация процесса отсутствовала, отмечался продолженный рост экстраретинальной пролиферации, сохранялся высокий вал пролиферации с приподнятостью сетчатки центральнее вала. После проведения второго этапа лазеркоагуляции по модифицированной методике перед валом регресс заболевания достигнут на 9 глазах (рис. 2а-г). В одном случае в связи с прогрессированием заболевания была проведена витреоретинальная операция.
У 17 детей (34 глаза) регресс заболевания достигнут после проведения первого этапа лазеркоагуляции в сроки 2 недели после операции, второй этап не проводился.
Выводы.
Полученные результаты исследования позволяют рекомендовать применение модифицированной методики лазерного лечения при выявлении тяжелых стадий активной ретинопатии недоношенных.
Эффективность лазеркоагуляции аваскулярных зон сетчатки в стандартном объеме в постпороговых стадиях значительно снижена, что ведет к высокому риску дальнейшего прогрессирования заболевания с развитием тракционной отслойки сетчатки.
Предложенная модифицированная технология лазерного лечения недоношенных детей позволяет повысить число благоприятных исходов РН, а также значительно сократить время и количество наркозных пособий у данной тяжелой категории пациентов.
Источник
Тухбатуллина Л.Ф., Назаров П.В.
Ретинопатия недоношенных (РН) — тяжелое вазопролиферативное заболевание, развивающееся преимущественно у глубоко недоношенных, незрелых детей, поздняя выявляемость которого приводит к потере зрения и ранней инвалидизации [7]. Частота встречаемости РН составляет от 6,9 до 37,4 % среди детей группы риска. В 22 % случаев заболевание прогрессирует до пороговой стадии [8].
Современным способом лечения ретинопатии недоношенных является лазеркоагуляция сетчатки.
Показанием к проведению лазерной коагуляции сетчатки при РН является пороговая стадия III (+) болезнь в зоне 2 или 3 с распространением экстраретинальной пролиферации на 5 последовательных или 8 суммарных часовых меридианов или при любом проявлении болезни в зоне 1 [4].
Возможна одномоментная и этапная лазеркоагуляция сетчатки, при которой сначала коагулируют часть аваскулярной зоны, затем, спустя некоторое время — оставшуюся сетчатку. Однако при тяжелых формах РН одномоментное вмешательство более эффективно [1].
Лазерная коагуляция сетчатки в зависимости от зоны локализации процесса может осуществляться транссклеральным или транспупиллярным доступом [4].
При применении бесконтактной лазеркоагуляции с использованием налобного офтальмоскопа некоторые авторы отмечают возможность возникновения таких интраоперационных осложнений, как повреждение хрусталика и радужки [14].
В настоящее время разработана методика транспупиллярной лазерной коагуляции сетчатки с использованием контактной линзы, при которой достигается широкое поле обзора, что повышает эффективность лазеркоагуляции, и снижается число осложнений [3].
Методика коагуляции заключается в массивной и плотной коагуляции поверхности аваскулярной сетчатки второй и третьей зон глазного дна: одномоментное нанесение от 960 до 2250 лазерных коагулятов, диаметр пятна — 400–600 мкм, промежуток: 0,5–1 диаметр коагулята.
При задней агрессивной форме РН коагуляты наносятся также и в I зоне на участки ишемии и экссудации. В работе используется широкоугольная контактная линза для панретинальной коагуляции модели «Mainster wide field» (компания Ocular Instruments, США) со статическим полем зрения 120 градусов. При ригидном зрачке и невозможности достижения оптимального мидриаза используется широкоугольная линза для проведения лазерной коагуляции сетчатки модели «Quad Pediatric Laser Lens» (компания Volk, США). Лазеркоагуляция выполняется в течение 1–3 суток после обнаружения патологии. При III стадии РН уже после выполнения одного сеанса лазеркоагуляции отмечается стабилизация процесса в подавляющем большинстве случаев [2].
Существуют методики, при которых используются фотосенсибилизаторы с целью снижения суммарной энергии лазерного воздействия на сетчатку, уменьшения продолжительности сеанса лазеркоагуляции и наркозного пособия недоношенному ребенку.
Новым способом лазеркоагуляции при РН является лазеркоагуляция по валу. Эффективность данного метода подтверждается данными флюоресцентной ангиографии [16].
В последнее время зарубежом в лечении задней агрессивной РН делают попытки использовать препараты, обладающие антиангиогенным действием (бевацизумаб), как изолированно, так и в сочетании с лазеркоагуляцией сетчатки и витреальной хирургией [9, 11, 13]. Но в отечественной детской офтальмологии бевацизумаб не разрешен для применения [5].
В 2005 году в клиническую практику была внедрена технология паттерной лазерной коагуляции, которая автоматизировала процедуру нанесения коагулятов: одним нажатием педали наносится несколько аппликаций в заранее определенной последовательности в виде паттерна [10].
Основными преимуществами методики транспупиллярной паттерной сканирующей лазеркоагуляции сетчатки при лечении РН являются: сокращение длительности лазерного воздействия и наркозного пособия недоношенному ребенку, повышение эффективности и безопасности лечения, точности постановки лазерных коагулятов, исключение возможности перекрывания лазерных пятен между собой, и, соответственно, эффекта гиперкоагуляции; возможность выполнения лазерной коагуляции необходимой площади аваскулярной сетчатки за один сеанс вне зависимости от локализации патологического процесса; значительно снижается риск осложнений за счет оптимизации параметров лазерной энергии, а также частота неблагоприятных исходов заболевания [5, 6].
Своевременно проведенная лазерная коагуляция сетчатки при пороговых стадиях РН позволяет достичь редукции процесса в подавляющем числе случаев [2].
Однако, число и плотность лазерного пятна остается дискуссионным вопросом. Лазеркоагуляты могут быть нанесены в рассеянный узор, почти сливающийся узор или иметь сливной характер. У пациентов, получивших сливную лазерную коагуляция, была низкая скорость прогрессирования заболевания [12, 15].
Вопрос о лучшем способе лазерного лечения при ретинопатии недоношенных остается дискутабельным и требует дальнейшего изучения.
Источник
Лазерное лечение ретинопатии недоношенных (РН) детей. Техника
Как упоминалось ранее, показаниями для лазерной коагуляции при ретинопатии недоношенных новорожденных являются поражение зоны II при наличии «плюс-болезни» (независимо от обширности области неоваскуляризации) и неоваскуляризация в зоне I, независимо от наличия «плюс-болезни».
Проведение анестезии при лазерном лечении ретинопатии недоношенных новорожденных. Авторы статьи предпочитают проводить лазерное лечение в неонатальном блоке интенсивной терапии (НБИТ) на фоне легкой внутривенной седации при мониторировании состояния пациента и обезболивания опиатами, без использования эндотрахеального наркоза во всех случаях, когда это возможно.
Техника выполнения лазерной коагуляции имеет большое значение для уменьшения продолжительности процедуры и вероятности осложнений со стороны других органов и систем. К сожалению, часто требуется проведение эндотрахеальной анестезии в связи с тяжестью сопутствующей сердечно-сосудистой патологии и интраоперационной десатурацией кислородом и брадикардией.
Тем не менее интубации у многих детей можно избежать, если на начальных этапах выполнения лазерной коагуляции пациент хорошо переносит лечение. Авторы статьи считают необходимым всегда проводить лечение в условиях операционной под контролем опытного детского анестезиолога или в неонатальном блоке интенсивной терапии (НБИТ) при доступности немедленного перехода на ИВЛ и при постоянном наблюдении пациента командой неонатологов.
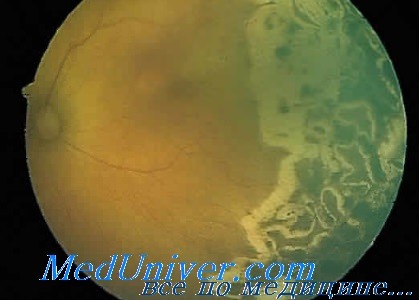
Техника выполнения лазерной коагуляции при лечении ретинопатии недоношенных новорожденных
Авторы статьи выполняют лазерную коагуляцию с помощью лазера, излучающего в БИК-диапазоне (длина волны 810 нм). Преимуществом использования данного типа лазера является меньшее поглощение энергии сосудистой оболочкой хрусталика, которое может привести к развитию катаракты. Целью лечения является нанесение сливных лазерных коагулятов по всей ава-скулярной области сетчатки.
Крайне важно в конце процедуры произвести осмотр всего глазного дна методом непрямой офтальмоскопии, чтобы быть уверенным, что все участки аваскулярной сетчатки были коагулированы и что отсутствуют зазоры между коагулятами. Для ротации глазного яблока в целях обеспечения визуального контроля при проведении лазерной коагуляции наиболее периферических участков сетчатки используют депрессор склеры.
Депрессию склеры следует осуществлять осторожно, чтобы уменьшить проявления глазосердечного рефлекса и минимизировать вероятность прогрессивного помутнения оптических сред во время лазерной коагуляции. Авторы книги редко считают необходимым повторное выполнение коагуляции, в большинстве случаев достаточно однократной процедуры сливной лазерной коагуляции. Исключением является агрессивная задняя уменьшения продолжительности процедуры и вероятности осложнений со стороны других органов и систем.
К сожалению, часто требуется проведение эндотрахеальной анестезии в связи с тяжестью сопутствующей сердечно-сосудистой патологии и интраоперационной десатурацией кислородом и брадикардией.
Тем не менее интубации у многих детей можно избежать, если на начальных этапах выполнения лазерной коагуляции пациент хорошо переносит лечение. Авторы книги считают необходимым всегда проводить лечение в условиях операционной под контролем опытного детского анестезиолога или в неонатальном блоке интенсивной терапии (НБИТ) при доступности немедленного перехода на ИВЛ и при постоянном наблюдении пациента командой неонатологов.
— Также рекомендуем «Лечение IVa стадии ретинопатии недоношенных новорожденных. Тракционная отслойка сетчатки (ТОС)»
Оглавление темы «Лечение заболеваний глаз»:
- Лазерное лечение ретинопатии недоношенных (РН) детей. Техника
- Лечение IV стадии ретинопатии недоношенных новорожденных. Тракционная отслойка сетчатки (ТОС)
- Лечение V стадии ретинопатии недоношенных новорожденных. Рекомендации
- Неудачное лазерное лечение ретинопатии недоношенных новорожденных. Организация медицинской помощи
- Терапия ретинопатии недоношенных новорожденных антагонистами СЭФР. Рекомендации
- Техника 25G витрэктомии при ретинопатии недоношенных детей. Рекомендации
- Поражение глаз Toxocara canis. Техника операции
- Осложнения кератопротезирования. Группы заболеваний
- Техника витрэктомии у пациентов с кератопротезами. Рекомендации
- Пенетрация глазного яблока: диагностика, лечение
Источник
Столяров М.В.
Актуальность
Ретинопатия недоношенных (РН) является тяжелым вазопролиферативным заболеванием, которое возникает у глубоко недоношенных младенцев и характеризуется неоваскуляризацией сетчатки, создающей высокий риск необратимой слепоты [10,12].
Совершенствование акушерской и неонатальной помощи приводит к повышению выживаемости детей с экстремально низкой массой тела.
К настоящему времени, среди проблем перинатальной медицины на первое место выходит РН [8,9].
Проведение лазерной коагуляции аваскулярной сетчатки (ЛКС) является единственным доказанным и наиболее эффективным способом лечения активной стадии РН [4,11,13], хотя, в то же время, нет абсолютных гарантий благоприятного исхода заболевания даже после лазерного лечения [1,4].
Недоношенные дети являются пациентами с высокой степенью операционно-анестезиологического риска. В структуре сопутствующей патологии у них имеют место тяжелые поражения нервной, сердечно-сосудистой систем, обусловленные их недоразвитием: перинатальное поражение ЦНС различной степени тяжести, тканевая гипоксия, внутрижелудочковые кровоизлияния, гипертензионно-гидроцефальный синдром; бронхолегочная дисплазия, пневмония новорожденных, респираторный дистресс-синдром новорождённых, кислородная зависимость и др.; врожденные пороки сердца, особенно гемодинамически значимые; внутриутробные инфекции [2].
Совокупность существенных отягощающих моментов на фоне экстремально низкой массы тела предъявляют особо высокие требования к анестезиологическому обеспечению и безопасности оперативных вмешательств, при лечении ретинопатии недоношенных РН.
Проблемы анестезии новорожденных с РН при выполнении им лазеркоагуляции сетчатки в литературе мало освещены. В нашей клинике ЛКС активно проводится с 2008 года [3-7,11].
Ввиду этого мы сочли целесообразным оценить собственный опыт проведения анестезий такой особой соматически отягощенной группы маленьких пациентов, поделиться накопленным опытом.
Цель
Сравнительный анализ клинической эффективности и безопасности проведения общей ингаляционной анестезии галотаном и севораном у недоношенных детей при ЛКС.
Материал и методы
За период с 2008 по 2017 год ЛКС выполнены 302 младенцам. Возраст детей варьировал от 28 дней до 4 мес. (метод сплошной выборки). Масса тела детей варьировала от 1420 до 4200 г.
Во всех случаях имели место 3-4 стадии РН. Подготовка к наркозу и операции включала: ограничение приема пищи и жидкости – не менее, чем за 4 часа, достижение медикаментозного мидриаза (5-6 мм). Премедикация включала пероральное введение 20 мкг/кг атропина, эпибульбарную анестезию (3-х кратные инстилляции 0,4% р-ра инокаина) [13].
У 167 детей проводилась индукция ингаляцией галотана с предварительной оксигенацией. Поддержание необходимой глубины анестезии обеспечивалось галотаном 0,5 об% через лицевую маску. В 117 случаях использовался севофлуран 1,5-2,5 об% в 100% кислороде при скорости потока свежего газа 2 л/мин. Применялась лицевая маска с дыхательным контуром Мейплсона на самостоятельном дыхании в положении лежа на боку. Севоран сертифицирован и разрешен к применению у детей в РФ с 2008 года [14].
ЛКС осуществлялась при положении младенца на боку с использованием контактной оптической линзы, после эпибульбарной анестезии 0,4% р-ром инокаина. При выполнении ЛКС офтальмохирургами использовался диодный лазер (544 нм). Коагуляции подвергались ишемические зоны периферии сетчатки. Продолжительность операций и анестезии составляли от 30 до 60 мин.
В течение всей операции осуществлялся интраоперационный мониторинг с помощью пульсоксиметрии и капнографии. По завершении операции прекращали подачу анестетика, пациентов переводили на дыхание кислородом через лицевую маску с FiO2 0,3 до полной элиминации анестетика.
Проводилось изучение особенностей действия севорана и галотана. Оценивались эффективность и безопасность анестезии соответственно объему оперативного вмешательства.
Результаты и обсуждение
Первоначально, при выполнении первых анестезий недоношенным детям с РН мы использовали анестетик галотан. С его применением проведено 167 общих анестезий. В 99 случаях удалось достичь достаточной глубины наркоза (59%). Но у 68 детей произошли различные негативные реакции на данный препарат (41%). Они включали: депрессию самостоятельного дыхания (40 детей), отсроченное апноэ в послеоперационном периоде (6 детей), брадикардию (22 детей). Эти реакции были связаны с побочным воздействием препарата на дыхательный центр продолговатого мозга, что сопровождается угнетением дыхания. Кроме того, галотан способен вызывать замедление проводимости в синоатриальном узле и появление АВ-узлового ритма или брадикардии.
Все негативные реакции были немедленно благополучно устранены путем моментального снижения концентрации анестетика в дыхательной смеси и применения вспомогательной вентиляции легких.
Во всех случаях имело место плавное пробуждение. В послеоперационном периоде, учитывая высокую частоту негативных реакций, дети наблюдались в течение более длительного периода (до двух часов).
В связи с высокой частотой негативных реакций у недоношенных детей, впоследствии мы отказались от применения галотана и перешли на использование более современного и безопасного препарата – севофлурана.
С использованием севофлурана и лицевой маски с дыхательным контуром Мейплсона было выполнено 117 общих анестезий. В 101 случае удалось достигнуть оптимальной глубины наркоза. Анестезия протекала без осложнений, как в интра-, так и в послеоперационном периоде. Негативные реакции произошли у 16 детей (13,6%). В большинстве случаев реакции проявлялись кратковременным угнетением дыхания. Во всех случаях они были быстро купированы проведением вспомогательной вентиляции легких. Пробуждение у всех детей было плавное, а послеоперационный период протекал без осложнений.
Таким образом, при выполнении анестезии подавляющему большинству младенцев удалось добиться достаточной глубины наркоза, обеспечить полный объем необходимой ЛКС. Негативные реакции гораздо чаще встречались при использовании галотана (41%), при его замене на севоран их частота снизилась до 13,6%.
Выводы
1. Применение лицевой маски и севофлурана при выполнении ЛКС обеспечило оптимальную глубину и продолжительность анестезии у 85% младенцев, при использовании галотана – в 59% случаев.
2. Возникшие интра- и постоперационные осложнения общей анестезии включали: депрессию самостоятельного дыхания; депрессию сердечной деятельности.
3. По нашему опыту, при общей ингаляционной анестезии у недоношенных детей младенческого возраста оптимальным анестетиком является севофлуран, частота его побочных эффектов и степень их выраженности крайне незначительны.
Источник