Центральная хориоретинальная дистрофия сетчатки глаза
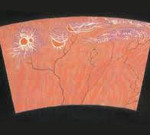
Хориоретинальная дистрофия – это инволюционные дистрофические изменения, затрагивающие преимущественно хориокапиллярный слой сосудистой оболочки глаза, пигментный слой сетчатки и расположенную между ними стекловидную пластинку (мембрану Бруха). К симптомам хориоретинальной дистрофии относятся искажение прямых линий, появление в поле зрения слепых пятен, вспышек света, утрата четкости зрения, способности к письму и чтению. Диагноз хориоретинальной дистрофии подтверждают данные офтальмоскопии, проверки остроты зрения, теста Амслера, кампиметрии, лазерной сканирующей томографии, периметрии, электроретинографии, флуоресцентной ангиографии сосудов сетчатки. При хориоретинальной дистрофии проводят медикаментозную, лазерную, фотодинамическую терапию, электро- и магнитостимуляцию, а также витрэктомию, реваскуляризацию и вазореконструкцию области сетчатки.
Общие сведения
В клинической офтальмологии хориоретинальная дистрофия (возрастная макулярная дегенерация) относится к сосудистой патологии глаза и характеризуется постепенными необратимыми изменениями макулярной области сетчатки со значительной потерей центрального зрения обоих глаз у пациентов старше 50 лет. Даже в тяжелых случаях хориоретинальная дистрофия не вызывает полную слепоту, так как периферическое зрение остается в пределах нормы, но полностью утрачивается способность к выполнению четкой зрительной работы (чтению, письму, управлению транспортом).
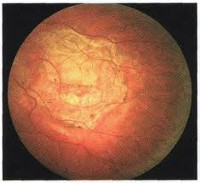
Хориоретинальная дистрофия
Причины
Хориоретинальная дистрофия является многофакторной патологией, механизмы возникновения и развития которой до конца не ясны. Хориоретинальная дистрофия может развиваться как врожденное заболевание с аутосомно-доминантным типом наследования или быть следствием инфекционно-воспалительных, токсических и травматических поражений глаза.
В основе развития хориоретинальной дистрофии могут лежать первичные инволюционные изменения макулярной области сетчатки и мембраны Бруха, атеросклероз и нарушение микроциркуляции в хориокапиллярном слое сосудистой оболочки, повреждающее действие ультрафиолетового излучения и свободных радикалов на пигментный эпителий, нарушение обменных процессов.
В зону риска по хориоретинальной дистрофии попадают лица:
- старше 50 лет, преимущественно женского пола, со светлой пигментацией радужной оболочки глаза;
- с иммунной и эндокринной патологией, артериальной гипертензией;
- злоупотребляющие курением;
- перенесшие хирургическое лечение катаракты.
Классификация
По патогенезу различают следующие формы возрастной хориоретинальной дистрофии: сухую атрофическую (неэкссудативную) и влажную (экссудативную).
- Сухая хориоретинальная дистрофия. Ранняя форма заболевания, встречается в 85-90% случаев, сопровождается атрофией пигментного эпителия и постепенным снижением зрения, причем поражение второго глаза развивается не позднее 5-ти лет после заболевания первого.
- Влажная хориоретинальная дистрофия. В 10% случаев сухая хориоретинальная дистрофия переходит в более тяжелую и быстротекущую экссудативную форму, осложняющуюся отслойкой пигментного и нейроэпителия сетчатки, геморрагиями и рубцовой деформацией.
Симптомы хориоретинальной дистрофии
Сухая форма
Клиническое течение хориоретинальной дистрофии хроническое, медленно прогрессирующее. В начальном периоде неэкссудативной формы хориоретинальной дистрофии жалобы отсутствуют, острота зрения долго остается в пределах нормы. В некоторых случаях может возникнуть искажение прямых линий, формы и размера предметов (метаморфопсия).
Сухая хориоретинальная дистрофия характеризуется скоплениями коллоидного вещества (ретинальными друзами) между мембраной Буха и пигментным эпителием сетчатки, перераспределением пигмента, развитием дефектов и атрофии пигментного эпителия и хориокапиллярного слоя. Вследствие этих изменений в поле зрения появляется ограниченный участок, где зрение сильно ослаблено или полностью отсутствует (центральная скотома). Пациенты с сухой формой хориоретинальной дистрофии могут предъявлять жалобы на двоение предметов, снижение четкости зрения вблизи, наличие слепых пятен в поле зрения.
Влажная форма
В развитии экссудативной формы хориоретинальной дистрофии выделяют несколько стадий.
- На стадии экссудативной отслойки пигментного эпителия могут наблюдаться достаточно высокая острота центрального зрения (0,8-1,0), появление временных невыраженных нарушений рефракции: дальнозоркости или астигматизма, признаков метаморфопсии, относительно положительной скотомы (полупрозрачного пятна в поле зрения глаза), фотопсии. Выявляется небольшая приподнятость сетчатки в виде купола в макулярной области (зона отслойки), имеющая четкие границы, друзы становятся менее различимыми. На этой стадии процесс может стабилизироваться, возможно самостоятельное прилегание отслойки.
- На стадии экссудативной отслойки нейроэпителия жалобы, в основном, остаются прежними, острота зрения снижается в большей степени, отмечается нечеткость границ отслойки и отечность приподнятой зоны сетчатки.
- Для стадии неоваскуляризации характерно резкое снижение остроты зрения (до 0,1 и ниже) с утратой способности к письму и чтению. Экссудативно-геморрагическая отслойка пигментного и нейроэпителия проявляется образованием большого бело-розового или серо-коричневого четко отграниченного очага со скоплениями пигмента, новообразованными сосудами, кистовидно измененной сетчаткой, выступающей в стекловидное тело. При разрыве новообразованных сосудов отмечаются субпигментные или субретинальные кровоизлияния, в редких случаях – развитие гемофтальма. Зрение держится на низком уровне.
- Рубцовая стадия хориоретинальной дистрофии протекает с образованием фиброзной ткани и формированием рубца.
Диагностика
В диагностике хориоретинальной дистрофии имеет значение наличие характерных проявлений заболевания (различных видов метаморфопсий, положительной скотомы, фотопсии). Проводится комплексное офтальмологическое обследование:
- Первичная диагностика: проверка остроты зрения, офтальмоскопия, тест Амслера на искажение зрения, кампиметрия (исследования центрального поля зрения).
- Основная диагностика. Наиболее информативными диагностическими методами при хориоретинальной дистрофии являются оптическая когерентная и лазерная сканирующая томография сетчатки, компьютерная периметрия, электроретинография, флуоресцентная ангиография сосудов сетчатки, позволяющие выявить самые ранние признаки поражения.
- Дополнительная диагностика. Могут применяться тесты для проверки цветоощущения, контрастности зрения, размеров центрального и периферического зрительных полей.
Необходимо проведение дифференциального диагноза хориоретинальной дистрофии с меланосаркомой хориоидеи.
Лечение хориоретинальной дистрофии
В лечении хориоретинальной дистрофии используют медикаментозные, лазерные, хирургические методы, электроокулостимуляцию и магнитостимуляцию, что позволяет стабилизировать и частично компенсировать состояние, т. к. полное восстановление нормального зрения невозможно.
Лечение сухой формы
Медикаментозная терапия при неэкссудативной форме хориоретинальной дистрофии включает в себя внутривенное, парабульбарное введение дезагрегантов и антикоагулянтов прямого и непрямого действия, ангиопротекторов, сосудорасширяющих препаратов, антиоксидантов, гормонов, ферментов, витаминов. Выполняется лазерстимуляция сетчатки низкоинтенсивным излучением полупроводникового лазера расфокусированным красным пятном.
Лечение влажной формы
При экссудативной форме хориоретинальной дистрофии показана местная и общая дегидратационная терапия и секторальная лазерная коагуляция сетчатки с целью разрушения субретинальной неоваскулярной мембраны, ликвидации отека макулярной области, что позволяет предупредить дальнейшее распространение дистрофического процесса. Перспективными методиками лечения экссудативной хориоретинальной дистрофии также являются фотодинамическая терапия, транспупиллярная термотерапия сетчатки.
Хирургическое лечение
Хирургическим лечением хориоретинальной дистрофии является витрэктомия (при неэкссудативной форме с целью удаления субретинальных неоваскулярных мембран), реваскуляризация хориоидеи и вазореконструктивные операции (при неэкссудативной форме для улучшения кровоснабжения сетчатки). Показатель остроты зрения, благоприятный для лечения составляет от 0,2 и выше.
Прогноз и профилактика
Прогноз в отношении зрения при хориоретинальной дистрофии в целом неблагоприятный. Профилактика заключается в минимизации факторов риска, своевременном лечении офтальмологических заболеваний.
Источник
Содержание:
- Что такое хориоретинальная дистрофия?
- Причины хориоретинальной дистрофии
- Симптомы хориоретинальной дистрофии
- Диагностика хориоретинальной дистрофии
- Лечение хориоретинальной дистрофии
Что такое хориоретинальная дистрофия?
Хориоретинальная дистрофия (ЦХРД) – это дистрофия центральной части сетчатки глаза. Синонимы: центральная дисциформная дистрофия, сенильная макулодистрофия. Это возрастная патология, которая встречается в возрасте 50-60 лет и чаще наблюдается у женщин.
При возрастной дегенерации сетчатки происходят постепенные необратимые изменения в макулярной (центральной) зоне сетчатки, последствием которых является значительная потеря центрального зрения. Ткань сетчатки замещается фиброзной тканью с формированием рубцов. Обычно этот процесс развивается параллельно на обоих глазах, но в некоторых случаях может происходить с опережением на одном глазу.
Даже в тяжелых случаях ЦХРД не приводит к полной слепоте, поскольку периферическое зрение сохраняется в пределах нормы. Однако при этом полностью теряется способность к выполнению работ, требующих четкого зрения (чтение, письмо, управление транспортными средствами и т. д.).
Частота заболевания увеличивается с возрастом: в возрасте 51–64 лет она составляет 1,6% от общей численности населения, в возрасте 65–74 лет – 11%, старше 75 лет – 28%.
Заболевание имеет хроническое, медленно прогрессирующее течение. Следует дифференцировать его от отслойки сетчатки – это разные патологии.
Причины хориоретинальной дистрофии
Причины и этиология ЦХРД полностью не выяснены.
Перечень факторов, повышающих вероятность её развития, включает:
Наследственную предрасположенность;
Ослабление иммунной системы;
Нарушения кровообращения в сосудистой системе глаз;
Эндокринные патологии (сахарный диабет);
Миопию (близорукость) средней и высокой степени;
Проблемы с сердечно-сосудистой системой (гипертоническая болезнь, атеросклероз);
Избыточное воздействие на глаза ультрафиолетового излучения;
Инфекционные, токсические или травматические поражения глаз;
Нерациональное питание;
Наличие вредных привычек.
Хориоретинальная дистрофия развивается под влиянием совокупности факторов. Она может быть, как врожденным заболеванием с аутосомно-доминантным типом передачи, так и последствием инфекционно-воспалительного процесса.
К дополнительным факторам риска относят:
Женский пол;
Светлую пигментацию кожи и радужной оболочки глаз;
Злоупотребление курением;
Оперативное лечение катаракты в анамнезе.
Симптомы хориоретинальной дистрофии
Различают две формы ЦХРД: неэкссудативную (сухую, атрофическую) и экссудативную (влажную).
Сухая неэкссудативная дистрофия представляет собой раннюю форму заболевания и встречается в 85-90% случаев. Характеризуется нарушениями обмена веществ между сосудами и сетчаткой глаза. Между базальным слоем, образованным сосудистой и сетчатой оболочками, и пигментным эпителием сетчатки накапливаются коллоидные вещества (продукты распада), происходит перераспределение пигмента и атрофия пигментного эпителия.
Болезнь начинается бессимптомно и прогрессирует медленно. Острота зрения долгое время остается нормальной, но может отмечаться искривление прямых линий, раздвоенность, искажение форм и размеров предметов. Постепенно появляется расплывчатость изображения при взгляде прямо (как через слой воды), острота зрения начинает снижаться. Этот процесс может стабилизироваться на каком-то этапе, но может и привести к полной потере центрального зрения.
На втором глазу заболевание начинает развиваться не позже, чем через пять лет после поражения первого. В 10% случаев сухая дистрофия переходит в более тяжелую влажную форму. При этом происходит проникновение жидкости (крови) через стенки новообразованных сосудов и её скопление под сетчаткой.
Экссудативная дистрофия имеет четыре стадии развития:
Отслойка пигментного эпителия. Острота зрения сохраняется, возможны слабые проявления дальнозоркости или астигматизма, появление тумана или мутных пятен перед глазами. Процесс может иметь обратное развитие (прилегание мест отслойки).
Отслойка нейроэпителия. К вышеуказанным симптомам добавляется значительное снижение зрения, вплоть до утраты возможности читать и писать. Отмечаются нечеткость границ и отек зоны отслойки, патологическое разрастание сосудов.
Геморрагическая отслойка пигментного и нейроэпителия. Зрение остается низким. Образуется большой розово-коричневый очаг скопления пигмента с четкими границами. Кистовидно измененная сетчатка выступает в стекловидное тело. При разрывах новообразованных сосудов происходят кровоизлияния.
Рубцовая стадия. На месте поражения образуется фиброзная ткань и формируется рубец.
Диагностика хориоретинальной дистрофии
Диагноз устанавливается на основе опроса пациента, проверки остроты зрения, офтальмоскопии, проведении кампиметрии и теста Амслера (исследований центрального зрительного поля).
Из инструментальных методов диагностики применяются:
Компьютерная периметрия;
Лазерная сканирующая томография сетчатки;
Электроретинография;
Флуоресцентная ангиография глазного дна.
Лечение хориоретинальной дистрофии
Выбор тактики лечения зависит от формы и стадии процесса. Основная цель – его стабилизация и компенсация. Методы лечения: медикаментозный, лазерный, хирургический.
При неэкссудативной форме назначаются внутривенные инъекции дезагрегантов, антикоагулянтов и ангиопротекторов, сосудорасширяющие препараты («Кавинтон»), антиоксиданты («Эмоксипин»), витаминотерапия. Лечение должно быть непрерывным и проходить курсами 2 раза в год (осенью и весной).
При экссудативной форме проводится общее и местное лечение, возможна лазерная коагуляция (прижигание) сетчатки с целью ликвидации отека и разрушения неоваскулярной (образованной из патологических сосудов) мембраны. Это позволяет приостановить дальнейшее развитие дистрофического процесса.
Оперативное лечение применяется для улучшения кровоснабжения задней части глаза. Это может быть витрэктомия (удаление части стекловидного тела), вазореконструкция, реваскуляризация (восстановление нормальной сети микрососудов).
Прогноз в целом неблагоприятный, так как восстановить зрение невозможно. Но даже при полной потере центрального зрения остается периферическое, достаточное для самообслуживания в быту и ориентирования в пространстве.
Автор статьи: Дегтярева Марина Витальевна, врач-офтальмолог, окулист
Источник
 Центральные хориоретинальные дистрофии — необратимые дегенеративные изменения в хориокапиллярном слое сосудистой оболочки глаза, затрагивающие пигментный слой сетчатки и мембрану Бруха. Это заболевание также называют возрастной макулярной дегенерацией, что указывает на то, что этот тип дистрофии сетчатки, как правило, характерен для пожилых людей и поражает центральное зрение.
Центральные хориоретинальные дистрофии — необратимые дегенеративные изменения в хориокапиллярном слое сосудистой оболочки глаза, затрагивающие пигментный слой сетчатки и мембрану Бруха. Это заболевание также называют возрастной макулярной дегенерацией, что указывает на то, что этот тип дистрофии сетчатки, как правило, характерен для пожилых людей и поражает центральное зрение.
- При неэкссудативной форме назначают дезагреганты и сосудорасширяющие препараты, показана стимуляция сетчатки низкоэнергетическим лазерным излучением.
- При экссудативной форме применяется дегидратационная терапия (местная и общая) и лазерная коагуляция сетчатки в центральной зоне. При неоваскуляризации делают прямую лазерную коагуляцию субретинальной неоваскулярной мембраны.
Хирургические методы лечения направлены в основном на улучшение кровоснабжения заднего полюса глаза и включают различные виды реваскуляризирующих и вазореконструктивных операций.
Неэкссудативная форма
Активный этап лечения центральной хориоретинальной дистрофии направлен на улучшение микроциркуляции, повышение антиоксидантной активности, устойчивости к ишемии и повреждающему действию света. Активное лечение инволюционной неэкссудативной центральной хориоретинальной дистрофии с последующей поддерживающей терапией необходимо проводить не менее 2 раз в год.
Для улучшения кровоснабжения заднего сегмента глаза проводят реваскуляризирующие и вазореконструктивные хирургические вмешательства, показанием к которым могут служить быстро прогрессирующее течение заболевания и отсутствие эффекта от проводимой консервативной терапии. В последние годы проводится лазерная коагуляция друз сетчатки.
Среди других методов лечения определенный интерес представляет транссклеральная диод-лазерная циклокоагуляция (на плоскую часть стекловидного тела наносят 8-10 лазерных аппликаций при мощности 1-2 Вт в экспозиции 3 с) или фокальная лазерная коагуляции сетчатки (наносят 30-40 коагулятов), на ее периферии или в зонах, лишенных светочувствительных элементов. Данные методы лечения можно сочетать с общепринятой консервативной терапией, так как они также способствуют улучшению обменных процессов в сетчатке.
Противопоказанием к использованию данных методов лечения служат воспалительные заболевания органа зрения. Введение раствора полипептидов сетчатки глаз скота (5 мг) в субтеноново пространство на фоне общепринятой терапии проводят однократно с периодичностью 1 р/ 6 мес.
Лекарственные средства выбора:
Пентоксифиллин парабульбарно 0,5 мл 1 р/сут, 10 сут +
- Пентоксифиллин в/в капельно 5-10 мл в 200 мл натрия хлорида изотонического р-ра 1 р/сут 7 сут или декстрана со средней молекулярной массой 30 000-40 000 1 р/ 2 сут всего 4-5 введений (под контролем АД) +
- Поливитамины группы В в/м 2 мл 1 р/сут, 10 сут или 2-3 р/нед 2 нед.
Альтернативные лекарственные средства:
Метилэтилпиридинол, 1% р-р, парабульбарно 0,5 мл 1 р/сут 10-15 сут +
- Трифосаденин, 1% р-р, в/м 2 мл 1 р/сут, 10-20 сут +
- Пиридоксин, 5% р-р, в/м 1 мл 1 р/2 сут, 10 введений +
- Тиамина, 2,5% р-р, в/м 1 мл 1 р/2 сут 10 введений (чередовать с пиридоксином) или
Пентоксифиллин парабульбарно 0,5 мл 1 р/сут, 10 сут +
- Трифосаденин, 1% р-р, в/м 2 мл 1 р/сут, 10-20 сут +
- Пиридоксин, 5% р-р, в/м 1 мл 1 р/2 сут, 10 введений +
- Тиамина хлорид, 2,5% р-р, в/м 1 мл 1 р/2 сут, 10 введений (чередовать с пиридоксином) +
- Лазерная стимуляция сетчатки (гелий-неоновый лазер с длиной волны 0,63 мкм и выходной мощностью 1,6 мВт), монокулярные сеансы с экспозицией 2 мин 1 р/сут, 10 сеансов или Ретиналамин парабульбарно (в разведении на 0,5-1 мл прокаином0,5% р-ром) 5 мг 1 р/сут, 10 сут или
Натрия хлорида изотонический раствор озонированный парабульбарно 0,5 мл 1 р/сут, 10 сут +
- Натрия хлорида изотонический р-р озонированный (концентрация озона 4-6 мг/л) в/в капельно 200 мл 1 р/сут или 1 р/ 2 сут, всего 6 введений.
Предложенные схемы активного лечения неэкссудативной центральной хориоретинальной дистрофии условны, возможна комбинация препаратов и методов лечения, используемых в различных схемах, а при необходимости их последовательное назначение. По окончании активной терапии целесообразно перейти ко второму этапу — поддерживающему лечению, длительность которого составляет не менее 1-2 мес; при этом нецелесообразно одновременное использование лекарственные средства, оказывающих сходное действие.
Лекарственные средства выбора:
- Поливитамины внутрь 1 табл 2-3 р/сут, 20-30 сут +
- Пентоксифиллин внутрь 100 мг 3 р/сут, 1-2 мес +
- Винпоцетин внутрь 5 мг 3 р/сут 2 мес +
- Никотиновая кислота внутрь 50 мг 2-3 р/сут, 1 мес +
- Никотиноил гамма-аминомасляная кислота внутрь 20 мг 3 р/сут, 2 мес +
- Гинкго билоба экстракт внутрь 40 мг 3 р/сут, 2 мес +
- Триметазидин внутрь 20 мг 3 р/сут 2 мес +
- лекарственные средства, стимулирующее синтез родопсина внутрь 1 капсулу 3 р/сут, 1 мес +
- лекарственные средства, содержащее экстракт водоросли Spirulina platensis, внутрь 2 табл 3 р/сут, 1 мес +
- Экстракт черники внутрь 1 табл 2 р/сут, 2-3 нед.
Экссудативная форма
Целью лечения центральной хориоретинальной дистрофии служат замедление прогрессирования процесса и сохранение или повышение остроты зрения за счет уменьшения выраженности либо исчезновения отслойки пигментного эпителия, уменьшения выраженности отслойки нейроэпителия, предотвращения кровоизлияний, полной или частичной резорбции отека сетчатки, геморрагий и экссудата, а также запустевания сосудов субретинальной неоваскулярной мембраны.
Показаниями к проведению лазерной коагуляции служат длительное сохранение экссудативной отслойки пигментного и/или нейроэпителия, прогресс экссудативной или экссудативно-геморрагической стадии ЦХРД с увеличением выраженности субретинальной неоваскуляризации, отсутствие эффекта от консервативной терапии. При лазерной коагуляции предпочтение следует отдавать лазерам с длиной волны, соответствующей красной, желтой или зеленой части спектра.
Фотодинамическая терапия показана при субретинальной неоваскуляризации в отсутствие эффекта от консервативной терапии и прогрессировании процесса.
Хирургическое удаление субретинальной неоваскулярной мембраны показано при увеличивающихся ее размерах и неэффективности консервативной терапии.
Из других методов лечения следует упомянуть интравитреальное введение триамцинолона в дозе 2-4 мг, показанием к которому служит длительное сохранение отека сетчатки.
Лекарственные средства выбора:
- Дексаметазон парабульбарно 2 мг 1 р/сут, 10-12 сут ±
- Метилэтилпиридинол, 1% р-р, парабульбарно 0,5 мл 1 р/сут, 10-12 сут +
- Декстран, средняя молекулярная масса 30 000-40 000 в/в капельно 200 мл или
Повидон / натрия хлорид / калия хлорид / кальция хлорид / магния хлорид / натрия гидрокарбонат в/в капельно 200-400 мл 1 р/сут, 5-7 введений +
- Фуросемид в/в капельно 1-2 мл 1 р/сут, 5-7 введений +
- Трифосаденин, 1% р-р, в/м 2 мл 1 р/сут, 10-20 сут +
- Пиридоксин, 5% р-р, в/м 1 мл 1 р/ 2 сут, 10 введений +
- Тиамин, 2,5% р-р, в/м 1 мл 1 р/2 сут 10 введений (чередовать с пиридоксином) +
- Ацетазоламид внутрь 250 мг 1 р/2 сут, 7-14 сут или (при наличии выраженных кровоизлияний)
- Дексаметазон 2 мг/гепарин натрий 750 ЕД/ декстран, средняя молекулярная масса 30 000-40 000 0,2 мл парабульбарно 1 р/сут 10-12 сут или
Дексаметазон 2 мг/ этамзилат, 12,5% р-р, 0,5 мл парабульбарно 1 р/сут 7-10 сут +
- Повидон / натрия хлорид / калия хлорид / кальция хлорид / магния хлорид / натрия гидрокарбонат в/в капельно 200-400 мл 1 р/сут, 5-7 введений +
- Фуросемид в/в капельно 1-2 мл 1 р/сут, 5-7 введений +
- Этамзилат, 12,5% р-р, в/м 2 мл 2 р/сут, 7-10 сут +
- Аскорбиновая кислота / рутозид внутрь 1 табл 4 р/сут, 10-20 сут или
Аминокапроновая кислота парабульбарно 0,5 мл (25 мг) 1 р/сут, 5-7 сут.
Затем:
Дексаметазон 2 мг / гепарин натрий 750 ЕД/ декстран, средняя молекулярная масса 30 000-40 000 0,2 мл парабульбарно 1 р/сут 10-12 сут или
Дексаметазон 2 мг/ этамзилат, 12,5% р-р, 0,5 мл парабульбарно 1 р/сут 7-10 сут +
- Этамзилат, 12,5% р-р, в/м 2 мл 2 р/сут, 7-10 сут +
- Аскорбиновая кислота/рутозид внутрь 1 табл 4 р/сут, 10-20 сут или
Плазминоген парабульбарно 0,5 мл (1000-2000 ЕД) 1 р/сут, 10-15 сут или
Проурокиназа парабульбарно 0,5 мл (5000 ЕД) 1 р/сут, 10-15 сут +
- Повидон / натрия хлорид / калия хлорид / кальция хлорид / магния хлорид / натрия гидрокарбонат в/в капельно 200-400 мл 1 р/ 2 сут 4-7 введений +
- Дексаметазон в/в капельно 4-8 мг 1 р/2 сут, 4-7 введений +
- Фуросемид в/в капельно 1-2 мл 1 р/2 сут, 4-7 введений.
Вместо дексаметазона можно использовать бетаметазон или триамцинолон:
- Бетаметазон (динатрия фосфат/дипропионат) парабульбарно 0,5 мл 1 р/ 7-10 сут, 2-3 введения или
- Триамцинолон парабульбарно 20 мг 1 р/ 5-7 сут, 2-3 введения или
Аутоплазма активированная парабульбарно 0,5 мл 1 р/сут, 10-15 сут +
- Аутоплазма активированная в/м 2-3 мл 1 р/сут, 10-15 сут или (фотодинамическая терапия)
- Вертепорфин, р-р, в/в 6 мг/м2 поверхности тела (30 мл за 10 мин) через 15 мин низкоинтенсивное лазерное облучение сетчатки (диодный лазер с длиной волны 689 плотность облучения 600 мВ/см2) в течение 83 с;
Обследование в динамике с интервалом 3 мес, при наличии подтекания контрастного вещества из очага повторное проведение вмешательства в аналогичном режиме. После окончания активной терапии целесообразно проведение поддерживающего лечения:
- Ретиналамин парабульбарно (в разведении на 0,5-1 мл 0,5% р-ра прокаина) 5 мг 1 р/сут, 10 сут или
- Актовегин в/м 2 мл 1 р/сут, 10-15 сут или
- Солкосерил в/м 2-5 мл 1 р/сут, 10-20 сут или внутрь 200 мг 3 р/сут, 20-30 сут ±
- Триметазидин внутрь 20 мг 3 р/сут 1-2 мес +
- Витамин Е внутрь 100-200 мг 1-2 р/сут, 1 мес +
- лекарственные средства, стимулирующее синтез родопсина внутрь 1 капсула 3 р/сут, 1 мес +
- лекарственные средства, содержащее экстракт водоросли Spirulina platensis, внутрь 2 табл 3 р/сут, 1 мес.
Репаративная стадия
Применяют те же лекарственные средства, что и в экссудативно-геморрагической стадии. Выбор конкретного препарата определяется преобладанием тех или иных клинических симптомов. Проведение лазерной коагуляции нецелесообразно. В заключение необходимо отметить что наибольшие трудности представляет медикаментозное лечение больных, у которых на одном глазу имеется неэкссудативная, а на другом – экссудативная форма инволюционной ЦХРД.
За последние 2 года произошли революционные изменения в лечении возрастной макулодистрофии — начали использоваться новые препараты, ингибирующие выработку фактора роста эндотелия сосудов (VEGF). Не смотря на то, что причины появления субретинальной неоваскулярной мембраны при возрастной макулярной дегенерации еще до конца не выяснены, результаты последних исследований показывают на важную роль VEGF в развитии мембраны. Фармакологическое уничтожение VEGF может стать новым перспективным направлением в терапии таких заболеваний.
Макуджен (пегаптаниб) стал одним из первых препаратов, уничтожающих VEGF, который нашел свое применение в офтальмологии. Макуджен также называют анти-VEGF аптамером. При терапии Макудженом наблюдается торможение процесса ухудшения остроты зрения у пациентов с экссудативной формой ВМД. Лечение препаратом Макуджен по своей эффективности, схоже с фотодинамической терапией. Макуджен был одобрен в 2004 году FDA для введения в полость стекловидного тела для лечения любых форм субретинальной неоваскуляризации при ВМД. Применение Макудженом более эффективно на ранних стадиях экссудативной формы ВМД.
Луцентис (ранибизумаб) — это антиген-связывающий фрагмент мышиного антитела к VEGF, произведенный с помощью генной инженерии. Молекула препарата Луцентис, являясь высокоспецифичной частью антитела к VEGF, имеет низкий молекулярный вес (48 кДа) и может легко проникать через все слои сетчатки к патологическим сосудам. Там она устраняет рецепторы VEGF новообразованных сосудов, которые входят в состав субретинальной неоваскулярной мембраны. Данный препарат стал первым средством в этой группы, применение которого не только ведет к торможению снижения центрального зрения, но и к частичному восстановлению остроты зрения (у 95% пациентов остановилось прогрессирование болезни, а у приблизительно 30% больных зрение улучшилось). В июне 2006 года Луцентис был утвержден FDA в качестве препарата для лечения хориоидальной неоваскуляризации, связанной с ВМД.
Авастин (бевацизумаб) — это полноразмерное антитело, направленное против любых разновидностей VEGF. С 2004 года препарат Авастин уже применяется в онкологии для лечения рака прямой кишки и толстого кишечника. За последние 1,5 года было опубликовано большое количество результатов лечения с использованием Авастина пациентами с экссудативной формой ВМД. Отдаленных результатов использования Авастина пока нет. Высокий процент успешного лечения при интравитреальном введении препаратов — ингибиторов VEGF говорят о появлении нового высокоэффективного метода лечения пациентов с экссудативной формой ВМД. Достойной альтернативой фотодинамической терапии становится применение Авастина и аналогичных препаратов в лечении пациентов с ВМД.
Источник


