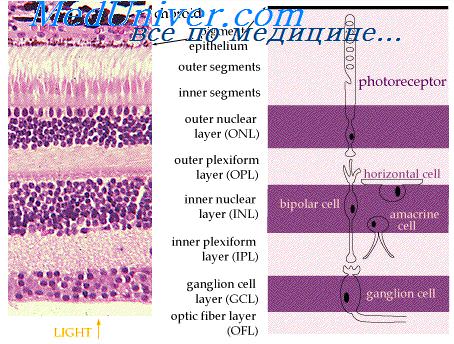
Вырастили сетчатку глаза в россии
В Федеральном научно-клиническом центре физико-химической медицины (ФНКЦ ФХМ) —подразделении Федерального медико-биологического агентства — научились выращивать сетчатку глаза из перепрограммированных клеток. Разработка позволит спасти от слепоты пациентов, теряющих зрение, например, из-за макуладистрофии. Первую трансплантацию в рамках клинических испытаний медики надеются провести уже в 2017 году. Необходимо лишь чтобы сделать это позволило законодательство.
«Перепрограммирование клеток — достаточно новое явление в науке, — рассказал Вадим Говорун, генеральный директор ФНКЦ ФХМ. — Открытие принадлежит профессору Университета Киото Синъе Яманаке».
Японский учёный обнаружил уникальную способность клеток человека той или иной ткани возвращаться в эмбриональное состояние при «выключении» определённых генов. Из таких недифференцированных (не определившихся со своими «обязанностями») стволовых клеток можно вырастить практически любую ткань. Например, из фибробластов (клеток соединительной ткани) кожи можно вырастить сетчатку глаза.
Такое преобразование позволит спасать от слепоты пациентов, теряющих зрение, например, из-за макулодистрофии — заболевания, являющегося одной из самых частых причин слепоты у людей старше 55 лет (и встречающееся у каждого второго жителя России старше 60 лет).
Исследователи Лаборатории клеточной биологии пояснили корреспондентам, что для перепрограммирования удобнее всего использовать именно кожу, потому что забор такой ткани практически не травмирует пациента. При этом клетки кожного покрова хорошо размножаются.
«Для каждого типа клеток есть специализированные стволовые клетки, то есть для восстановления клеток крови подходят только стволовые клетки крови, — рассказал Сергей Киселёв, заведующий Лабораторией биомедицинских технологий ФНКЦ ФХМ. — Универсальностью обладают лишь плюрипотентные стволовые клетки. Их можно получить или из эмбрионов, или из клеток кожи с помощью метода репрограммирования. Эти клетки пригодны для выращивания любого типа ткани».
Понятно, что из эмбриональных клеток (забираются из нежизнеспособных эмбрионов) получается только неродственный пациенту трансплантат. А это значит, что он может быть отторгнут организмом (либо человеку придётся всю оставшуюся жизнь принимать иммуносупрессивные препараты). Однако в организме человека есть ткани, на которые иммунная система «не обращает внимания». К ним относятся головной мозг и глаза. Для таких органов родственность тканей при трансплантации не очень важна. Хотя предполагается, что трансплантаты из родственных или перепрограммированных клеток будут приживаться лучше.
В США и Европе (в частности, в Великобритании) сейчас проходят клинические испытания по пересадке сетчатки глаза (операция впервые была проведена в 2014 году). В Японии они также велись, затем были временно приостановлены из-за изменений в законодательстве, но в 2017 году будут продолжены.
Применение перепрограммированных, то есть универсальных клеток, пригодных для большого количества реципиентов, упростит технологию и уменьшит стоимость операции, а значит, сделает её более массовой.
В ФНКЦ ФХМ такие технологии уже опробованы на кроликах. Однако клинические испытания пока невозможны: российские учёные ждут вступления в силу закона «О биомедицинских клеточных продуктах» (произойдёт 1 января 2017 года) и принятия по нему нормативных актов (срок пока неизвестен, потому что они не разработаны).
Как отмечают авторы материала в издании «Известия», в центре уже знают, кто станет первыми добровольцами для пересадки «искусственной» сетчатки глаза. Несколько лет назад к учёным обратилась за помощью семья с наследственной макулодистрофией. В отличие от возрастной макулодистрофии наследственная форма — это орфанное заболевание, то есть встречается крайне редко. Она обусловлена «поломкой» в генах. И если возрастная форма слепоты поддаётся некоторое время разным видам терапии, то лекарства от генетической макулодистрофи нет вообще. Между тем такие пациенты начинают слепнуть в 20–30 лет.
В семье, обратившейся в ФНКЦ ФХМ, носителями мутации являются дед по отцовской линии, отец и дети.
«Для детей этой семьи мы подготовили клетки сетчатки с отредактированным геномом, — рассказал Киселев. — Но, скорее всего, на первом этапе мы начнём испытания с неродственных клеток, потому что на это проще будет получить разрешение».
Центр физико-химической медицины планирует найти медицинских партнёров, с которыми уже в 2017 году сможет осуществить пациентам трансплантацию выращенной в лаборатории сетчатки.
Добавим, что эксперты ФНКЦ ФХМ похожим способом вырастили нейроны головного мозга и испытали их приживаемость на животных моделях. Трансплантация «исправленных» клеток вместе с процедурой редактирования генома поможет в лечении пациентов с болезнью Паркинсона. В мире такие клинические испытания также уже ведутся. В России они будут возможны при наличии интереса со стороны профильных учреждений — нейрохирургических и неврологических институтов — и тоже только после принятия закона.
Видео дня. Голосование за поправки в конституцию пройдёт 22 апреля
Источник
В Федеральном научно-клиническом центре физико-химической медицины (ФНКЦ ФХМ) —подразделении Федерального медико-биологического агентства — научились выращивать сетчатку глаза из перепрограммированных клеток. Разработка позволит спасти от слепоты пациентов, теряющих зрение, например, из-за макуладистрофии. Первую трансплантацию в рамках клинических испытаний медики надеются провести уже в 2017 году. Необходимо лишь чтобы сделать это позволило законодательство.
«Перепрограммирование клеток — достаточно новое явление в науке, — рассказал Вадим Говорун, генеральный директор ФНКЦ ФХМ. — Открытие принадлежит профессору Университета Киото Синъе Яманаке».
Японский учёный обнаружил уникальную способность клеток человека той или иной ткани возвращаться в эмбриональное состояние при «выключении» определённых генов. Из таких недифференцированных (не определившихся со своими «обязанностями») стволовых клеток можно вырастить практически любую ткань. Например, из фибробластов (клеток соединительной ткани) кожи можно вырастить сетчатку глаза.
Такое преобразование позволит спасать от слепоты пациентов, теряющих зрение, например, из-за макулодистрофии — заболевания, являющегося одной из самых частых причин слепоты у людей старше 55 лет (и встречающееся у каждого второго жителя России старше 60 лет).
Исследователи Лаборатории клеточной биологии пояснили корреспондентам, что для перепрограммирования удобнее всего использовать именно кожу, потому что забор такой ткани практически не травмирует пациента. При этом клетки кожного покрова хорошо размножаются.
«Для каждого типа клеток есть специализированные стволовые клетки, то есть для восстановления клеток крови подходят только стволовые клетки крови, — рассказал Сергей Киселёв, заведующий Лабораторией биомедицинских технологий ФНКЦ ФХМ. — Универсальностью обладают лишь плюрипотентные стволовые клетки. Их можно получить или из эмбрионов, или из клеток кожи с помощью метода репрограммирования. Эти клетки пригодны для выращивания любого типа ткани».
Понятно, что из эмбриональных клеток (забираются из нежизнеспособных эмбрионов) получается только неродственный пациенту трансплантат. А это значит, что он может быть отторгнут организмом (либо человеку придётся всю оставшуюся жизнь принимать иммуносупрессивные препараты). Однако в организме человека есть ткани, на которые иммунная система «не обращает внимания». К ним относятся головной мозг и глаза. Для таких органов родственность тканей при трансплантации не очень важна. Хотя предполагается, что трансплантаты из родственных или перепрограммированных клеток будут приживаться лучше.
В США и Европе (в частности, в Великобритании) сейчас проходят клинические испытания по пересадке сетчатки глаза (операция впервые была проведена в 2014 году). В Японии они также велись, затем были временно приостановлены из-за изменений в законодательстве, но в 2017 году будут продолжены.
Применение перепрограммированных, то есть универсальных клеток, пригодных для большого количества реципиентов, упростит технологию и уменьшит стоимость операции, а значит, сделает её более массовой.
В ФНКЦ ФХМ такие технологии уже опробованы на кроликах. Однако клинические испытания пока невозможны: российские учёные ждут вступления в силу закона «О биомедицинских клеточных продуктах» (произойдёт 1 января 2017 года) и принятия по нему нормативных актов (срок пока неизвестен, потому что они не разработаны).
Как отмечают авторы материала в издании «Известия», в центре уже знают, кто станет первыми добровольцами для пересадки «искусственной» сетчатки глаза. Несколько лет назад к учёным обратилась за помощью семья с наследственной макулодистрофией. В отличие от возрастной макулодистрофии наследственная форма — это орфанное заболевание, то есть встречается крайне редко. Она обусловлена «поломкой» в генах. И если возрастная форма слепоты поддаётся некоторое время разным видам терапии, то лекарства от генетической макулодистрофи нет вообще. Между тем такие пациенты начинают слепнуть в 20–30 лет.
В семье, обратившейся в ФНКЦ ФХМ, носителями мутации являются дед по отцовской линии, отец и дети.
«Для детей этой семьи мы подготовили клетки сетчатки с отредактированным геномом, — рассказал Киселев. — Но, скорее всего, на первом этапе мы начнём испытания с неродственных клеток, потому что на это проще будет получить разрешение».
Центр физико-химической медицины планирует найти медицинских партнёров, с которыми уже в 2017 году сможет осуществить пациентам трансплантацию выращенной в лаборатории сетчатки.
Добавим, что эксперты ФНКЦ ФХМ похожим способом вырастили нейроны головного мозга и испытали их приживаемость на животных моделях. Трансплантация «исправленных» клеток вместе с процедурой редактирования генома поможет в лечении пациентов с болезнью Паркинсона. В мире такие клинические испытания также уже ведутся. В России они будут возможны при наличии интереса со стороны профильных учреждений — нейрохирургических и неврологических институтов — и тоже только после принятия закона.
Видео дня. Голосование за поправки в конституцию пройдёт 22 апреля
Источник
В Федеральном научно-клиническом центре физико-химической медицины (ФНКЦ ФХМ) — подразделении Федерального медико-биологического агентства (ФМБА) — научились выращивать сетчатку глаза из перепрограммированных клеток. Разработка позволит лечить пациентов, теряющих зрение, например, из-за макуладистрофии.
Первую трансплантацию в рамках клинических испытаний собираются произвести в 2017 году. Следующая задача ученых ФХМ — научиться с помощью новых клеточных технологий лечить болезнь Паркинсона.
«Перепрограммирование клеток — достаточно новое явление в науке, — рассказал „Известиям“ генеральный директор ФНКЦ ФХМ Вадим Говорун.
— Открытие принадлежит профессору Университета Киото Синье Яманаке (в 2012 году ученый был удостоен за него Нобелевской премии). Яманака обнаружил уникальную способность клеток человека той или иной ткани, например фибробластов или кожного эпителия, перепрограммироваться в эмбриональное состояние. Из таких недифференцированных (плюрипотентных) стволовых клеток можно вырастить практически любую ткань.
Например, из фибробластов кожи можно вырастить сетчатку глаза. Такая операция позволит лечить, например, пациентов, теряющих зрение из-за макулодистрофии — заболевания, являющегося одной из самых частых причин слепоты у людей старше 55 лет.»
В Лаборатории клеточной биологии «Известиям» пояснили, что для перепрограммирования удобнее всего использовать именно кожу, потому что забор ткани почти не травматичен для пациента, при этом клетки хорошо размножаются.
«Для каждого типа клеток есть специализированные стволовые клетки, то есть для восстановления клеток крови подходят только стволовые клетки крови, — рассказал заведующий Лабораторией биомедицинских технологий ФНКЦ ФХМ Сергей Киселев.
— Универсальностью обладают лишь плюрипотентные стволовые клетки. Их можно получить или из эмбрионов, или из клеток кожи с помощью метода репрограммирования. Эти клетки пригодны для выращивания любого типа ткани.»
Ученый пояснил, что из эмбриональных клеток получается только аллогенный, то есть неродственный трансплантат. Однако в организме человека есть ткани, на которые иммунная система не распространяет свое влияние. К ним относятся головной мозг и глаза. Для таких органов родственность тканей при трансплантации не очень важна. Хотя предполагается, что трансплантаты из родственных или перепрограммированных клеток будут приживаться лучше.
По словам Сергея Киселева, в США и Европе (в частности, в Великобритании) сейчас проходят клинические испытания пересадки сетчатки глаза. В Японии они также велись, затем были временно приостановлены из-за изменений в законодательстве, но в 2017 году будут продолжены.
Применение перепрограммированных, то есть универсальных клеток, пригодных для большого количества реципиентов, упростит технологию и уменьшит стоимость операции.
В ФНКЦ ФХМ такие препараты уже выращены и опробованы на кроликах. Однако клинические испытания пока невозможны: ученые ждут вступления в силу закона «О биомедицинских клеточных продуктах» (1 января 2017 года) и принятия по нему нормативных актов (срок неизвестен, потому что акты пока не разработаны).
В центре уже знают, кто станет первыми пациентами для пересадки сетчатки глаза. Несколько лет назад к ученым обратилась за помощью семья с наследственной макулодистрофией.
В отличие от возрастной макулодистрофии, которой страдает примерно половина населения страны старше 60 лет, наследственная форма — это орфанное заболевание. Но если возрастная форма слепоты поддается некоторое время разным видам терапии, то лекарства от генетической макулодистрофи нет. Между тем такие пациенты начинают слепнуть в 20–30 лет.
В семье, обратившейся в ФНКЦ ФХМ, носителями мутации являются дед по отцовской линии, отец, дети.
«Для детей этой семьи мы подготовили клетки сетчатки с отредактированным геномом, — рассказал Сергей Киселев.
— Но, скорее всего, на первом этапе мы начнем испытания с неродственных клеток, потому что на это проще будет получить разрешение.»
Центр физико-химической медицины планирует найти медицинских партнеров, с которыми уже в 2017 году сможет осуществить пациентам трансплантацию выращенной в лаборатории сетчатки.
Вадим Говорун также сообщил «Известиям», что в ФНКЦ ФХМ вырастили и испробовали на животных нейроны головного мозга.
Их трансплантация вместе с процедурой редактирования генома поможет в лечении пациентов с болезнью Паркинсона. В мире такие клинические испытания уже ведутся. В России они будут возможны при наличии интереса со стороны профильных учреждений — нейрохирургических и неврологических институтов — и тоже только после принятия закона.
Источник
2016-12-01T02:58+0300
2020-03-03T01:38+0300
https://ria.ru/20161201/1482561355.html
СМИ: российские ученые научились выращивать сетчатку глаза
https://cdn21.img.ria.ru/images/138763/17/1387631799_0:100:2000:1233_1036x0_80_0_0_8bd0e38d3ed26dd434aa648e0045e687.jpg
РИА Новости
https://cdn22.img.ria.ru/i/export/ria/logo.png
РИА Новости
https://cdn22.img.ria.ru/i/export/ria/logo.png
02:58 01.12.2016 (обновлено: 01:38 03.03.2020)
11043
Отмечается, что новые технологии возможно позволят лечить болезнь Паркинсона.
МОСКВА, 1 дек — РИА Новости. Ученые Федерального научно-клинического центра физико-химической медицины (ФНКЦ ФХМ), подразделения Федерального медико-биологического агентства (ФМБА), научились выращивать сетчатку глаза из перепрограммированных клеток; разработка поможет лечить слепоту, сообщает в четверг газета «Известия».
Как отмечает издание, первую трансплантацию в рамках клинических испытаний собираются произвести в 2017 году. С помощью новых клеточных технологий ученые планируют впоследствии научиться лечить болезнь Паркинсона.
«Перепрограммирование клеток — достаточно новое явление в науке. Открытие принадлежит профессору университета Киото Синье Яманаке. Яманака обнаружил уникальную способность клеток человека той или иной ткани, например фибробластов или кожного эпителия, перепрограммироваться в эмбриональное состояние. Из таких недифференцированных (плюрипотентных) стволовых клеток можно вырастить практически любую ткань. Например, из фибробластов кожи можно вырастить сетчатку глаза. Такая операция позволит лечить, например, пациентов, теряющих зрение из-за макулодистрофии — заболевания, являющегося одной из самых частых причин слепоты у людей старше 55 лет», — приводит газета слова генерального директора ФНКЦ ФХМ Вадима Говоруна.
В Лаборатории клеточной биологии газете сообщили, что кожу для перепрограммирования использовать удобнее всего, ведь забор ткани почти не травматичен для пациента, при этом клетки хорошо размножаются.
Заведующий Лабораторией биомедицинских технологий ФНКЦ ФХМ Сергей Киселев рассказал газете, что клинические испытания пересадки сетчатки глаза проходят сегодня в США и Европе. Они велись также и в Японии, но были временно приостановлены из-за изменений в законодательстве, однако в 2017 году их планируют продолжить. Что касается России, то здесь ученые «ждут вступления в силу закона «О биомедицинских клеточных продуктах» (1 января 2017 года) и принятия по нему нормативных актов», пишет издание.
Первыми пациентами для пересадки сетчатки станут люди с наследственной макулодистрофией, отмечают «Известия». Если возрастная форма слепоты поддается некоторым видам лечения, то пациенты с генетической макулодистрофи начинают слепнуть в 20–30 лет, и лекарства от нее нет.
Говорун также заявил изданию, что в ФНКЦ ФХМ вырастили и испробовали на животных нейроны головного мозга.
«Их трансплантация вместе с процедурой редактирования генома поможет в лечении пациентов с болезнью Паркинсона. В мире такие клинические испытания уже ведутся. В России они будут возможны при наличии интереса со стороны профильных учреждений — нейрохирургических и неврологических институтов — и тоже только после принятия закона», — отмечают «Известия».
Подпишитесь на ежедневную рассылку РИА Наука
Спасибо, вам отправлено письмо со ссылкой для подтверждения подписки
Источник
Ученые ФМБА вырастили из клеток кожи человека сетчатку глаза, с помощью которой можно лечить слепоту
В Федеральном научно-клиническом центре физико-химической медицины (ФНКЦ ФХМ) —подразделении Федерального медико-биологического агентства (ФМБА) — научились выращивать сетчатку глаза из перепрограммированных клеток. Разработка позволит лечить пациентов, теряющих зрение, например, из-за макуладистрофии. Первую трансплантацию в рамках клинических испытаний собираются произвести в 2017 году. Следующая задача ученых ФХМ — научиться с помощью новых клеточных технологий лечить болезнь Паркинсона.
— Перепрограммирование клеток — достаточно новое явление в науке, — рассказал «Известиям» генеральный директор ФНКЦ ФХМ Вадим Говорун. — Открытие принадлежит профессору Университета Киото Синье Яманаке (в 2012 году ученый был удостоен за него Нобелевской премии). Яманака обнаружил уникальную способность клеток человека той или иной ткани, например фибробластов или кожного эпителия, перепрограммироваться в эмбриональное состояние. Из таких недифференцированных (плюрипотентных) стволовых клеток можно вырастить практически любую ткань. Например, из фибробластов кожи можно вырастить сетчатку глаза. Такая операция позволит лечить, например, пациентов, теряющих зрение из-за макулодистрофии — заболевания, являющегося одной из самых частых причин слепоты у людей старше 55 лет.
В Лаборатории клеточной биологии «Известиям» пояснили, что для перепрограммирования удобнее всего использовать именно кожу, потому что забор ткани почти не травматичен для пациента, при этом клетки хорошо размножаются.
— Для каждого типа клеток есть специализированные стволовые клетки, то есть для восстановления клеток крови подходят только стволовые клетки крови, — рассказалзаведующий Лабораторией биомедицинских технологий ФНКЦ ФХМ Сергей Киселев. — Универсальностью обладают лишь плюрипотентные стволовые клетки. Их можно получить или из эмбрионов, или из клеток кожи с помощью метода репрограммирования. Эти клетки пригодны для выращивания любого типа ткани.
Ученый пояснил, что из эмбриональных клеток получается только аллогенный, то есть неродственный трансплантат. Однако в организме человека есть ткани, на которые иммунная система не распространяет свое влияние. К ним относятся головной мозг и глаза. Для таких органов родственность тканей при трансплантации не очень важна. Хотя предполагается, что трансплантаты из родственных или перепрограммированных клеток будут приживаться лучше.
По словам Сергея Киселева, в США и Европе (в частности, в Великобритании) сейчас проходят клинические испытания пересадки сетчатки глаза. В Японии они также велись, затем были временно приостановлены из-за изменений в законодательстве, но в 2017 году будут продолжены.
Применение перепрограммированных, то есть универсальных клеток, пригодных для большого количества реципиентов, упростит технологию и уменьшит стоимость операции. В ФНКЦ ФХМ такие препараты уже выращены и опробованы на кроликах. Однако клинические испытания пока невозможны: ученые ждут вступления в силу закона «О биомедицинских клеточных продуктах» (1 января 2017 года) и принятия по нему нормативных актов (срок неизвестен, потому что акты пока не разработаны).
В центре уже знают, кто станет первыми пациентами для пересадки сетчатки глаза. Несколько лет назад к ученым обратилась за помощью семья с наследственной макулодистрофией. В отличие от возрастной макулодистрофии, которой страдает примерно половина населения страны старше 60 лет, наследственная форма — это орфанное заболевание. Но если возрастная форма слепоты поддается некоторое время разным видам терапии, то лекарства от генетической макулодистрофи нет. Между тем такие пациенты начинают слепнуть в 20–30 лет.
В семье, обратившейся в ФНКЦ ФХМ, носителями мутации являются дед по отцовской линии, отец, дети.
— Для детей этой семьи мы подготовили клетки сетчатки с отредактированным геномом, — рассказал Сергей Киселев. — Но, скорее всего, на первом этапе мы начнем испытания с неродственных клеток, потому что на это проще будет получить разрешение.
Центр физико-химической медицины планирует найти медицинских партнеров, с которыми уже в 2017 году сможет осуществить пациентам трансплантацию выращенной в лаборатории сетчатки.
Вадим Говорун также сообщил «Известиям», что в ФНКЦ ФХМ вырастили и испробовали на животных нейроны головного мозга. Их трансплантация вместе с процедурой редактирования генома поможет в лечении пациентов с болезнью Паркинсона. В мире такие клинические испытания уже ведутся. В России они будут возможны при наличии интереса со стороны профильных учреждений — нейрохирургических и неврологических институтов — и тоже только после принятия закона.
Источник