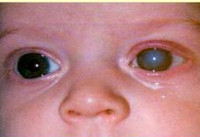
Врожденная вторичная глаукома и ее лечение
Вторичная глаукома – это заболевание, при котором повышение внутриглазного давления и поражение зрительного нерва возникает на фоне основной патологии органа зрения. Проявляется прогрессирующим снижением остроты зрения, болевым синдромом, спазмом аккомодации. Постановка диагноза основывается на результатах гониоскопии, тонометрии, тонографии, визометрии, офтальмоскопии, биомикроскопии и периметрии. Терапевтическая тактика определяется этиологией заболевания и может включать гипотензивную терапию, хирургическое вмешательство, лазерную коагуляцию сетчатой оболочки.
Общие сведения
Вторичная глаукома – одно из наиболее опасных заболеваний в офтальмологии. В структуре всех глазных патологий данная форма глаукомы занимает от 0,8 до 22%. В среднем у одного-двух больных из ста она становится причиной госпитализации. Болезнь относится к числу инвалидизирующих, т. к. в 28% приводит к необратимой потере зрительных функций. В 20-45% длительное повышение ВГД ведет к тяжелому поражению зрительного нерва и требует осуществления энуклеации глазного яблока. В половине случаев диагностируют увеальную форму заболевания. У лиц мужского и женского пола встречается с одинаковой частотой. Географических особенностей эпидемиологии не наблюдается.

Вторичная глаукома
Причины вторичной глаукомы
Повышение ВГД при данной форме глаукомы связано с рядом патогенентически разнородных факторов. Доказано, что патология является полиэтиологичной. Основные причины развития включают:
- Воспалительные процессы. Наиболее распространенные причины болезни – рецидивирующий эписклерит, склерит и увеит. При данных патологических процессах поражается дренажная система глаза, что влечет за собой повышение ВГД.
- Хронический кератит. Повышение ВГД напрямую связано как с воспалением роговой оболочки, так и с вторичным формированием бельма, передних синехий и тяжелыми дегенеративно-дистрофическими изменениями роговицы. Помимо органических предпосылок к развитию вторичной глаукомы, постоянное раздражение оболочки ведет к рефлекторному гипертонусу.
- Эктопия хрусталика. Клинические проявления развиваются при вывихе хрусталика в ПКГ или стекловидное тело, что обусловлено нарушением внутриглазной гидродинамики.
- Катаракта. Глаукоматозные изменения характерны только для незрелой возрастной, травматической или старческой перезрелой формы катаракты. ВГД при этом возрастает из-за сопутствующего хрусталикового блока и сужения передней камеры.
- Тромбоз центральной вены сетчатки. Из-за того, что тромбоз ЦВТ приводит к ишемии, возникает неоваскуляризация радужки, которая в дальнейшем распространяется на область передней камеры.
- Травматические повреждения. Причиной выступает контузия глаза или рана, при которой наблюдается врастание эпителия по ходу зрительного канала. При ожоговой природе патологии повышение ВГД — следствие гиперпродукции водянистой влаги.
- Дегенеративные изменения. Триггером выступают дистрофические изменения в зоне УПК, при которых затрудняется отток внутриглазной жидкости.
- Патологические новообразования внутриглазной локализации. ВГД повышается из-за наличия объемного образования в полости глазного яблока. Из злокачественных патологий наиболее распространенны ретинобластома и меланома глаза.
Патогенез
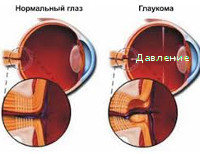
В основе развития вторичной глаукомы лежит нарушение гидродинамики внутриглазной жидкости, в частности, ее оттока. К этому приводит механическое блокирование угла передней камеры (УПК), вызванное отеком трабекулярной сети. В 20% случаев ключевая роль в механизме развития отводится патологической гиперсекреции, что ведет к накоплению большого объема экссудата. Повышение проницаемости стенки сосудов венозного русла и спазм артериол дополнительно стимулируют развитие глазной гипертензии как одного из проявлений болезни. При эктопии хрусталика возникает компрессия роговой оболочки к УПК и трабекуле. При вторичном повреждении стекловидного тела, помимо возникновения зрачкового блока, возможна его обтурация массами межтрабекулярных щелей.
При длительном течении заболевания в области дренажной системы глаза на смену функциональным изменениям приходит формирование органических преград на пути оттока. Прогрессирующее образование гониосинехий, организация экссудата в зоне трабекул и усиление ангиогенеза ведет к нарастанию клинических проявлений зрительной дисфункции. При неопластическом происхождении патологии степень нарастания клинических проявлений определяется скоростью роста новообразования в полости орбиты. При кровотечении в полость стекловидного тела или переднюю камеру повышение ВГД коррелирует с объемом кровоизлияния. Давление снижается по мере рассасывания крови, однако из-за организации сгустков и обтурации трабекулярной сети может быстро нарастать после периода мнимого благополучия.
Классификация
Заболевание имеет исключительно приобретенное происхождение. С клинической точки зрения выделяют одно- и двухстороннюю форму. По этиологии вторичную глаукому классифицируют на:
- Увеальную поствоспалительную. Возникает из-за продолжительного течения воспалительных процессов или наличия поствоспалительных изменений.
- Факогенную. Развивается из-за травматических повреждений хрусталика или является осложнением катаракты.
- Сосудистую. Этиология этой формы напрямую связана с тромбозом или стойким повышением давления в эписклеральных венах глазного яблока.
- Травматическую. В основе формирования глаукомы лежат повреждения органа зрения, вызванные действием термических, химических или ионизирующих факторов.
- Дегенеративную. Дегенеративно-дистрофические изменения приводят к развитию заболевания у больных увеопатиями, аномалией Фукса и иридокорнеальным эндотелиальным синдромом.
- Неопластическую. Возникновению этого варианта патологии предшествует появление доброкачественных и злокачественных новообразований глазного яблока, которые ведут к повышению офтальмотонуса.
Симптомы вторичной глаукомы
Клинические проявления зависят от особенностей течения основной патологии. В большинстве случае поражается только один глаз. При двухсторонней форме изменения развиваются несимметрично. Длительное время симптоматика заболевания отсутствует, за исключением случаев, когда возникновение патологии обусловлено травмой или послеоперационными осложнениями. При увеальной форме пациенты чаще ощущают повышение офтальмотонуса в вечернее время. Наблюдается быстрое, прогрессирующее снижение остроты зрения. Зачастую в течение 1 года наступает полная потеря зрительных функций.
Если заболевание развивается на фоне эктопии хрусталика или катаракты, пациенты предъявляют жалобы на резкую боль в области глазницы, снижение зрения, покраснение переднего отдела глазного яблока. Патология может сопровождаться тошнотой, рвотой, головокружением. Отличительный симптом – дрожание хрусталика при движениях глазных яблок (факодонез). Особенность глаукомы у больных с онкологическими новообразованиями — в медленном нарастании клинических проявлений. Общие симптомы для всех форм – появление радужных кругов перед глазами при взгляде на источник света, затуманивание зрения, головная боль с иррадиацией в надбровные дуги. Часто нарушается аккомодационная способность, в которой превалирует спазм аккомодации. При выполнении зрительной работы быстро развиваются астенопические жалобы.
Осложнения
Наиболее тяжелое осложнение вторичной глаукомы – слепота. Пациенты с данной патологией подвержены высокому риску атрофии зрительного нерва. При сосудистой форме и раневом генезе заболевания распространены кровоизлияния в стекловидное тело и гифема. Возможен рубеоз радужки и неоваскуляризация роговицы. Увеальная глаукома часто осложняется воспалительными и инфекционными заболеваниями (кератит, конъюнктивит, блефарит). Из-за быстрого повышения офтальмотонуса при контузии глаза в практической офтальмологии широко встречаются субконъюнктивальные кровотечения (гипосфагма). При разрывах капсулы хрусталика у пациентов с факолитической формой возникает пластический иридоциклит.
Диагностика
Для постановки диагноза вторичной глаукомы необходимо тщательно собрать анамнез с целью выявления первопричины повышения давления внутри глазного яблока. Наружный осмотр неинформативен, что часто приводит к несвоевременной диагностике. Специфический комплекс офтальмологического обследования включает:
- Гониоскопию. Исследование позволяет изучить состояние передней камеры глазного яблока, выявить морфологические предпосылки к нарушению оттока ВГЖ, а именно, сниженные объема камеры, закрытие УПК, патологии строения роговично-склеральной трабекулы.
- Бесконтактную тонометрию глаза. Выявляется превышение внутриглазным давлением толерантных значений (более 20-22 мм. рт. ст.). Для большей информативности изменений внутриглазного давления в течение дня используют суточную тонометрию.
- УЗИ глаза. Цель ультразвукового исследования – выявить органические изменения, которые потенцируют повышение офтальмотонуса. Дает возможность выявить злокачественные новообразования, признаки эктопии хрусталика.
- Офтальмоскопию. Осмотр глазного дна информативен для визуализации атрофических изменений диска зрительного нерва, вторичного поражение внутренней оболочки, которые возникают при длительном повышении офтальмотонуса.
- Биомикроскопию глаза. Проводится детальный осмотр передней поверхности глазного яблока для выявления язв и бельма роговой оболочки.
- Электронную тонографию глаза. Для вторичной глаукомы характерен инвертированный тип кривой повышения давления с типичным вечерним подъемом. Тонография глазного яблока позволяет измерить объем ВГЖ и рассчитать коэффициент ее оттока.
- Визометрию. У пациентов диагностируют прогрессирующую зрительную дисфункцию. При дополнительном проведении рефрактометрии чаще определяется миопический тип клинической рефракции.
- Периметрию. Определяется сужение полей зрения по концентрическому типу.
Лечение вторичной глаукомы
Цель этиотропной терапии – устранить основное заболевание. При контузионной природе заболевания терапевтическая тактика базируется на назначении анальгетиков, седативных и десенсибилизирующих средств. В комплексном лечении патологии используется:
- Гипотензивная терапия. Применяется при диагностике повышенного ВГД, вызванного гиперсекрецией водянистой влаги. Для достижения толерантных значений внутриглазного давления используют лекарственные средства из группы М-холиномиметиков, адреноблокаторов, ингибиторов карбоангидразы, альфа-2-агонистов и простагландинов.
- Хирургическое вмешательство. При развитии патологии из-за бомбажа роговой оболочки и уменьшения объема передней камеры показана трепанация роговицы. Возникновение зрачкового блока из-за эктопии требует экстракции хрусталика. Если заболевание сопровождается стойким расширением зрачка, на роговую оболочку накладывают кисетный шов. При сужении роговично-склерального угла применяется иридэктомия.
- Лазерная коагуляция сетчатки. Методика лечения используется только при стойком повышении давления в сосудах эписклеры. Доказана эффективность применения тотальной лазерной коагуляции сетчатки при первых признаках стаза крови в передних цилиарных артериях и водоворотных венах.
Прогноз и профилактика
Прогноз для жизни и трудоспособности при своевременной диагностике и лечении благоприятный. Особенность вторичной глаукомы в том, что при адекватной терапии можно восстановить зрительные функции. Специфические методы профилактики отсутствуют. В основе неспецифических превентивных мер лежит контроль показателей внутриглазного давления. Регулярно измерять ВГД рекомендовано пациентам, которым в течение года проводились оперативные вмешательства на глазном яблоке, имеющим травматические повреждения или отягощенный офтальмологический анамнез (глазная мигрень, катаракта, кровоизлияния в переднюю камеру).
Вторичная глаукома — лечение в Москве
Источник
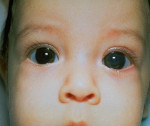
Врожденная глаукома – чаще наследственное заболевание, сопровождающееся постепенным увеличением внутриглазного давления и обусловленными этим сопутствующими зрительными нарушениями. К основным симптомам данной патологии относят увеличение размеров глаз (у грудных детей), болезненность, которая приводит к беспокойству и плаксивости ребенка, светобоязнь, миопию или астигматизм. Диагностика врожденной глаукомы производится на основании данных офтальмологического осмотра, изучения наследственного анамнеза пациента и течения беременности, генетических исследований. Лечение только хирургическое, причем оно должно быть выполнено как можно ранее до развития необратимых вторичных нарушений в органе зрения.
Общие сведения
Врожденная глаукома – генетическое, реже — приобретенное внутриутробно заболевание, которое характеризуется недоразвитием угла передней камеры глаза и трабекулярной сети, что в конечном итоге приводит к повышению внутриглазного давления. Это состояние считается в офтальмологии относительно редким и встречается примерно в одном случае на 10000 родов. Некоторые исследователи полагают, что данная статистика не совсем корректно отражает действительность, ведь некоторые формы врожденной глаукомы могут не проявлять себя вплоть до подросткового возраста. Несмотря на то, что патология наследуется по аутосомно-рецессивному механизму, среди больных несколько превалируют мальчики – половое распределение составляет примерно 3:2. По возрасту развития основных симптомов, а также наличию или отсутствию генетических дефектов выделяют несколько клинических форм этого заболевания. Важность своевременного обнаружения врожденной глаукомы обусловлена тем, что без проведенного лечения ребенок может ослепнуть через 4-5 лет после развития первых проявлений патологии.
Причины врожденной глаукомы
Подавляющее большинство случаев врожденной глаукомы (не менее 80%) сопровождаются мутацией гена CYP1B1, который локализован на 2-й хромосоме. Он кодирует белок цитохром Р4501В1, функции которого на сегодняшний момент изучены недостаточно. Предполагается, что данный протеин каким-то образом участвует в синтезе и разрушении сигнальных молекул, которые принимают участие в формирование трабекулярной сети передней камеры глаза. Дефекты структуры цитохрома Р4501В1 приводят к тому, что метаболизм вышеуказанных соединений становится аномальным, что и способствует нарушению формирования глаза и развитию врожденной глаукомы. Сейчас известно более полусотни разновидностей мутаций гена CYP1B1, достоверно связанных с развитием этого заболевания, однако выявить взаимосвязь между конкретными дефектами гена и определенными клиническими формами пока не удалось.
Помимо этого, имеются указания на роль в развитии врожденной глаукомы другого гена – MYOC, расположенного на 1-й хромосоме. Продукт его экспрессии, протеин под названием миоциллин, широко представлен в глазных тканях и тоже участвует в формировании и функционировании трабекулярной сети глаза. Ранее было известно, что мутации этого гена являются причиной открытоугольной ювенильной глаукомы, однако при одновременном повреждении MYOC и CYP1B1 развивается врожденная разновидность этой патологии. Некоторые исследователи в области генетики полагают, что обнаружение мутации гена миоциллина на фоне дефекта CYP1B1 не играет особой клинической роли в развитии врожденной глаукомы и является просто совпадением. Мутации этих обоих генов наследуются по аутосомно-рецессивному механизму.
Кроме наследственных форм данной патологии примерно в 20% случаев диагностируется врожденная глаукома при отсутствии, как случаев заболевания, так и патологических генов у родителей. В таком случае причиной развития глазных нарушений могут выступать либо спонтанные мутации, либо же повреждение тканей глаза во внутриутробном периоде. Последнее может быть обусловлено заражением матери во время беременности некоторыми инфекциями (например, токсоплазмозом, краснухой), внутриутробными травмами плода, ретинобластомой, воздействием тератогенных факторов. Так как в такой ситуации не имеется генетического дефекта, такая патология носит название вторичной врожденной глаукомы. Кроме того, подобные нарушения органа зрения могут иметь место при некоторых других врожденных заболеваниях (синдром Марфана, ангидроз и другие).
Какой бы ни была причина врожденной глаукомы, механизм развития нарушений при этом состоянии практически одинаков. Из-за недоразвития угла передней камеры глаза и трабекулярной сети водянистая влага не может нормально покидать полость, происходит ее накопление, что сопровождается постепенным повышением внутриглазного давления. Особенностью врожденной глаукомы является тот факт, что ткани склеры и роговицы у детей обладают большей эластичностью, нежели у взрослых, поэтому при накоплении влаги происходит увеличение размеров глазного яблока (чаще всего двух сразу, очень редко только одного). Это несколько снижает внутриглазное давление, однако со временем и этот механизм становится недостаточным. Происходит уплощение хрусталика и роговицы, на последней могут появиться микроразрывы, ведущие к помутнению; повреждается диск зрительного нерва, истончается сетчатка. В конечном итоге может произойти ее отслоение – помутнение роговицы и отслойка сетчатой оболочки глаза являются ведущими причинами слепоты при врожденной глаукоме.
Классификация врожденной глаукомы
В клинической практике врожденную глаукому в первую очередь разделяют на три разновидности – первичную, вторичную и сочетанную. Первичная обусловлена генетическими нарушениями, наследуется по аутосомно-рецессивному механизму и составляет около 80% от всех случаев заболевания. Причина вторичной врожденной глаукомы заключается во внутриутробном нарушении формирования органов зрения различной негенетической природы. Сочетанная разновидность, как следует из названия, сопровождается наличием врожденной глаукомы на фоне иных наследственных заболеваний и состояний. Первичная форма, обусловленная генетическими дефектами, в свою очередь подразделяется на три клинические формы:
- Ранняя врожденная глаукома – при этой форме признаки заболевания выявляются при рождении, или они проявляются в первые три года жизни ребенка.
- Инфантильная врожденная глаукома – развивается в возрасте 3-10 лет, ее клиническое течение уже мало похоже на ранний тип и приближается к таковому у взрослых людей при других формах глаукомы.
- Ювенильная врожденная глаукома – первые проявления этой формы заболевания регистрируются чаще всего в подростковом возрасте, симптоматика очень схожа с инфантильным типом патологии.
Такой значительный разлет в возрасте развития врожденной глаукомы напрямую связан со степенью недоразвития трабекулярной сети глаза. Чем более выражены нарушения в этих структурах, тем ранее начинается накопление водянистой влаги с повышением внутриглазного давления. Если же недоразвитие угла передней камеры глаза не достигает значительных величин, то в первые годы жизни ребенка отток происходит вполне нормально, и нарушения развиваются намного позже. Попытки связать определенные клинические формы врожденной глаукомы с конкретными типами мутаций гена CYP1B1 на сегодняшний день не увенчались успехом, и механизмы развития того или иного типа заболевания до сих пор неизвестны.
Симптомы врожденной глаукомы
Наиболее своеобразными проявлениями характеризуется ранняя форма первичной врожденной глаукомы, что обусловлено анатомическими особенностями строения глаза у ребенка в возрасте до 3-х лет. В очень редких случаях глаукомные изменения можно заметить уже при рождении, чаще всего в первые 2-3 месяца жизни заболевание ничем себя не проявляет. Затем ребенок становится беспокойным, плохо спит, очень часто капризничает – это обусловлено неприятными и болезненными ощущениями, с которых дебютирует врожденная глаукома. Через несколько недель или месяцев начинается медленное увеличение размеров глазных яблок (реже — одного). Повышение внутриглазного давления и эластичность тканей склеры могут привести к значительному увеличению глаз, что внешне создает ложное впечатление красивого «большеглазого» ребенка. Затем к этим симптомам присоединяется отек, светобоязнь, слезотечение, иногда возникает помутнение роговицы.
Инфантильная и ювенильная формы врожденной глаукомы во многом очень схожи, различается только возраст развития первых проявлений заболевания. Увеличения размеров глазных яблок при этом, как правило, не происходит, патология начинается с ощущения дискомфорта и болезненности в глазах, головных болей. Ребенок может жаловаться на ухудшение зрения (появление ярких ореолов вокруг источников света, «мошки» перед глазами). Эти типы врожденной глаукомы часто сопровождаются другими нарушениями зрительного аппарата – косоглазием, астигматизмом, миопией. Со временем происходит сужение поля зрения (теряется возможность видеть предметы боковым зрением), нарушение темновой адаптации. Светобоязнь, отек и инъецирование сосудов склеры, характерные для ранней формы заболевания, при этих формах чаще всего не наблюдаются. При отсутствии лечения любая разновидность врожденной глаукомы со временем приводит к слепоте по причине отслойки сетчатки или атрофии зрительного нерва.
Диагностика врожденной глаукомы
Выявление врожденной глаукомы производится врачом-офтальмологом на основании данных осмотра, офтальмологических исследований (тонометрии, гониоскопии, кератометрии, биомикроскопии, офтальмоскопии, УЗ-биометрии). Также немаловажную роль в диагностике этого состояния играют генетические исследования, изучение наследственного анамнеза и течения беременности. При осмотре обнаруживаются увеличенные (при ранней форме) или нормальные размеры глаз, может также наблюдаться отек окружающих глазное яблоко тканей. Горизонтальный диаметр роговицы увеличен, на ней возможны микроразрывы и помутнение, склера истончена и имеет голубоватый оттенок, поражается при врожденной глаукоме и радужная оболочка – в ней возникают атрофические процессы, зрачок вяло реагирует на световые раздражители. Передняя камера глаза углублена (в 1,5-2 раза больше возрастной нормы).
На глазном дне длительное время не возникает никаких патологических изменений, так как за счет увеличения размеров глазного яблока внутриглазное давление поначалу не достигает значительных величин. Но затем довольно быстро развивается экскавация диска зрительного нерва, однако при снижении давления выраженность этого явления также уменьшается. По причине увеличения размеров глаз при врожденной глаукоме происходит истончение сетчатки, что при отсутствии лечения может привести к ее разрыву и регматогенной отслойке. Часто на фоне таких изменений обнаруживается миопия. Тонометрия показывает некоторое увеличение внутриглазного давления, однако этот показатель следует сопоставлять с передне-задним размером глаза, так как растяжение склеры сглаживает показатели ВГД.
Изучение наследственного анамнеза может выявить аналогичные изменения у родственников больного, при этом нередко удается определить аутосомно-рецессивный тип наследования – это свидетельствует в пользу первичной врожденной глаукомы. Наличие в ходе беременности инфекционных заболеваний матери, травм, воздействия тератогенных факторов указывает на возможность развития вторичной формы заболевания. Генетическая диагностика осуществляется посредством прямого секвенирования последовательности гена CYP1B1, что позволяет выявить его мутации. Таким образом, однозначно доказать наличие первичной врожденной глаукомы может только врач-генетик. Кроме того, при наличии такого состояния у одного из родителей или их родственников можно производить поиск патологической формы гена до зачатия или пренатальную диагностику путем амниоцентеза или других методик.
Лечение и прогноз врожденной глаукомы
Лечение врожденной глаукомы только хирургическое, возможно применение современных лазерных технологий. Консервативная терапия с использованием традиционных средств (капли пилокарпин, клонидин, эпинефрин, дорзоламид) является вспомогательной и может использоваться некоторое время в ходе ожидания операции. Хирургическое вмешательство сводится к формированию пути оттока водянистой влаги, что снижает внутриглазное давление и устраняет врожденную глаукому. Метод и схема проведения операции избирается в каждом конкретном случае строго индивидуально. В зависимости от клинической картины и особенностей строения глазного яблока могут выполняться гониотомия, синустрабекулэктомия, дренажные операции, лазерная циклофотокоагуляция или циклокриокоагуляция.
Прогноз врожденной глаукомы при своевременной диагностике и проведении операции чаще всего благоприятный, если же лечение произведено с опозданием, возможны различные по выраженности нарушения зрения. После устранения глаукомы необходимо не менее трех месяцев диспансерного наблюдения у офтальмолога.
Источник