Репаративные процессы в роговице
Канюков В.Н., Стадников А.А., Трубина О.М., Яхина О.М.
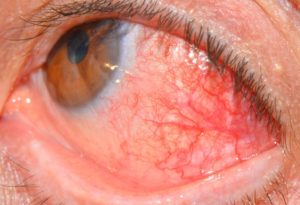
Регенерация роговицы при травматических повреждениях переднего отрезка глаза является основополагающим фактором в восстановлении зрения у пациентов. Особую важность представляет изучение репаративных процессов в роговице после химических ожогов, так как в результате ожога нарушается не только ее структура, но и метаболизм. В связи с особенностями кровотока области лимба в зоне ожога быстро накапливаются токсические продукты, что еще более усугубляет патологический процесс [3-5, 7]. Патогенетически направленное лечение должно проводиться с целью восстановления оптических свойств роговицы, подавления аутоиммунных реакций, предупреждения избыточной васкуляризации, конъюнктивальных сращений, иритов, иридоциклитов, вторичной глаукомы и катаракты [2, 6, 9].
Механизмы патологического процесса и реакций организма при ожогах глаз настолько сложны и разнообразны, что применяемые средства терапии далеко не всегда купируют развитие активного ожогового процесса [8]. Установлено, что растворы щелочей, омыляя жиры и жироподобные вещества клеточных мембран, проникают в тело клетки, изменяя рН клеточного вещества, приводят к растворению (колликвации) белков, разрушают клетку и проникают глубоко в ткани [2, 4, 5, 11].
Щелочной ожог роговицы вызывает дестабилизацию уровня гликозаминогликанов оптических сред глаза и сыворотки крови, выражающуюся в изменении их фракционного состава, при этом наблюдается активация реакций глюкуронидной конъюгации в тканях органа зрения, наиболее выраженная в переднем отрезке глаза [9]. Иной механизм воздействия оказывают растворы кислот, вызывая некроз конъюнктивы и роговицы с коагуляцией белков, что предотвращает распространение детергента вглубь тканей [2, 8, 11].
При ожоговой болезни глаз нередко происходит отторжение и некроз трансплантата вследствие нарушения микроциркуляции собственной поврежденной ткани, развития в организме иммунологического конфликта, формирования васкуляризованных бельм [3-5, 10].
Следовательно, разработка медикаментозных и хирургических методов оптимизации репаративной регенерации роговицы после химических ожогов является одним из факторов успешного лечения данной патологии.
Цель
Оценка течения процессов репаративной регенерации роговицы при применении биопластического материала – наноструктурированного биополимера гиалуроновой кислоты на модели химического (щелочного и кислотного) ожога роговицы.
Материал и методы
Наноструктурированный биопластический материал «Гиаматрикс» представляет собой биополимер гиалуроновой кислоты в виде плёнки толщиной 0,3-0,5 мм (рис. 1, 2). Он разработан в научно-производственной лаборатории клеточных технологий Оренбургского государственного университета и предназначен для восстановления дефектов кожных покровов [1], разрешен к применению в общей и пластической хирургии (регистрационное удостоверение ФСР 2011/10313 от 18.03.2011 г.).
Экспериментальное моделирование химического ожога роговицы проведено на 36 кроликах (72 глаз).
В первой серии эксперимента на 36 глазах 18 экспериментальных животных моделировали щелочной ожог роговицы. После чего животных разделили на две группы: опытную (18 правых глаз) и контрольную (18 левых глаз).
В опытной группе проводили аппликацию биопластического материала «Гиаматрикс» по оригинально разработанной методике (Патент на изобретение № 2485919 от 12.04.2012 г.). После стандартной обработки операционного поля, проведения эпибульбарной анестезии (Sol. Inocaini 0,4% 3-кратно), веки фиксировали векорасширителем.
Предварительно из биоматериала
«Гиаматрикс» трепаном выкраивали диск диаметром 10 мм. Затем «Гиаматрикс» укладывали на поверхность роговицы, смачивали физиологическим раствором для улучшения эластических свойств биоматериала и накрывали мягкой контактной линзой, которую фиксировали двумя перекидными швами.
В контрольной группе закладывали глазной гель Солкосерил. В обеих группах проводили инстилляции 0,3%-ного раствора Ципромеда.
Во второй серии формировали кислотный ожог роговицы средней степени тяжести (18 кроликов, 36 глаз). Далее в опытной группе проводили аппликацию биопластического материала по описанной выше методике (18 глаз), а в контрольной группе – закладывание глазного геля Солкосерил (18 глаз).
Клиническое исследование включало биомикроскопию переднего отрезка глаз с динамической оценкой состояния конъюнктивы, роговицы и глубже лежащих сред; флуоресцеиновую пробу.
На сроках 3, 7, 14, 30 и 90 суток животных выводили из эксперимента методом передозировки наркоза (3-разовых доз хлороформа).
Для проведения светооптического и иммуноцитохимического исследований энуклеированные глазные яблоки фиксировали в растворе нейтрального формалина, подвергали макромикроскопическому препарированию, затем промывали проточной водой, обезвоживали в спиртах восходящей концентрации и заливали в парафин, выполняли серии меридиональных гистологических срезов с применением окраски гематоксилин-эозином. Изучение ультратонких срезов и их фотографирование проводили на электронном микроскопе ЭМВ 100АК при увеличении от ?8000 до ?40000.
Для иммуноцитохимического исследования использовали первичные антитела с целью обнаружения клеток экспрессии белков р53 и bcl2, участвующих в инициации апоптоза и выявлении интернуклеосомальной фрагментации ДНК. Во всех случаях подсчитывали процент окрашенных клеток в случайно выбранных полях зрения.
Результаты
Щелочной ожог сопровождался признаками роговичного синдрома: блефароспазмом, светобоязнью, слезотечением. Клиническое исследование показало, что воздействие 2,5%-ного раствора гидрооксида натрия приводило к формированию эрозии роговицы в виде круга диаметром до 7 мм, что сопровождалось признаками реактивного воспаления: отеком и инъекцией конъюнктивы. Применение биопластического материала «Гиаматрикс» способствовало эпителизации раневого дефекта у всех животных опытной группы к 4 суткам (рис. 3), на сроке 7 суток в области воздействия щелочи отмечали нежное поверхностное помутнения (рис. 4), в то время как в контрольной группе дефект сохранялся до 7 суток. Так же было отмечено, что признаки асептического воспаления в опытной группе проходили на трое суток раньше, чем в контрольной группе.
Морфологически в зоне роговицы, подверженной действию щелочи, отмечали гибель и десквамацию клеток переднего эпителия роговицы, фрагментацию и исчезновение клеток стромы. Исследование конъюнктивы показало, что ток крови резко замедлялся, в мелких сосудах формировались тромбы, плазма выходила в окружающие ткани, что сопровождалось резким отеком конъюнктивы. Следует отметить, что характер морфологических изменений тканей глаза в условиях некроза, вызванного химической травмой, был сходным (относительно воздействия кислот и щелочей).
Существенным являлось то обстоятельство, что по мере усиления эрозивного процесса (поздние сроки наблюдений) в живых (сохранных в гистологическом отношении тканях), прилежащих к некротизированным, возникало выраженное реактивное воспаление. Оно характеризовалось вазодилатацией кровеносных сосудов, экстравазацией плазмы и форменных элементов крови с формированием демаркационной зоны (рис. 5).
Анализ серийных гистологических препаратов показал, что демаркационная линия в исследованных участках глаза была выражена слабо, а в лимбальной зоне она отсутствовала. Это приводило к утяжелению и прогрессированию некротических процессов эпителиальных и соединительнотканных структур.
В переднем эпителии роговицы и эпителии слизистой оболочки конъюнктивы отмечались грубые повреждения, завершающиеся десквамацией эпителиоцитов и обнажением базальной мембраны. Одновременно усиливалась секреция слизь-продуцирующих элементов (бокаловидные клетки конъюнктивального эпителия) (рис. 6).
При этом альтерация тканей роговицы не сопровождалась адекватными экссудативной (сосудистой) и продуктивной (пролиферативной) реакциями, что свидетельствовало о сохранении дистрофических процессов в моделируемых условиях. Таким образом, фокус воспаления в связи с процессами экссудации не в полной мере выполняет дренажную и элиминативную функции при ожоговой травме роговицы.
Преобладающее большинство эмигрирующих лейкоцитов составили сегментоядерные нейтрофилы. Помимо них, значительно реже экстравазации подвергались лимфоциты, моноциты, базофильные гранулоциты и эозинофилы. Данные клетки продвигались в зону повреждения роговицы между волокнистыми структурами по направлению к центру воспаления, где и наблюдалось их наибольшее скопление (рис. 7).
В области повреждения роговицы и прилежащих участков конъюнктивы, по мере угасания воспалительного процесса, происходила активизация камбиальных клеток и клеток фибробластического дифферона (рис. 8). При этом образовывались волокнистые структуры без разрастаний эпителиальной ткани.
Исследование показало, что травматическое (химическое) повреждение роговицы экспериментальных животных приводило к развитию некротического воспаления. Исход альтеративного воспаления зависел от глубины поражения и повреждения тканей глаза (по срокам наблюдений) и, как правило, заканчивался рубцеванием посттравматического дефекта.
Морфологические исследования, проведенные на различных сроках эксперимента, позволили устано-вить последовательность процессов, протекающих от момента нанесения химического ожога роговицы до завершения ее восстановления, которые были различными в опытной и контрольной группах.
Воздействие кислоты (3%-ный раствор уксусной кислоты) на неизмененную роговицу приводило к поверхностному помутнению (рис. 9), но инстилляция 0,1%-ного раствора флюоресцеина натрия показала, что ткань стромы не прокрашивалась, а следовательно эпителиальный покров был сохранен (рис. 10). Однако гистологически выявляли коагуляционный некроз эпителия без отторжения уплотненного струпа. В процессе лечения некротизированные ткани отторгались и на более поздних сроках исследования флуоресцеиновая проба становилась положительной. Клинически было показано, что применение «Гиаматрикса» способствовало более раннему уменьшению отека роговицы и признаков реактивного воспаления по сравнению с контрольной группой, помутнение в опытной группе рассасывалось к 14 суткам, в то время как в контроле – к 30 суткам.
Морфологическое исследование глаз на сроке 3-х суток как опытной, так и контрольной групп пока зало, что клетки переднего эпителия роговицы были повреждены; в мелких сосудах конъюнктивы формировались тромбы. Кроме деструктивных изменений эпителиоцитов, отмечались нарушения в строме, которые строго соответствовали участку ожога и захватывали не менее 1/3 толщины стромы. В период с 7 по 14 сутки в опытной группе уже наблюдали переход экссудативной фазы воспаления в пролиферативную, в контрольной группе этот процесс был выявлен только к концу месяца.
Иммуноцитохимическое исследование показало, что при применении биопластического материала снижалась апоптотическая доминанта эпителиоцитов и фибробластов роговицы, взятой для исследования на третьи и четырнадцатые сутки эксперимента. С другой стороны, возрастала экспрессия синтеза протеина bcl2, что свидетельствовало о выраженности пролиферативной фазы воспаления, это подтверждало результаты световой микроскопии. Таким образом, иммуноцитохимическое исследование показало, что аппликация «Гиаматрикса» оптимизировала репаративные гистогенезы с включением механизмов лимитирования экспрессии проапоптатического гена p53, уменьшение иммунопозитивных эпителиоцитов в 2,5-3 раза по сравнению с контрольной группой
Выводы
Аппликация биопластического материала на роговицу на начальных этапах лечения повреждений роговицы (щелочной и кислотный ожог) уменьшает выраженность отека и гиперемии и, как следствие, сокращает экссудативную фазу воспаления.
В результате клинико-функционального анализа особенностей течения щелочного повреждения роговицы установлено, что применение «Гиаматрикса» ускоряет закрытие дефекта роговицы в 1,5 раза быстрее по сравнению с контрольной группой.
Применением биоматериала в исходе кислотного ожога за счет сокращения экссудативной фазы воспаления ускоряет рассасывание помутнений роговицы по сравнению с применением глазного геля Солкосерил.
Источник
Что такое дистрофия роговицы глаза?
Описание заболевания
Дегенерация роговицы глаза, или дистрофия- это серьезное офтальмологическое заболевание невоспалительного характера, в результате которого происходит помутнение роговой оболочки. Из-за этого могут возникнуть осложнения, которые приведут к слепоте. Лечение болезни осложняется тем, что причин развития патологии может быть несколько. Именно поэтому дегенерацию роговицы глаз нельзя назвать самостоятельным заболеванием.
Она объединяет в себе ряд заболеваний, которые не характеризуются воспалительным процессом.
Дистрофия роговицы затрагивает оба глаза, а если вовремя не начать лечения, промедление может привести к полной потере зрения. Учеными доказано, что заболевание имеет наследственный характер и наследуется от родителей к детям. Однако, дистрофия роговицы может длительное время не проявлять себя. У большинства пациентов первая симптоматика может дать о себе знать в 30–40 лет. Однако, самой опасной считается дистрофия роговицы, которая возникает у новорожденных. Несвоевременная диагностика патологии может привести к полной слепоте уже через несколько месяцев после рождения.
Симптомы заболевания
Перед тем как начать разговор о лечении патологии, необходимо сказать пару слов о том, как себя проявляет дистрофия роговицы. К основным симптомам наследственного заболевания можно отнести:
- незначительное покраснение роговицы глаз;
- постоянное слезотечение и боль в глазах при падении солнечного света;
- болевые ощущения, которые не снимаются обезболивающими глазными каплями;
- ощущение инородного тела в глазах;
- отечность;
- быстрая потеря зрения.
Типология заболевания
Заболевание может проявляться по разному. По симптоматике выделяют несколько типов заболевания:
- эпителиальная дистрофия роговицы, которая развивается уже в детском возрасте. Этот тип заболевания характеризуется образованием кистообразных образований на роговице глаза, которые приводят к помутнению;
- мембранная дистрофия — первичная патология, которая в большинстве случаев поражает один глаз. Мембранная дистрофия может очень длительное время не проявлять себя, однако очень редко регрессирует;
- стромальная форма дистрофии. Эта форма заболевания суммирует несколько видов патологии: дистрофия Гренува, дистрофия Шиндера, патология Димера и кератоконус.
- эндотелиальная дистрофия — тип патологии, когда соединительная ткань роговой оболочки очень сильно истончается. Вследствие этого возникает отечность, а роговица приобретает серо-голубой цвет.
Лечение дистрофии роговицы глаза
Если правильно подойти к лечению, можно добиться полного замедления распространения дистрофии, однако полностью избавиться от дистрофии роговицы поможет только хирургическая операция.
Рассмотрим наиболее популярные методы консервативного лечения, которые используются врачами-офтальмологами.
Глазные капли
Врачи на первых парах лечения отдают предпочтение лечебным глазным каплям и мазям, которые помогают восстановить целостность тканей роговицы глаза, увлажнить слизистую и снять отек. После снятия отека и воспаления слизистой, назанчают кератолитические препараты.
К наиболее эффективным лекарственным средствам можно отнести:
- капли для глаз «Тауфон», в состав которых входит вещество таурин. Это соединение способствует улучшению энергетических процессов в клетках. Оно стимулирует регенерацию и репарацию тканей, сопровождающихся резкими нарушениями метаболизма. Кроме этого, таурин нормализует функции клеточных мембран;
- капли «Баларпан». Препарат активирует репаративные процессы при нарушениях питания роговицы. В частности, при дистрофии роговицы, травматизации, ожогах и воспалительных заболеваниях;
- глазной гель «Корнерегель» обладает высокими репаративными свойствами. Декспантенол, который входит в его состав, является предшественником пантотеновой кислоты, которая участвует во всех процессах метаболизма;
- глазную мазь «Солкосерил». Препарат обладает аналогичными свойствами, что и «Корнерегель», за счет аналогичного состава;
- мазь и глазные капли «ВитА-Пос». Лекарственное средство содержит натуральный ретинола пальмитат, который позволяет восстановить структуру роговицы. Кроме этого, витамин А входит в состав пигмента, отвечающего за зрение.
Лечебные линзы
Лечебные контактные линзы известны довольно давно. Первые сведения о них появились в 1882 году. Они представляли собой желатиновые чашечки, которые наполнялись лекарственными веществами. На данный момент наука ушла далеко вперед, и теперь используются гидрофильные мягкие контактные линзы.
Лечебные линзы используются на ранних стадиях заболевания, когда основным фактором снижения зрения является отек слизистой роговицы глаза. При наличии помутнения, складок и трещин мембраны роговицы предпочтение отдается трансплантационным методам лечения. Лечить заболевание можно и при помощи линз, однако должной эффективности наблюдаться не будет, особенно в запущенных стадиях.
Лечение дистрофии роговицы глаза народными средствами
Медикаментозное лечение и оперативное вмешательство имеют серьезную доказательную базу, поэтому их эффективность оспорить очень сложно. Тем не менее, пациенты отдают предпочтение народным методам лечения. Ученые связывают этот факт с высокой стоимостью лечения патологии.
Однако, если рассмотреть данный метод с точки зрения эффективности, можно сказать, что народные методы прекрасно зарекомендовали себя в лечении дистрофии роговоцы глаз.
Медовые капли
О полезных свойствах меда известно довольно давно. Практически все продукты пчеловодства нашли свое применение в народной медицине.
Для того чтобы изготовить медовые капли, необходимо небольшое количество меда и маточное молочко. Компоненты смешивают и заливают в равной пропорции теплой водой. Полученные капли закапывают в конъюнктивальный мешок 2–3 раза в день. Кроме этого, советуют принимать настой прополиса параллельно основному лечению.
Апитерапия направлена на укрепление иммунной защиты организма. Однако при аллергии на пчелиные продукты метод применять нельзя — будет отек слизистой и сильное раздражение.
Травяные примочки
Не менее популярным методом считается траволечение, как самый древний способ целебной медицинской практики. Лечить дистрофию предпочитали следующими составами:
- примочки с использованием очанки;
- луково-медовые капли, которые готовятся аналогично медовым;
- капли из желчи щуки;
- закапывание грудного молока.
Пихтовая живица
В 19 веке, когда народная медицина была единственным методом лечения, знахари и врачи лечили многие заболевания с помощью целительной живицы.
Натуральное лекарство обладает прекрасными противомикробными и антибактериальными свойствами. Благодаря этому его используют и в наше время.
Капли из живицы необходимо делать на основе кедрового масла (97,5 на 2,5 %). В чистом виде живицу закапывать в глаза нельзя, так как можно получить ожог. Кедровое масло полезный продукт для глаз, его можно закапывать и в профилактических целях перед сном. Кедровое масло обладает свойством восстанавливать клетки тканей глаза. В профилактических целях масло кедра закапывают в каждый глаз по капле 1,5 месяца.
Как еще можно лечить дистрофию роговицы глаза
Несмотря на всю эффективность народного лечения, такими способами лучше пользоваться после консультации специалиста. На данный момент, самым лучшим методом является хирургическое вмешательство или кератопластика. Дистрофия роговицы предполагает поэтапное поражение тканей, или их отмирание.
В ходе данной операции послойно удаляется пораженная ткань. Если дегенерация глаза имеет локальный характер, на места, где была удалена роговица, пересаживается донорская ткань.
В большинстве случаев операция позволяет полностью восстановить зрение и убрать помутнение.
В случаях, когда зрение утрачено полностью, больной орган подлежит удалению. На его место имплантируют искусственный глаз. Обычно это происходит при лентовидной форме деградации, когда слизистая полностью травмирована, либо при развитии глаукомы.
Помимо кератопластики используется малоинвазивный метод кросслинкинга. Этот метод лечения представляет собой фотополимеризацию соединительного белка роговицы, а именно коллагена. Операция не требует каких-либо специальных условий. Пораженный орган обезболивают с помощью местной анестезии. Затем закапывают в глаз раствор рибофлавина и облучают ультрафиолетом. Орган, на котором была проведена процедура, закрывают специальной лечебной линзой и отправляют пациента домой.
Главным условием, которое гарантирует успех операции, является соблюдение правил асептики и чистоты поверхности раны после процедуры. Необходимо вовремя менять повязки и следовать рекомендациям офтальмолога.
Исходя из всех данных, можно сделать вывод, что дистрофия роговицы поддается лечению на любой стадии. Главным условием является своевременное обращение к врачу и соблюдение всех рекомендаций.
Что касается дистрофии у новорожденных, не стоит начинать лечение самостоятельно. У детей заболевание протекает гораздо быстрее, чем у взрослых. Главным условием успеха является своевременная диагностика. Если упустить момент, ребенок очень быстро потеряет зрение, а шансы на его восстановление будут сведены к минимуму.
Больше интересных статей →
Источник