Рефрактерная глаукома клапан ахмед
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ РЕФРАКТЕРНОЙ ГЛАУКОМЫ.
НАШ ОПЫТ ПРИМЕНЕНИЯ КЛАПАННОЙ СИСТЕМЫ
AHMED GLAUKOMA VALVE
ã Е.Ю. Красюк, С.И. Акулов
Ключевые слова: рефрактерная глаукома; клапан Ахмеда; имплантация.
В настоящей работе приведены краткие сведения о клапанной системе Ahmed Glaukoma Valve, а также показана эффективность ее применения на примере пациентов, прооперированных в условиях областного государственного бюджетного учреждения здравоохранения «Тамбовская офтальмологическая больница».
В последнее время в литературе для обозначения тяжелых форм глаукомы используется термин «рефрактерная глаукома», т. е. невосприимчивая к медикаментозной терапии и традиционной хирургии [1]. Сегодня в лечении данной патологии предпочтение отдается операциям, в ходе которых для снижения ВГД имплантируются различные дренажи, в основе которых лежит оригинальная конструкция Molteno (рис. 1).
Из множества видов дренажей наибольшее распространение получил клапан Ahmed (рис. 2).
Клапан был изобретен доктором М.А. Ахмедом, получившим образование в области медицины и инженерии в Государственном институте медицинских наук.
Разработку своего клапана начал в 1981 г. 14 лет длилась разработка клапана, 3 года – получение FDA (1993). Кроме США, клапан зарегистрирован и успешно применяется более чем в
50 странах [2]. Гибкий глаукомный силиконовый клапан Ahmed™ (Ahmed Glaucoma Valve – AGV) предназначен для лечения различных видов рефрактерной глаукомы, имеет прогнозируемое поведение, дает эффективный контроль внутриглазного давления на длительное время [3–4]. После имплантации клапана внутриглазное давление снижается немедленно, клапан сам регулирует и контролирует давление, не допуская излишнего оттока внутриглазной жидкости, тем самым снижая количество осложнений до минимума.
Клапан состоит из гибкого силиконового основания, мембраны и трубки (рис. 3). Основным элементом конструкции, собственно обладающим пропускной способностью, является двойная мембрана из тонкого эластомера. Она размещена и удерживается в растянутом состоянии на четырех штифтах. Трубка, изготовленная из медицинского силикона, обеспечивает доступ внутриглазной жидкости к мембране. Размещается клапан Ахмеда между склерой и теноновой капсулой на расстоянии 8–10 мм от лимба между прямыми мышцами и подшивается к склере через отверстия клапана. Трубка помещается в передней камере через предварительно произведенный прокол иглой 23G, подшивается к склере и накрывается предварительно выкроенным склеральным лоскутом. Операция имплантации проходит под местной анестезией. В послеоперационном периоде необходимо закапывать противовоспалительные капли в течение 2–3 недель [5].
Рис. 3. Конструкция клапанной системы Ahmed
Рассмотрим отдельно взятые случаи из практики имплантации клапанной системы Ahmed Glaukoma Valve.
Цель работы: показать на примере прооперированных в нашей больнице пациентов эффективность применения клапанной системы Ahmed Glaukoma Valve при глаукоме после травмы переднего отрезка (ребенок 10-ти лет), постувеальной и посттромботической глаукоме.
АКТУАЛЬНОСТЬ
Компенсация внутриглазного давления в детском возрасте является зачастую довольно сложной задачей из-за выраженных анатомических изменений в углу передней камеры. А потому основным методом лечения данной патологии является хирургический. Традиционные антиглаукоматозные операции не всегда позволяют добиться необходимого результата, чреваты высоким риском осложнений. Вследствие этого часто единственным вариантом может быть применение дренажных систем. При данном методе силиконовая трубочка, введенная в переднюю камеру, обеспечивает отток внутриглазной жидкости (ВГЖ), тем самым поддерживая постоянное внутриглазное давление (ВГД). В последние годы появились работы по применению клапанной системы Ahmed у детей. Преимуществами данного вмешательства являются микроинвазивность, низкий уровень осложнений, эффективность.
Неоваскулярная глаукома является одной из самых тяжелых форм вторичной глаукомы, часто неподдающаяся консервативной терапии, поэтому основным является хирургическое лечение [6]. Традиционные непроникающие и проникающие антиглаукоматозные операции не позволяют добиться требуемого эффекта из-за быстрой неоваскуляризации фильтрационной зоны и обширных кровоизлеяний из новообразованных сосудов в ходе операции. Предпочтение отдается использованию шунтирующих дренажей, что дает возможность достичь стойкого гипотензивного эффекта и, как следствие, купирования болевого синдрома.
МАТЕРИАЛЫ И МЕТОДЫ
В настоящей публикации рассматриваем 3 случая применения клапанной системы Ahmed Glaukoma Valve.
Случай № 1. Пациент Х., 2002 года рождения, обратился в поликлинику ОГБУЗ «ТОБ» 2 сентября 2012 г. с жалобами на нестерпимые боли в течение недели, отсутствие зрения левого глаза. Из анамнеза известно: 10 мая 2006 г. была получена травма левого глаза, с диагнозом «Проникающее корнеосклеральное ранение с выпадением оболочек, травматическая катаракта OS» пациент госпитализирован в детское отделение ОГБУЗ «ТОБ», где была произведена первичная хирургическая обработка проникающего корнеосклерального ранения. При выписке: VIS OS = светоощущение, слизистая бледно-розовая, узловые швы на роговице, склере, передняя камера неравномерной глубины, радужка спаяна с рубцом роговицы, зрачок неправильной формы, хрусталик мутный. Через 2 месяца были сняты швы, предложено оперативное лечение травматической катаракты.
До 2 сентября 2012 г. пациент к офтальмологу не обращался. При поступлении в стационар: VIS OS = 0, ВГД = 49 мм рт. ст., смешанная инъекция глазного яблока, корнеосклеральный рубец, спаянный с радужкой, роговица отечная, передняя камера практически отсутствует, радужка отечная, вне рубца прилежит к эндотелию роговицы, зрачок заращен. ЭХО-графически определяются высокоамплитудные сигналы. Установлен диагноз: «Вторичная болящая IV «С» глаукома, корнеосклеральный рубец, сращенный с радужкой, тотальная отслойка сетчатки». Консервативными методами достичь компенсации ВГД не удалось, болевой синдром не купировался. Вследствие этого было принято решение (как альтернатива удалению глазного яблока) имплантировать дренажную систему Ahmed Glaukoma Valve [7].
6 сентября 2012 г. произведена имплантация клапанной системы Ahmed Glaukoma Valve. Сам клапан был помещен в карман между склерой и теноновой капсулой на удалении 10 мм от лимба между прямыми мышцами в верхненаружном сегменте, силиконовая трубка (из-за отсутствия передней камеры) – в заднюю камеру. Уже на следующий день болевой синдром купировался, ВГД = 18 мм рт. ст. При выписке 12 сентября 2012 г. ВГД = 18 мм рт. ст. При контрольном осмотре через месяц пациента боли не беспокоят,
ВГД = 18 мм рт. ст. Больше пациент на контрольные осмотры не являлся.
Случай № 2. Пациентка Ж., 63-х лет, обратилась в поликлинику ОГБУЗ «ТОБ» 23 мая 2013 г. с жалобами на боли, покраснение, резкое снижение зрения правого глаза. В анамнезе в феврале 2013 г. факоэмульсификация катаракты с имплантацией интраокулярной линзы. При поступлении в стационар: VIS OD = 0,01 н/к, ВГД = 35 мм рт. ст., смешанная инъекция глазного яблока, выраженная болезненность при пальпации, множественные полиморфные преципитаты на эндотелии отечной роговицы, рубеоз радужки. Консервативная терапия дала возможность снять острый воспалительный процесс, но компенсировать ВГД не удалось. 28 мая 2013 г. была произведена глубокая склерэктомия на правом глазу – ВГД при выписке 19 мм рт. ст. Уже через 10 дней после выписки пациентка снова обратилась за помощью: VISOD = неправильная светопроекция, ВГД – 39 мм рт. ст., смешанная инъекция, роговица отечная, тотальная гифема. Было принято решение произвести шунтирующую операцию с использованием клапанной системы Ahmed Glaukoma Valve. 4 июля 2013 г. произведена имплантация клапанной системы Ahmed Glaukoma Valve. Передняя камера предварительно была промыта физиологическим раствором и заполнена вискоэластиком. При выписке ВГД = 20 мм рт. ст. При контрольных осмотрах через 1, 2 и 3 месяца ВГД компенсировано без применения миотиков, болевого синдрома нет.
Случай № 3. Пациентка Ф. обратилась за помощью 17 июня 2013 г. с жалобами на боли, покраснение, практически отсутствие зрения на правом глазу. Из анамнеза известно: больна в течение 2,5 месяцев, лечилась амбулаторно, затем в стационаре с диагнозом «Тромбоз центральной вены сетчатки, вторичная гипертензия OD». Из стационара пациентка была выписана с купированным болевым синдромом, внутриглазное давление 23 мм рт. ст. (при поступлении – 34 мм рт. ст.) на миотиках, VIS OD = счет пальцев у лица. В течение 2-х недель после выписки из стационара глаз не беспокоил, затем появился выраженный болевой синдром. При повторном поступлении в стационар: выраженная инъекция глазного яблока, роговица отечная, передняя камера средней глубины, рубеоз радужной оболочки, зрачок 4,5 мм, на свет не реагирует, ВГД – 46 мм рт. ст., VIS OD = правильная светопроекция. Учитывая тяжесть заболевания, 18 июня 2013 г. была произведена имплантация клапанной системыAhmed Glaukoma Valve. На следующий после операции день ВГД – 22 мм рт. ст., болевого синдрома нет. При выписке VIS OD = счет пальцев у лица, ВГД – 22 мм рт. ст. без миотиков. На контрольных осмотрах через 1, 2 и 3 месяца болевого синдрома нет, острота зрения на прежнем уровне, ВГД – 20–22 мм рт. Ст.
ВЫВОДЫ
1.Имплантация клапанной системы Ahmed Glaukoma Valve является эффективным методом хирургического лечения рефрактерной глаукомы у детей, позволяет сохранить глазное яблоко, что немаловажно для адаптации в детском коллективе.
2.Имплантация клапанной системы Ahmed Glaukoma Valve позволяет нормализовать ВГД и купировать болевой синдром даже у пациентов с неоваскулярной болящей глаукомой.
3.Имплантация клапанной системы Ahmed Glaukoma Valve может быть альтернативой не всегда эффективной традиционной хирургии глаукомы.
Источник
DOI: 10.21689/2311-7729-2016-16-2-103-107
Актуальность
Клапан Ahmed представлен в 1993 г. как первое дренажное устройство с однонаправленным клапанным механизмом, размещенным в корпусе дренажа, способствующим предотвращению послеоперационной гипотонии [1]. Имплантация клапана Ahmed считается эффективным методом лечения пациентов с рефрактерной глаукомой. По данным разных авторов, успех операции варьирует в широком диапазоне – от 43% до 94,4% [1–4]. Эффективность шунтирующей хирургии глаукомы во многом зависит от формирования полупроницаемой капсулы вокруг корпуса дренажных устройств, которая определяет скорость резорбции внутриглазной жидкости и, тем самым, степень снижения ВГД [5, 6]. По данным Minckler D. et al., эффективность трубчатых дренажных устройств снижается примерно на 10% в течение 1 года, и к 5 годам наблюдения имплантаты работают в 50% случаев [7].
Наряду с высоким успехом применения клапана Ahmed при хирургии глаукомы некоторые авторы [6, 8–10] отмечают довольно высокий (23–40%) процент осложнений. В научной литературе осложнения и отдаленные результаты дренажных операций при глаукоме отражены противоречиво. Дискутабельными являются вопросы возникновения побочных явлений дренажной хирургии, технических подходов и качества получаемых фильтрационных подушек на протяжении длительного периода наблюдения [2, 6, 10].
Имплантация клапана вне зависимости от сектора операции часто вызывает тяжелые осложнения, такие как отслойка сосудистой оболочки, мелкая передняя камера, транссклеральное прорезывание трубки, дислокация клапана, гипотония, диплопия, декомпенсация роговицы, катаракта, внутриглазные кровоизлияния, в ряде случаев – отслойка сетчатки, эндофтальмит [11–13].
Цель – проанализировать осложнения после имплантации клапана Ahmed в раннем и отдаленном послеоперационном периодах у пациентов с глаукомой.
Материал и методы
Под наблюдением находились 116 пациентов (121 глаз) с рефрактерной некомпенсированной глаукомой, среди них мужчин – 67 (57,8%), женщин – 49 (42,2%). Возраст пациентов – от 20 до 87 лет (в среднем 62,71±14,25 года). Все больные были с высоким риском развития интра- и послеоперационных осложнений. В 18 глазах операция проводилась на единственно зрячем глазу. В 42 (34,7%) глазах была первичная открытоугольная глаукома (ПОУГ), ранее оперированная. В остальных случаях зарегистрирована неоваскулярная глаукома на фоне посттромботической и пролиферативной диабетической ангиоретинопатии – 21 (17,4%) глаз, при артифакии – 20 (16,6%), вторичная глаукома после перенесенного хронического иридоциклита – 10 (8,4%), после травмы – 8 (6,7%), афакии – 5 (4%), силиконовой тампонады витреальной полости – 5 (4%), сквозной кератопластики – 2 (1,6%), ювенильная – 2 (1,6%), закрытоугольная глаукома – 6 (5%). У 61 (50%) пациента были предшествующие антиглаукомные операции. Сопутствующие заболевания (субкомпенсированный сахарный диабет, гипертоническая болезнь и атеросклероз) имелись у 74 (63,8%) пациентов.
К моменту операции пациенты постоянно проводили инстилляции 1–3 гипотензивных препаратов. Исходное ВГД варьировало от 26 до 57 мм рт. ст. В 14 глазах офтальмотонус из-за высоких цифр определялся пальпаторно и составлял +++. В 5 глазах ранее проводилась витрэктомия по поводу гемофтальма и выраженной диабетической пролиферативной ангиоретинопатии. Нередко показанием к применению клапана Ahmed было отсутствие успеха после антиглаукомных операций. Техника имплантации клапана и послеоперационное ведение были традиционными. Больных обследовали с помощью общепринятых клинико-офтальмологических методов, у ряда пациентов применяли оптическую когерентную томографию (ОКТ) переднего отрезка на аппарате Visante ОСТ (Carl Zeiss) для оценки зоны планируемой имплантации, а также фильтрационной подушки и местоположения клапана после операции. Непосредственные результаты хирургического лечения оценивались у всех пациентов в течение 1-го мес., в дальнейшем – по обращаемости. Срок наблюдения – с 2008 по 2015 г.
Результаты и обсуждение
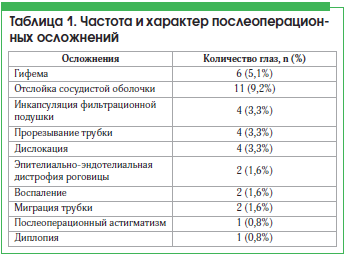
Послеоперационные осложнения в нашем исследовании установлены в 37 случаях (30,5%), что было сопоставимо с литературными данными [6, 8–10]. Частота и характер послеоперационных осложнений представлены в таблице 1. При имплантации клапана Ahmed у пациентов с неоваскулярной глаукомой появление гифемы в 6 глазах (5,2%) было связано с перепадами ВГД при вхождении в переднюю камеру и кровотечением из новообразованных сосудов рубеозно измененной радужки и угла передней камеры. Количество геморрагических осложнений значительно сократилось после предварительного наполнения передней камеры высокомолекулярным вискоэластиком, который, в свою очередь, предупреждал резкий перепад ВГД и тампонировал поврежденные новообразованные сосуды. По завершении операции вискоэластик сохраняли в полости глаза до полной самостоятельной резорбции. Основной объем вискоэластика элиминировался на 2-е сут после операции через трубку клапана, остатки резорбировались в течение 3–4 дней. Гифема уровнем 2–3 мм рассасывалась самостоятельно в течение 7–9 дней. При значительном объеме гифемы и окклюзии просвета трубки кровяным сгустком (рис. 1) проводили промывание передней камеры аспирационно-ирригационной системой факомашины на 3-й день после имплантации клапана.
В первые дни после операции в 15 случаях (12,4%) отмечали гипотонию и избыточную фильтрацию водянистой влаги. Отслойка сосудистой оболочки развилась в 11 глазах (9,1%), причем в 8 случаях (6,6%) потребовалось оперативное вмешательство. В ряде случаев наличие виско-эластика в передней камере предупреждало развитие отслойки сосудистой оболочки.
Офтальмогипертензия вследствие инкапсуляции фильтрационной подушки развилась в 4 (3,3%) случаях, причем в 1 случае это обусловило развитие диплопии. Нидлинг с введением дексаметазона и ранибизумаба с целью разрушения фиброзной капсулы и ингибирования процессов пролиферации не способствовал снижению ВГД. Пациентам проведено удаление фиброзной капсулы вокруг клапана с максимально возможным сохранением конъюнктивы. Рецидив инкапсуляции отмечен у 1 пациента, ВГД компенсировалось на усиленном медикаментозном режиме.
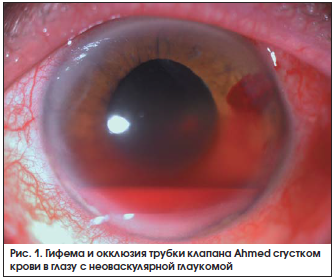
В результате эрозии собственной склеры и конъюнктивы, покрывающих клапан, в 4 случаях (3,3%) произошло обнажение трубки. В 1 случае у пациента с артифакией и силиконовой тампонадой витреальной полости произошло прорезывание трубки клапана сквозь роговицу, склеру и конъюнктиву (рис. 2). Обнажение трубки после операции происходило в сроки от 6 до 24 мес. после операции (в среднем через 15,2 мес.). Во всех случаях была попытка сохранения клапана путем пластики тканей над трубкой ауто- и алломатериалом, а также реимплантацией в другой сектор с удлинителем трубки модели ТЕ. Однако во всех случаях произошло повторное прорезывание трубки в сроки от 1 нед. до 2 мес. В связи с сохраняющимся риском развития эндофтальмита дренажные устройства были эксплантированы.
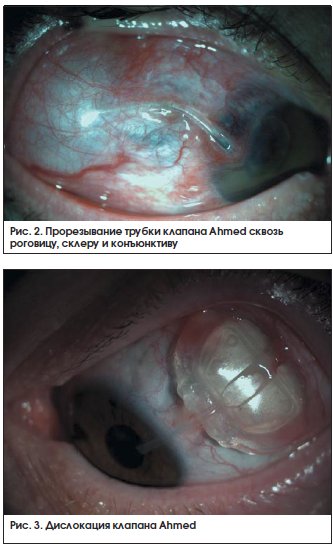
В 4 случаях (3,3%) в сроки от 2 до 5 мес. после имплантации произошла дислокация клапана Ahmed, что потребовало в дальнейшем его эксплантации (рис. 3). Несостоятельность тканей, покрывающих корпус и трубку Ahmed, вероятно, связана с дистрофическими процессами, происходящими в конъюнктиве и склере, а именно в зоне максимального напряжения и растяжения инородным телом. По данным иностранных публикаций, вероятность прорезывания трубки и дислокации клапана значительно сокращается при дополнительном покрытии поверхностного склерального лоскута донорским трансплантатом из склеры, перикарда, твердой мозговой оболочки, фасции и др. [15].
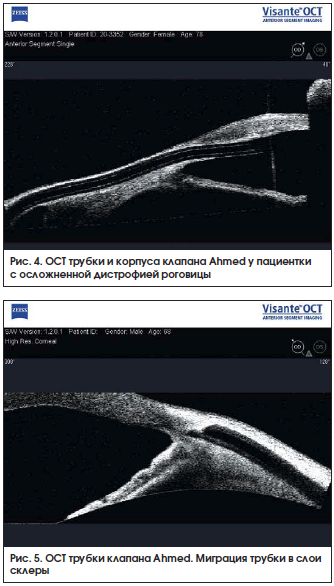
В 2 глазах (1,6%) в отдаленном послеоперационном периоде развилась эпителиально-эндотелиальная дистрофия роговицы. При биомикроскопии клапан не контактировал с роговицей, однако ОКТ переднего отрезка глаза установила контакт трубки в углу передней камеры с эндотелиальным слоем (рис. 4). В дальнейшем у 1 пациента проведена сквозная пересадка роговицы. Во втором случае из-за отсутствия зрения пациент находится под наблюдением и получает корнеопротекторное лечение.
ОКТ позволяет оценить местоположение корпуса и трубки клапана, состояние конъюнктивы и склеры пациента. Таким образом, по данным ОКТ установлена миграция трубки клапана в слои склеры в 2-х случаях спустя 12 и 18 мес. после операции (рис. 5). Вероятно, пролиферативный процесс при провисании фиксирующих швов со временем смещает корпус клапана в сторону наименьшего сопротивления. В этих случаях проведена реимплантация клапана с удлинителем трубки модели TE, ВГД компенсировано.
В 1 случае у пациента с ювенильной глаукомой наблюдали развитие индуцированного астигматизма. По данным рефрактометрии до операции была эмметропия, однако после операции пациент отметил ухудшение зрения. При оптической коррекции цилиндром величиной в 2 диоптрии зрение улучшилось с 0,2 до 0,7. У данного пациента трубка располагалась более поверхностно относительно роговицы, что привело к изменению ее кривизны.
Воспаление в раннем послеоперационном периоде в основном проявлялось в виде экссудата и фибриновой пленки в области зрачка у 2 (1,6%) пациентов и купировалось на фоне медикаментозной терапии. При блокировании клапана экссудатом выполняли лазерное разрушение воспалительных элементов в устье и внутри трубки.
Заключение. Большинство осложнений хирургического лечения рефрактерной глаукомы с имплантацией клапана Ahmed обусловлены исходно тяжелым состоянием оперируемых глаз и дистрофическими процессами в тканях, покрывающих клапан, который, как любой дренаж, является инородным телом. Несмотря на большое количество послеоперационных осложнений, имплантация клапана Ahmed зарекомендовала себя эффективным методом нормализации ВГД у пациентов с рефрактерной глаукомой.
Источник


