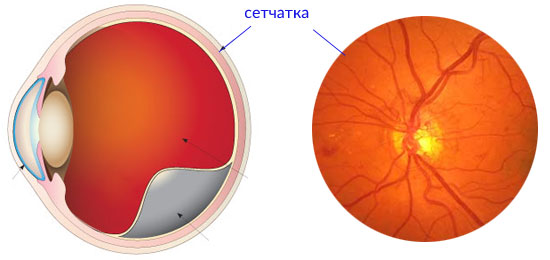
Пигментная дистрофия сетчатки германия
Дистрофия сетчатки глаза – это, строго говоря, не отдельная болезнь, а целый комплекс болезней, так или иначе представленных дегенеративным пораженим сетчатки или ее недоразвитием. Обычно дегенеративные изменения обусловлены возрастом. Старческое ухудшение зрения – из числа таких изменений. Однако офтальмологи Германии глубоко разбираются с причинами недугов зрения. Широкая клиническая практика и эпидемиологический анализ свидетельствуют о том, что, во-первых, не все виды старческих болезней глаз обусловлены дегенерацией тканей зрительного аппарата. И во-вторых, не следует исключать риск дегенерации в молодые годы, в том числе и в раннем детстве. Есть специфические заболевания (например, наследственные, связанные с изменениями в генах), при которых дистрофия сетчатки глаза развивается в молодом или совсем юном возрасте.
В любом случае требуется квалифицированное лечение, основанное на детальном выявлении причин поражения сетчатки и на выработке индивидуальных терапевтических решений по его устранению или сдерживанию. Индивидуальный подход к лечению болезней глаз – одна из сильнейших сторон в деятельности офтальмологических клиник и врачебных практик Германии.
Колбочко-палочковая недостаточность – особо распространенная дистрофия сетчатки глаза
Данный недуг распространен и среди молодых людей, возникая, как правило, к двадцатилетнему возрасту (хотя, к сожалению, не все подмечают это своевременно). Колбочко-палочковая дистрофия – отмирание в сетчатке фоторецепторов, особых клеток (в форме колбочек и палочек), преобразующих свет в нервные импульсы, направляемые в мозг.
На остроту зрения сильней всего влияет отмирание колбочек. Отмирание палочек, развивающееся обычно как следующая ступень дистрофической прогрессии, еще больше осложняет патофизиологическую картину.
Типичные симптомы:
- нистагм (дрожание глаз)
- страбизм (нарушение параллельности зрительных осей глаз, в особо выраженной форме – косоглазие)
- нарушения цветовосприятия
Диагностика в Германии преследует цель не только определить степень дистрофии сетчатки, но и выявить конкретный характер поражений: развивается ли болезненный процесс на уровне колбочек и каких именно (их три типа) или уже дошел до уровня палочек.
Специальные средства диагностики (электроретинография) позволяют справиться с этой задачей. Иногда требуется генная диагностика – для выбора правильной схемы лечения. Пациентам обычно назначают витамин А в высоких дозах. Однако если болезнь возникла из-за мутации гена ABCA4, то высокодозированная витаминная терапия противопоказана, она может еще больше нарушить зрение.
Лечение подобного рода дистрофии сетчатки глаза в Германии нередко состоит в подборе специальной защитной оптики. В принципе, это солнечные очки, но с особыми стеклами, фильтрующими по краям определенную часть спектра.
Как уже сказано, при определенных типах заболевания (но не при всех!) показан высокодозированный прием витамина А (в виде пищевых добавок).
Пигментная дистрофия
Это также весьма распространенная дистрофия сетчатки глаза.
В наследственной форме возникает рано: в детстве или юности. Прогрессия замедленная, на протяжении десятилетий – но в глубокой старости может стать причиной полной слепоты. Фоторецепторы, отмирающие при данной форме дистрофии, находятся в особо глубинном слое сетчатки, возле сети питающих сосудов. С прогрессией заболевания у пациентов развивается так называемое туннельное зрение (выпадение картинки по периферии, человек как бы смотрит в трубу).
Электроретинография – также основной вид обследований, который в Германии нередко подкрепляют генной диагностикой.
Лечение пигментной дистрофии:
- витамин А
- гипербарическая оксигенация (пребывание в барокамере, насыщенной кислородом)
Инновационные методики:
- генная терапия на основе реимплантации стволовых клеток сетчатки
- оптико-электронно-дигитальный протез (искусственная сетчатка)
Искусственную сетчатку в Германии имплантируют пациентам, у которых дистрофия сетчатки глаза развилась до стадии фактической слепоты.
Источник
Автор Вера Давыдова На чтение 7 мин. Просмотров 398 Опубликовано Вторник Август 2nd, 2016
Новое направление в зарубежной офтальмологической практике – регенерационная медицина. По утверждениям медиков, этот метод практически революционно изменяет результаты лечения пигментной дегенерации сетчатки.
Дистрофия сетчатки глаза – патология, возникающая вследствие того, что клетки сетчатки перестают выполнять требуемую функцию. Это приводит к ухудшению зрения либо полной слепоте.

Причины «отмирания» клеток часто связаны с плохим кровоснабжением, нарушением обмена веществ в зрительном анализаторе, активном росте патологических тканей.
Зарубежная медицина достигла внушительного уровня и имеет все средства для борьбы с дистрофией сетчатки глаз.
Симптомы дистрофии сетчатки глаза
- В первую очередь – снижается острота зрения. Человеку сложно воспринимать предметы в сумерках, он перестает видеть в темноте.
- Предметы словно «размываются», теряя очертания, а порой и вовсе искажаются.
- Перед глазами появляются темные пятна. Ослабевает периферическое зрение.
Эти признаки являются серьезным поводом для обращения к специалисту.
Заболевание бывает врожденным (наследственным) и приобретенным.

- Наследственная этимология заболевания имеет множество разновидностей (в зависимости от места протекания процесса, формы заболевания, типа поражения тканей и др.).
- Приобретенные заболевания возникают как следствие различных травматических явлений, после перенесенных на глазах операций, воспалительных процессов в области глаза.
Часто причиной данной болезни является наличие у пациента глаукомы или катаракты, миопии.
Актуальной проблемой в современном мире стала возрастная дистрофия сетчатки глаза. Этому процессу подвержены люди, преодолевшие шестидесятилетний порог.
Пигментная дистрофия – одна из разновидностей заболевания сетчатки глаза. Характерной особенностью является то, что она зачастую проявляется уже в раннем детстве. Страдают оба глаза одновременно. Происходит поражение пигментного эпителия (отсюда название), а также фоторецепторных клеток.
 Так видит мир человек с пигментной дистрофией
Так видит мир человек с пигментной дистрофией
На сетчатке образуются костные тельца – пигментные пятна, диск зрительного нерва атрофируется. Область зрения сужается, зрение приобретает трубочный характер.
Параллельно человек теряет возможность видеть и различать предметы в сумеречной обстановке и темноте.
Заболевание чаще носит наследственный характер, прогрессирует медленно. Но без лечения, с возрастом, приводит к потере зрения.
Современная медицина научилась решать эту проблему, помогая малышам обрести качественное визуальное восприятие. Дистрофию сетчатки глаза успешно лечит зарубежная медицина.
Почему стоит ехать за границу?
В клиниках Германии используют инновационные технологии. Одна из них – генная терапия на основе реимплантации стволовых клеток сетчатки. Также поврежденная сетчатка заменяется искусственной – вшивается оптико-электронно-дигитальный протез.

Искусственную сетчатку имплантируют в тех случаях, когда у пациента наступает полная слепота.
В Израиле, к примеру, проводятся эндоветриальные (хирургическое вмешательство осуществляется внутри глазного яблока) и экстраклеральные (операции проводятся на поверхности склеры: в местах разрыва сетчатки вшивают искусственную – экстраклеральную пломбу) операции.
Также в зарубежных клиниках используется лечение поврежденной сетчатки при помощи аргонового лазера. Именно этот метод позволил решать проблемы дистрофии сетчатки.
Принцип метода заключается в том, что луч лазера резко повышает местную температуру в очаге, белок патологической ткани свертывается, ее дальнейшее развитие останавливается.
Методы лечения дистрофии сетчатки
Основной задачей в лечении дистрофии сетчатки является необходимость разрушения патологичных клеток и сосудов, не повредив нервную ткань.

Офтальмологи для лечения заболевания применяют как медикаментозное, так и оперативное лечение.
Выбор определяется видом, стадией, прогрессированием болезни, прогнозом.
Одним из широко применяемых зарубежными специалистами методов является впрыскивание Авастина (Avastin) и Луцентиса (Lusntis). Эти препараты блокируют вещество VEGF (Vascular Endothelial Growth Factor), которое порождает быстрое размножение дефектных клеток.
Израильские офтальмологи, наряду с традиционными препаратами Авастин и Луцентис, ведут лечение препаратом нового поколения – Bevasirinad. Его эффективность заключается в том, что, воздействуя непосредственно на гены, он направлен на устранение самой причины заболевания.
Широко применяется за рубежом лазерная терапия и лазерные микрохирургические операции. Лазер облучает очаг дегенерации, локализуя процесс, и таким образом препятствует его дальнейшему развитию.

Новое направление в зарубежной офтальмологической практике – регенерационная медицина. Она применяется, в частности, в лечении приобретенных патологий. По утверждениям медиков, этот метод практически революционно изменяет результаты лечения пигментной дегенерации сетчатки.
Это происходит в результате активизации восстановительных процессов в поврежденной сетчатке глаза у пациентов, перенесших травмы или операции на зрительном анализаторе. Быстро регенерируют нервные ткани и сосуды.
[adsp-pro-3]
Зарубежные клиники
Германия
Глазная клиника в Карлсруэ — одна из самых известных зарубежных офтальмологических клиник. Именно здесь впервые была проведена операция по вживлению искусственной сетчатки. Это система Argus II, преобразующая изображение с миниатюрной видеокамеры в нервные сигналы, поступающие в зрительный центр мозга.
Уникальная система протезирования сетчатки и единственная возможность вернуть зрение больным с пигментной ретинопатией.
Глазная клиника Артемис в городе Франкфурт-на-Майне
Одна из современнейших офтальмологических лечебниц, оснащена самой передовой аппаратурой. Специалисты высокого класса имеют большой опыт по проведению операций с применением лазерных технологий. Здесь представляется полный спектр рефракционной хирургии.
В городе Кёльн – глазная клиника Ам Ноймаркт
Применяются методы щадящей хирургии, в частности лазерная хирургия. Пациенты выбирают клинику за применение надежного, точного и безопасного метода Femto-LASIK. В ней лечат практически все глазные патологии.
Стоимость операций варьируется в зависимости от вида заболевания, а также от того – один или оба глаза подлежат оперативному вмешательству. В среднем она составляет 4-7 тысяч евро.
Клиники Германии охотно принимают иностранных пациентов. Организовать поездку можно минимум двумя способами.
- Первый – самостоятельно. Для этого потребуется знание немецкого или английского языков, так как в клинике может не быть русскоговорящего специалиста. Можно решить вопрос с переводчиком, но это значительно удорожит пребывание. Первичные переговоры ведутся заочно (по телефону, электронной почте, через интерактивные приемы сайта, если таковые имеются). Далее клиника высылает приглашение. Пациент самостоятельно оформляет визовые документы и пребывает в Германию. В аэропорту по договоренности его встретит представитель клиники. Однако можно добраться и самостоятельно.
- Второй вариант: пациент обращается в специализированное агентство, например, WP German Med CARE AG. Здесь помогут и подобрать профильную клинику и всю процедуру оформления документов, прибытия и поступления в клинику берут на себя консультанты. Достаточно заключить договор и оплатить стоимость пакета услуг. У пациента не возникнет проблем с трансфертом и языковым барьером.
Аэропорты прибытия в вышеперечисленные клиники:
- Клиника в Карлсруэ – аэропорт Штутгарт, г. Штутгарт
- Артемис – аэропорт Франкфурт-на-Майне
- Ам Ноймаркт – аэропорт Кёльн-Бонн, г. Кёльн
Израиль
Топ Клиника Ассута
Здесь практикуют известные в Израиле офтальмологи хирурги. Широко применяется щадящая лазерная микрохирургия сетчатки глаза.
 Фото клиники
Фото клиники
В частности, успешно осуществляется экстрасклеральное пломбирование, показывающие положительные результаты. В случаях, когда пациенту не показан данный вид операции (например, при изменении стекловидного тела), специалисты делают операцию внутри глаза: стекловидное тело извлекается и с помощью силиконового масла или специального газа прижимается сетчатка. Операции проводятся под микроскопом.
В настоящий момент зарубежные офтальмологи испытывают новейший метод – имплантацию искусственной сетчатки Nano Retina. Это устройство преобразует свет в электрический импульс (как это делает природная сетчатка) с помощью специальных очков, которые надевает пациент.
Медицинский центр Ихилов
(Тель-Авивский медицинский центр им. Сураски).
Центром получены хорошие практические результаты в использовании лазерных микрохирургических операций. Применяется комплексное лечение: оперативное и медикаментозное.
Стоимость лечения в израильских клиниках зависит от уровня лечащего врача и уровня самой клиники. В большинстве клиник цены официально утверждены министерством Здравоохранения Израиля. Обратившись на официальный сайт любой из клиник с запросом по цене, как правило, в течение часа пациент получит ответ.
Первая консультация обычно бесплатна. Далее потенциальный пациент попадает под сопровождение консультанта международного отдела клиники. Он изучает представленную медицинскую документацию, составляет план лечения, рассчитывает стоимость.
Если нужна помощь в приобретении билетов, бронирования гостиницы, подключается специалист туристического отдела (во многих клиниках он есть) либо консультант по сопровождению иностранных пациентов.
Самолеты из России в Израиль пребывают в аэропорт Бен-Гурион Тель-Авива. Пациента встречает представитель лечащей стороны, сопровождает в гостиницу, информирует о дальнейшем плане.
Проблем с языком нет – все представители клиник, работающие с россиянами, говорят на русском языке.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 16 марта 2018;
проверки требуют 13 правок.
Пигментный ретинит (RP) — наследственное, дегенеративное заболевание глаз, которое вызывает сильное ухудшение зрения и часто слепоту[1]. Прогрессирование RP не является последовательным. Некоторые люди могут иметь симптомы с детства, другие могут заметить симптомы позднее[2]. В общем, чем позже начало, тем быстрее ухудшение зрения. Те, кто не имеет RP, имеют 90-градусное периферийное зрение, в то время как люди, имеющие RP, имеют периферийное зрение менее 90 градусов.
Как форма дистрофии сетчатки, RP вызвана аномалиями фоторецепторов (палочек и колбочек) или пигментного эпителия сетчатки (ПЭС) , ведущими к прогрессирующей потере зрения. Пострадавшие люди могут испытывать дефектную адаптацию от светлого к тёмному, от тёмного к светлому или никталопию (ночную слепоту), в результате дегенерации периферического поля зрения (так называемое туннельное зрение). Иногда раньше теряется центральное зрение, вынуждая человека смотреть искоса на объекты.
Эффект RP лучше всего иллюстрируется сравнением с экраном телевизора или компьютера. Светящиеся пикселы, формирующие изображение на экране можно приравнять к миллионам световых рецепторов на сетчатке глаза. Чем меньше пикселей на экране, тем менее отчётливо будет отображаться изображение. Менее 10 процентов фоторецепторов в глазе способны воспринимать цвет, при высокой интенсивности света в условиях яркого освещения или дневного света. Эти рецепторы расположены в центре круга сетчатки. Остальные 90 процентов фоторецепторов получают серую шкалу при низкой интенсивности света, используются при низкой освещённости и ночном видении и расположены по периферии сетчатки. RP разрушает световые рецепторы снаружи внутрь, от центра к краю, или по спорадическим путям с соответствующим снижением эффективности зрения. Это вырождение является прогрессирующим и не имеет никакого известного лечения.
Признаки и симптомы[править | править код]
Тот же вид с туннельным зрением от пигментного ретинита. Чернота вокруг центра изображения указывает не на тьму, а на отсутствие визуальной информации.
RP характеризуется прогрессирующей потерей фоторецепторов и в конечном итоге может привести к слепоте[3]. У людей могут возникнуть один или несколько следующих симптомов:
- Ночная слепота или никталопия;
- Туннельное зрение (отсутствует периферийное зрение);
- Периферийное зрение (отсутствует центральное зрение);
- Сеточное зрение;
- Антипатия к яркому свету;
- Медленная регулировка от темного к светлому, и наоборот;
- Нечеткость зрения;
- Плохое различение цветов;
- Крайняя усталость.
Ассоциированные условия[править | править код]
RP может быть:
(1) несиндромальной, то есть, это происходит в одиночку, без каких-либо других клинических данных,
(2) Синдромный с другими нейросенсорными расстройствами, нарушениями развития или сложными клиническими данными, или
(3) Вторичным к другим системным заболевания[4].
- RP в сочетании с глухотой (врождённой или прогрессирующей) называется синдромом Ушера.
- RP в сочетании с офтальмоплегией, дисфагией, атаксией, и пороками сердца, видимыми как митихондриальным DNA нарушением — Синдром Барде — Бидля (также известный как рваная красная волоконная миопатия)
- RP в сочетании с отсталостью, периферической невропатией, акантозными (с шипами) эритроцитами, атаксией, стеатореей, указывает на недостаток ЛПОНП, видимо из-за абеталипопротеинемии.
- RP с клинически видимым сочетанием с рядом других редких генетических заболеваний (в том числе мышечной дистрофией и хронической гранулематозной болезнью) как часть синдрома Маклеода. Это X-хромосомный рецессивный фенотип характеризуется полным отсутствием поверхностных XK-клеточных белков, и поэтому указывает на снижение экспрессии всех красных кровяных клеток келл-антигенов. Для целей переливания эти пациенты считаются полностью несовместимы со всеми нормальными и К0 / К0 донорами.
- RP, связанные с гипогонадизмом, и задержкой развития с аутосомно-рецессивным типом наследования, по-видимому с синдромом Лоуренс-Луна-Барде-Biedl
Другие условия включают в себя нейросифилис, токсоплазмоз ( Emedicine «Retinitis Pigmentosa») и синдром Рефсума.
Генетика[править | править код]
Пигментный ретинит (RP) является одним из наиболее распространённых форм наследственной дегенерации сетчатки[5]. Существуют различные гены, которые, будучи мутированы, способны привести к фенотипу пигментного ретинита[6]. В 1989, мутаций в гене родопсина, пигмент, который играет существенную роль в визуальной фототрансдукции в условиях низкой освещённости, выявлено не было. С тех пор, более 100 мутаций были обнаружены в этом гене, что составляет 15% от всех видов дегенерации сетчатки. Большинство из этих мутаций миссенс-мутации и наследуются в основном в доминирующей манере.
Типы включают в себя:
| OMIM | Ген | Тип |
|---|---|---|
| 180100 | RP1 | Пигментный ретинит-1 |
| 312600 | RP2 | Пигментный ретинит-2 |
| 300029 | RPGR | Пигментный ретинит-3 |
| 608133 | PRPH2 | Пигментный ретинит-7 |
| 180104 | RP9 | Пигментный ретинит-9 |
| 180105 | IMPDH1 | Пигментный ретинит-10 |
| 600138 | PRPF31 | Пигментный ретинит-11 |
| 600105 | CRB1 | Пигментный ретинит-12, аутосомно-рецессивный |
| 600059 | PRPF8 | Пигментный ретинит-13 |
| 600132 | TULP1 | Пигментный ретинит-14 |
| 600852 | CA4 | Пигментный ретинит-17 |
| 601414 | HPRPF3 | Пигментный ретинит-18 |
| 601718 | ABCA4 | Пигментный ретинит-19 |
| 602772 | EYS | Пигментный ретинит-25 |
| 608380 | CERKL | Пигментный ретинит-26 |
| 607921 | FSCN2 | Пигментный ретинит-30 |
| 609923 | TOPORS | Пигментный ретинит-31 |
| 610359 | SNRNP200 | Пигментный ретинит 33 |
| 610282 | SEMA4A | Пигментный ретинит-35 |
| 610599 | PRCD | Пигментный ретинит-36 |
| 611131 | NR2E3 | Пигментный ретинит-37 |
| 268000 | MERTK | Пигментный ретинит-38 |
| 268000 | USH2A | Пигментный ретинит-39 |
| 612095 | PROM1 | Пигментный ретинит-41 |
| 612943 | KLHL7 | Пигментный ретинит-42 |
| 268000 | CNGB1 | Пигментный ретинит-45 |
| 613194 | BEST1 | Пигментный ретинит-50 |
| 613464 | TTC8 | Пигментный ретинит 51 |
| 613428 | C2orf71 | Пигментный ретинит 54 |
| 613575 | ARL6 | Пигментный ретинит 55 |
| 613617 | ZNF513 | Пигментный ретинит 58 |
| 613861 | DHDDS | Пигментный ретинит 59 |
| 613194 | BEST1 | Пигментный ретинит, концентрический |
| 608133 | PRPH2 | Пигментный ретинит, дигенический |
| 613341 | LRAT | Пигментный ретинит, ювенильный |
| 268000 | SPATA7 | Пигментный ретинит, ювенильный, аутосомно-рецессивный |
| 268000 | CRX | Пигментный ретинит, запоздалый доминирующий |
| 300455 | RPGR | Пигментный ретинит, X-хромосомный, с синореспираторной инфекцией, с глухотой или без неё |
Ген родопсина кодирует главный белок наружных сегментов фоторецепторов. Исследования показывают, что мутации в этом гене ответственны примерно за 25% аутосомно-доминантных форм RP[5][7].
Мутации в четырёх пре-мРНК факторах сплайсинга как известно, вызывают аутосомно-доминантный пигментный ретинит. Это PRPF3 (человек с PRPF3 является с HPRPF3, а также с PRP3), PRPF8 , PRPF31 и PAP1 . Эти факторы экспрессируются повсеместно, и предполагается, что дефекты в повсеместном факторе (белок, экспрессируемый повсеместно) должны вызывать заболевание только в сетчатке, так как клетки фоторецепторов сетчатки имеют гораздо большую потребность в обработке белка (родопсина), чем любой другой тип клеток.
О свыше 150 мутациях, зарегистрированных на сегодняшний день в гене опсина, связанного с RP мутацией Pro23His в интрадискальном домене белка впервые было сообщено в 1990 году. Эти мутации встречаются по всему гена опсина и распределяются по трём областям белка (внутридисковому, трансмембранному и цитоплазматическому доменам). Одной из основных биохимических причин RP в случае мутаций белка родопсина является фолдинг белка и молекулярные шапероны.[8] Было обнаружено, что мутация кодона 23 в гене родопсина, в котором пролин преобразуется в гистидин, приходится наибольшая доля мутаций родопсина в Соединённых Штатах. Ряд других исследований сообщили о других мутациях, которые также коррелируют с болезнью. Эти мутации включают Thr58Arg, Pro347Leu, Pro347Ser, а также удаление Ile-255[7][9][10][11][12]. В 2000 году сообщалось о редкой мутации в кодоне 23 вызывающей аутосомно-доминантный пигментный ретинит, в которой пролин изменялся на аланин. Тем не менее, это исследование показало, что дистрофии сетчатки, связанная с этой мутацией была характерна мягкая форма и течение. Кроме того, тем более сохранено в электроретинографии амплитуд, чем более преобладала мутация Pro23His[13].
Патофизиология[править | править код]
Опыты на животных показывают, что пигментный эпителий неудачно фагоцитирует потерянные палочки внешнего сегмента диска, что ведёт к накоплению мусора из палочек внешнего сегмента. У мышей с гомозиготно-рецессивной дегенеративной мутацией сетчатки палочки фоторецепторов прекращают развитие и подвергаются дегенерации до завершения созревания клеток. Также присутствует дефект цГМФ-фосфодиэстеразы; это приводит к токсичным уровням цГМФ.
Симптомы[править | править код]
Пигментный ретинит (как правило, называют «RP») является заболеванием, которое характеризуется потерей светочувствительных клеток фоторецепторов, расположенных в задней части глаза, как плёнка в камере. Обычно палочки фоторецепторов (ответственные за ночное зрение) поражаются первыми, поэтому потеря ночного зрения (никталопия), является как правило, первым симптомом. Дневное зрение (при посредничестве колбочек) обычно сохраняется до поздних стадий заболевания. Пятнистость пигментного эпителия сетчатки с чёрной боне-спикулярной пигментацией (или патогномоничный симптом, как правило, указывает из пигментный ретинит. Другие глазные функции включают в себя паллор головки зрительного нерва, ослабление (истончение) сосудов сетчатки, целлофановую макулопатию, кистозный макулярный отёк и заднюю субкапсулярную катаракту.
Диагностика[править | править код]
Диагноз пигментного ретинита опирается на документацию прогрессирующей потери функций клеток фоторецепторов посредством электроретинографии (ЭРГ) и визуального тестирования поля.
Режим наследования RP определяется историей семьи. По крайней мере, 35 различных генов или локусов, как известно, вызывают «несиндромальный RP» (RP, не являющийся результатом другого заболевания или частью более широкого синдрома).
ДНК-тестирование доступно на клинической основе для:
- RLBP1 (аутосомно-рецессивный, тип Bothnia RP)
- RP1 (аутосомно-доминантный, RP1)
- RHO (аутосомно-доминантный, RP4)
- RDS (аутосомно-доминантный, RP7)
- PRPF8 (аутосомно-доминантный, RP13)
- PRPF3 (аутосомно-доминантный, RP18)
- CRB1 (аутосомно-рецессивный, RP12)
- ABCA4 (аутосомно-рецессивный, RP19)
- RPE65 (аутосомно-рецессивный, RP20)
Для всех других генов (например, DHDDS), молекулярное генетическое тестирование доступно только на исследовательской основе.
RP может быть унаследован аутосомно-доминантным, аутосомно-рецессивным, или Х-хромосомым образом. Х-хромосомный RP может быть или рецессивный, затрагивающий в первую очередь только мужчин, или доминирующий, затрагивающие как мужчин, так и женщин, хотя на мужчин, как правило, более мягко влияет. Некоторые дигенические (контролируемые двумя генами) и митохондриальные формы были также описаны.
Генетическое консультирование зависит от точного диагноза, определения типа наследования в каждой семье, и результатов молекулярно-генетического тестирования.
Лечение[править | править код]
В настоящее время нет лекарств от пигментного ретинита, но лечение, теперь доступно в некоторых странах. Прогрессирование заболевания может быть снижено за счёт ежедневного потребления 15000 МЕ (соответствует 4,5 мг) витамина А пальмитата у некоторых пациентов[14]. Последние исследования показали, что правильные витаминные добавки могут отсрочить слепоту до 10 лет (за счёт снижение годовых потерь с 10% до 8,3%) у некоторых пациентов в определённых стадиях заболевания[15]., Получивший признание на рынке, в феврале 2011 года, протез сетчатки Argus стал первым одобренным средством для лечения этого заболевания, доступен в Германии, Франции, Италии и Великобритании. Операция протезирования здесь описана. Промежуточные результаты долгосрочных исследований 30 пациентов были опубликованы в 2012 году[16].
Имплантат сетчатки Argus II также получил разрешение для экспериментального использования в США.[17][18][19] Устройство может помочь взрослым с RP, которые потеряли способность воспринимать формы и движения, чтобы быть более мобильными и выполнять ежедневные мероприятия. В июне 2013 года 12 больниц в США объявили в ближайшее время начать консультации для пациентов с RP в рамках подготовки к запуску Argus II в том же году[20].
Исследования[править | править код]
Лечение в будущем может включать трансплантацию сетчатки, искусственные имплантаты сетчатки[21], генную терапию, стволовые клетки, пищевые добавки, и / или лекарственную терапию.
2006: Стволовые клетки: Исследователи Великобритании, работающие с мышами, пересаживали мышам стволовые клетки уже на продвинутой стадии развития, и уже программировали развитие клеток фоторецепторов мышей, которые были генетически индуцированны, чтобы имитировать человеческие условия пигментного ретинита и возрасто-зависимую дегенерацию жёлтого пятна. Эти фоторецепторы развились и сделали необходимые нервные связи в сетчатке глаза животного, ключевой шаг в восстановлении зрения. Ранее считалось, что зрелая сетчатка не имеет регенеративной способности. Это исследование может в будущем привести к использованию пересадки на людях, чтобы облегчить слепоту[22].
2008: Учёные Биологического научного института Осака выявили белок, названный Пикачурин, который, по их мнению, может привести к лечению пигментного ретинита [23][24]
2010: Доступная генная терапия, кажется, работает на мышах[1].
2010: R-Tech Ueno (японский медицинское производственное предприятие) завершает вторую фазу клинических исследований офтальмологического раствора UF-021 (название продукта Ocuseva (TM)) для пигментного ретинита.
2012: Учёные из Медицинского центра Колумбийского университета показали, на животной модели, что генная терапия и терапия индуцированных плюрипотентных стволовых клеток могут быть жизнеспособными вариантами для лечения пигментного ретинита в будущем[25].
2012: Учёные из Университета Майами института глаза Баском Палмер представили данные, показывающие защиту фоторецепторов в животной модели, когда в глаза были введены мезенцефалические астроциты нейротрофического фактора (MANF)[26].
2014: исследование, проведённое в Университете Аликанте в Испании показали, что каннабиноиды из марихуаны могут замедлить потерю зрения в случаях пигментного ретинита[27].
Исследователи из Университета Беркли Калифорния, смогли восстановить зрение слепым мышам, эксплуатируя «photoswitch», который активизирует ганглиозные клетки сетчатки в образце с повреждёнными клетками палочек и колбочек[28].
2019: Ученые из Офтальмологического института Вилмера, Медицинской школы университета имени Джона Хопкинса и компании MD 3Nacuity Pharmaceuticals объявили о том, что исследовательский принимаемый во внутрь препарат N-ацетилцистеин (N-acetylcysteine) улучшает функционирование фоторецепторов-колбочек сетчатки глаза у пациентов с пигментным ретинитом.
Известные случаи[править | править код]
- Деррик Морган, ямайский ска, рокстеди и регги — музыкант.
- Нил Fachie, британский паралимпийский велосипедист. [29]
- Линди Хоу, австралийский тандем-велосипедист и пловец [30]
- Джон Уэллнер, американский актёр [31]
- Стив Уинн, американский бизнес-магнат и разработчик казино в Лас-Вегасе [32]
- Рэйчел Leahcar, австралийская певица
- Вилли Браун, бывший мэр Сан-Франциско
- Стив Лонеган, мэр Боготы, Нью-Джерси, Республиканский кандидат в Сенат США
- Аманда Своффорд, американская модель[33]
- Ричард Бернштейн, Мичиган судья Верховного суда.
- Ян Трехерн, британский фотограф.
- Мэтью Бентон, суперзвезда кабаре и владелец / управляющий директор / художественный руководитель танцоров Мэтью Бентон.
- Молли Бёрк, мотивационный спикер, блогер.
Примечания[править | править код]
- ↑ 1 2 Genetic Reactivation of Cone Photoreceptors Restores Visual Responses in Retinitis pigmentosa.
- ↑ Koenekoop, R.K.; Loyer, Magali; Hand, Collette K; Al Mahdi, Huda; Dembinska, Olga; Beneish, Raquel; Racine, Julie; Rouleau, Guy A. Novel RPGR mutations with distinct retinitis pigmentosa phenotypes in French-Canadian families (англ.) // American Journal of Ophthalmology (англ.)русск. : journal. — 2003. — Vol. 136, no. 4. — P. 678—668. — doi:10.1016/S0002-9394 (03)00331-3.
- ↑ Farrar G.J., Kenna P.F., Humphries P. On the genetics of retinitis pigmentosa and on mutation-independent approaches to therapeutic intervention (англ.) // The EMBO Journal (англ.)русск. : journal. — 2002. — March (vol. 21, no. 5). — P. 857—864. — doi:10.1093/emboj/21.5.857. — PMID 11867514.
- ↑ Daiger SP, Sullivan LS, Bowne SJ. Genes and mutations causing retinitis pigmentosa.
Clin Genet 2013: 84: 132–141. - ↑ 1 2 Hartong D.T., Berson E.L., Dryja T.P. Retinitis pigmentosa (англ.) // The Lancet. — Elsevier, 2006. — November (vol. 368, no. 9549). — P. 1795—1809. — doi:10.1016/S0140-6736 (06)69740-7. — PMID 17113430.
- ↑ OMIM 268000
- ↑ 1 2 Berson E.L., Rosner B., Sandberg M.A., Dryja T.P. Ocular findings in patients with autosomal dominant retinitis pigmentosa and a rhodopsin gene defect (Pro-23-His) (англ.) // JAMA Ophthalmology (англ.)русск. : journal. — 1991. — January (vol. 109, no. 1). — P. 92—101. — doi:10.1001/archopht.1991.01080010094039. — PMID 1987956.
- ↑ Senin I.I., Bosch L., Ramon E., et al. Ca2+/recoverin dependent regulation of phosphorylation of the rhodopsin mutant R135L associated with retinitis pigmentosa (англ.) // Biochemical and Biophysical Research Communications (англ.)русск. : journal. — 2006. — October (vol. 349, no. 1). — P. 345—352. — doi:10.1016/j.bbrc.2006.08.048. — PMID 16934219.
- ↑ Dryja T.P., McGee T.L., Reichel E., et al. A point mutation of the rhodopsin gene in one form of retinitis pigmentosa (англ.) // Nature : journal. — 1990. — January (vol. 343, no. 6256). — P. 364—366. — doi:10.1038/343364a0. — PMID 2137202.
- ↑ Dryja T.P., McGee T.L., Hahn L.B., et al. Mutations within the rhodopsin gene in patients with autosomal dominant retinitis pigmentosa (англ.) // The New England Journal of Medicine : journal. — 1990. — November (vol. 323, no. 19). — P. 1302—1307. — doi:10.1056/NEJM199011083231903. — PMID 2215617.
- ↑ Berson E.L., Rosner B., Sandberg M.A., Weigel-DiFranco C., Dryja T.P. Ocular findings in patients with autosomal dominant retinitis pigmentosa and rhodopsin, proline-347-leucine (англ.) // American Journal of Ophthalmology (англ.)русск. : journal. — 1991. — May (vol. 111, no. 5). — P. 614—623. — PMID 2021172.
- ↑ Inglehearn C.F., Bashir R., Lester D.H., Jay M., Bird A.C., Bhattacharya S.S. A 3-bp deletion in the rhodopsin gene in a family with autosomal dominant retinitis pigmentosa (англ.) // American Journal of Human Genetics (англ.)русск. : journal. — 1991. — January (vol. 48, no. 1). — P. 26—30. — PMID 1985460.
- ↑ Oh, Kean T.; Weleber, RG; Lotery, A; Oh, DM; Billingslea, AM; Stone, E.M. Description of a New Mutation in Rhodopsin, Pro23Ala, and Comparison With Electroretinographic and Clinical Characteristics of the