Пересадка сетчатки из стволовых клеток
Глаза являются важным и значимым органом в жизни каждого человека. С их помощью получается спокойно жить в окружающем мире, осуществлять различные действия. Но под воздействием внешних раздражителей, качество зрения ухудшается. К сожалению, не все недуги, связанные с глазами, возможно излечить с помощью медикаментов. В запущенных случаях обойтись без операции невозможно.
Хирургическое вмешательство способно спасти положение, решить появившиеся проблемы и восстановить зрение. А позднее обращение к специалисту, может спровоцировать полную слепоту.
Замена сетчатки глаза в России с 2017 года не является новостью. В процессе процедуры, осуществляется пересадка сетчатки, что значительно повышает качество зрения. Данная операция обладает рядом особенностей, о которых необходимо знать каждому, кто на нее решился.
Первая пересадка сетчатки глаза
Первая трансплантация сетчатки была проведена японскими исследователями. Им удалось вырастить из стволовых клеток функционирующие клетки сетчатки и имплантировать их слепым мышам, после чего зрение было частично восстановлено.
Ученые центра Riken в японском городе Кобе исследовали эмбриональные стволовые клетки мышей, чтобы сформировать так называемые глазные чашки, примитивную структуру глаза. Внутри глазного стакана образуется сетчатка, на которой находятся фоторецепторы, позволяющие видеть. Снаружи образуется так называемый ретинальный пигментный эпителий (RPE), который позже в глазу образует границу с сосудистой оболочкой. У человеческого эмбриона глазные кружки видны примерно на шестой неделе.
Показания
Хирургическое вмешательство необходимо только в определенных случаях. Перед тем, как приступать к нему, пациент должен пройти полное обследование. Это необходимо для того, чтобы поставить точный диагноз и оценить степень повреждения сетчатки. Операция по пересадке сетчатки глаза необходима в следующих ситуациях:
- Когда на сетчатке наблюдаются отчетливые рубцы, после травмы или сильного удара.
- Если начался процесс деформации.
- При наличии воспаления.
- Если наблюдается дистрофия.
- Если пациент получил химический ожог, в результате чего глаз был поврежден.
- При наличии различных грибков и паразитов, оказывающих негативное воздействие на глаза.
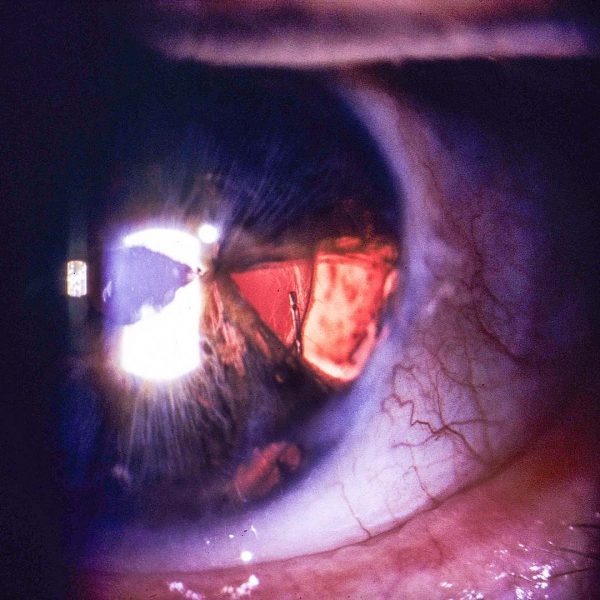
Травма глаза
В запущенных случаях, когда в глазах уже начались необратимые изменения, исправить положение возможно с помощью трансплантации сетчатки глаза. Подобная операция активно практикуется отечественными специалистами. Эта операция осуществляется в следующих случаях:
- Когда происходит серьезное повреждение, вплоть до отмирания отдельных клеток. Подобное наблюдается при дистрофии желтого тела.
- Когда в сетчатке нарушается кровообращение, что происходит в результате макулодистрофии.
- Когда на глазах образуется опухоль.
- Когда начинается процесс отслаивания сетчатки.
Трансплантация способна помочь даже в запущенных ситуациях и является единственным шансом человека сохранить зрение. Важно обращаться к врачу с появлением первых признаков болезни. Опытные специалисты способны сохранить зрение даже в тяжелых ситуациях. Но перед началом такой тяжелой и сложной операции, необходимо пройти ряд важных обследований. К ним относятся следующие:
- Проконсультироваться у офтальмолога.
- Сдать кровь на анализ.
- Пройти процедуру биомикроскопии.
- Пройти процедуру компьютерной кератографии.
- Пройти обследование глазного дна.
Отзывы на операцию по пересадке искусственной сетчатки для незрячих в целом положительные. В большинстве случаев удалось частично или полностью восстановить зрение. Отечественные врачи начинают активно практиковать данную операцию.
Тонкости операции
Операция по замене сетчатки глаза производится различными способами. Обычно она производится с помощью специализированного протеза.
Первый вариант считается настоящим прорывом в медицине, ведь с его помощью удалось многого достичь. После того как в практике начали активно использовать протезы, большее количество пациентов получили возможность вернуть зрение и излечиться. Если в прошлом необходимо было ждать в очереди, пока не появится донор, то теперь эта проблема нашла свое решение.
Поврежденный участок необходимо удалить. Это делается при помощи специального лазера. Он действует точно и аккуратно, удаляет только мертвые клетки, не задевая живые. Объем удаляемой ткани зависит от степени тяжести случая и необходимости. Этот факт также определяет финальную стоимость операции.
Как проводится операция?
Перед началом хирургического вмешательства в обязательном порядке проводится анестезия. Операцию возможно проводить под местным или общим обезболиванием. Протез фиксируется на глазу при помощи саморассасывающихся нитей. В конце операции, пациенту вводятся противовоспалительные препараты.
В качестве реабилитации и восстановления после осуществления операции, пациенту назначается курс препаратов, необходимых для поддержания здоровья. Также необходимо носить очки и линзы. После проведения операции пациент должен бережно относиться к своему зрению, беречь себя от прямого воздействия солнечных лучшей и прочих внешних факторов, способных навредить глазам.
Преимущества операции
Заболевания сетчатки и ее повреждения, являются первой причиной возникновения слепоты. Но даже при серьезных повреждения, зрительный нерв может сохранять свою работоспособность, что дает шанс на восстановление зрения. Если сохранены нервные окончания глазного яблока, специалисты могут воспользоваться этим фактором, чтобы осуществить хирургическое вмешательство.
С помощью операции, можно не только улучшить зрение человека, но и даже вернуть способность видеть незрячим. Ученые проводят активные исследования на слепых мышах, чтобы однажды подарить всем людям, потерявшим зрение, шанс вновь увидеть мир.
Ожидаемые новшества
Наука не стоит на месте и ученые активно применяют новые методы в своих опытах, чтобы использовать их на практике. На данный момент активно изучается лечение стволовыми клетками, с помощью которых возможно серьезно повлиять на ситуацию. С помощью стволовых клеток планируется найти путь к регенерации, что поможет быстро устранять повреждения сетчатки глаза. В случае успеха, это может стать полноценной заменой пересадке.
Сетчатка является легким объектом для опытов, что позволяет специалистам делать новые открытия. Несмотря на свое сложное строение, он всегда доступен, содержит однотипные клетки, благодаря чему осуществлять опыты с глазом гораздо проще, чем с любым другим органом.
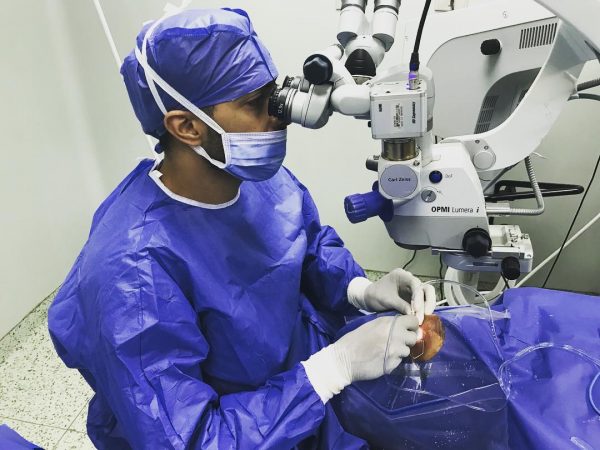
Операция по пересадке сетчатки глаза
К тому же глаз небольшой орган, а значит для проведения опытов и будущей операции, потребуется небольшое число стволовых клеток. Это значительно облегчает задачу и в будущем позволит оперировать большое количество пациентов. При доставлении клеток к месту, где наблюдается патология, риск отторжения сводится к минимальным показателям. К тому же существует множество устройств и изобретений, созданных специально для того, чтобы регулировать все процессы, происходящие в человеческом глазу.
Несмотря на тот факт, что в исследованиях есть определенные сдвиги и продвижения, использовать эту методику в ближайшее время не будут. Это объясняется степенью риска и количеством вопросов, на которых еще нет ответа. В результате развития болезни, клетки могут не прижиться, что чревато негативными последствиями.
Пересадка сетчатки глаза в России
На данный этап времени, пересадка сетчатки доступна в России. Человек, потерявший зрение или испытывающий серьезные трудности, может рассчитывать на долгожданное восстановление способность видеть. Операции по восстановлению зрения, в случае проблем с сетчаткой, активно практикуются в России. В 2017 году впервые в РФ была проведена успешная операция по имплантации бионической сетчатки глаза. Любой желающий может обратиться в медицинский центр, чтобы получить консультацию и соответствующую помощь.
Одной из главных причин, которая становится причиной консультации и операции, считается отслоение сетчатки. Это сложное заболевание, которое требует немедленного вмешательства специалистов. В этом случае необходимо прикрепить сетчатку обратно к глазу. При этом очень важно провести операцию быстро, пока ситуация не слишком серьезная. В противном случае можно полностью потерять зрение, без возможности на восстановление.
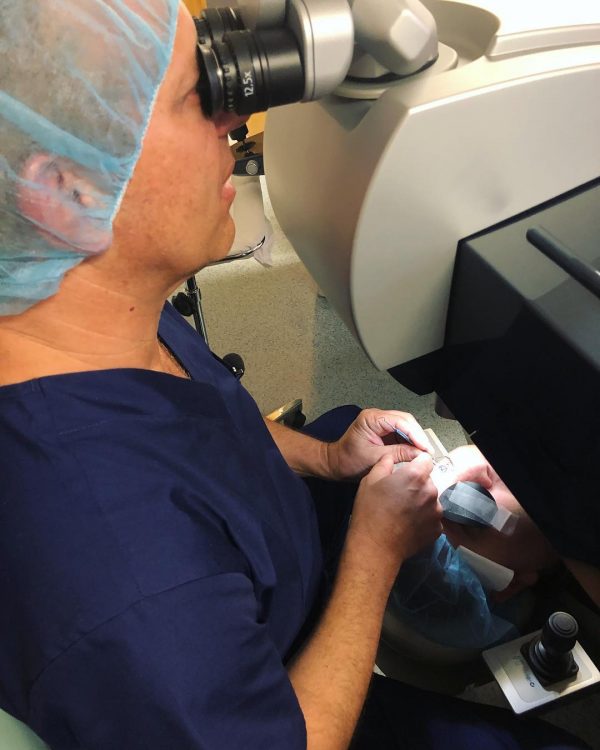
Последнее время в России активно внедряется методика по трансплантации сетчатки глаза. После осуществления ряда исследований и опытов, были достигнуты успехи, что позволило применять методику на пациентах. Общая цена операции может обойтись пациентам примерно в 90 тысяч рублей или больше, зависимости от степени повреждения. Финальная цена выясняется после полного обследования.
Также стоимость операции напрямую зависит от опыта врача и престижности клиники, где будет осуществляться хирургическое вмешательство. Как правило, в хороших клиниках цена намного выше, но и операции проводятся более успешно и качественно. Отечественные хирурги практикуют два метода по трансплантации сетчатки.
- При эстрасксеральном методе, все действия производятся исключительно на поверхности глаза.
- При эндовитреальном методе, все действия производятся исключительно внутри глаза.
Серьезный прорыв в медицине и технологический прогресс, открывают перед людьми большие возможности. Сегодня у человечества появилась возможность вернуть зрение, даже при серьезных проблемах с глазами. Однако помощь возможна лишь при своевременном обращении к врачу. Халатность к собственному здоровью и нежелание посещать клинику, может стать причиной необратимых последствий и полной потери зрения.
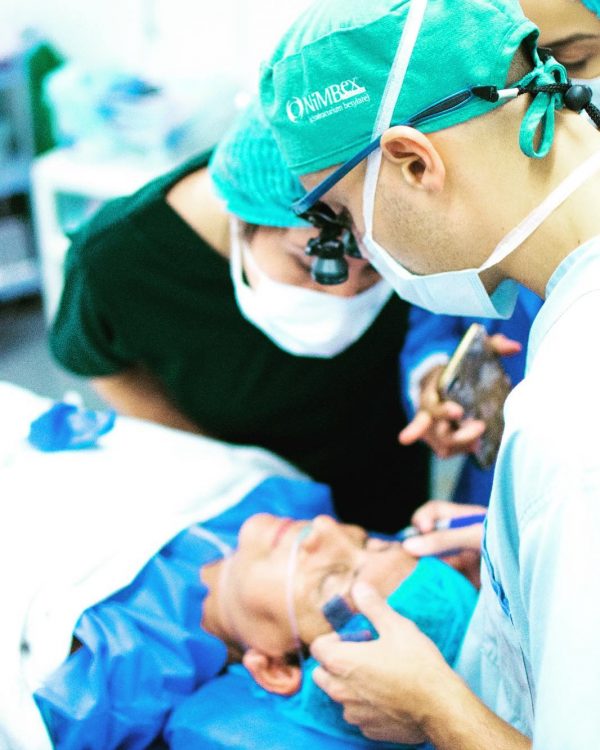
Трансплантация сетчатки глаза
Отслоение сетчатки и прочие проблемы, связанные с ней – это серьезная патология, требующая немедленного лечения. При верном медицинском лечении, можно добиться улучшений и полного восстановления зрения.
По этой причине важно уделять внимание своему здоровью, а особенно глазам, ведь они являются неотъемлемой частью человеческой жизни. При появлении неприятных симптомов и различных проблем с данным органом, следует поскорее обратиться к врачу, чтобы получить соответствующую медицинскую помощь и избежать печальных последствий.
Источник
Одним из наиболее распространенных офтальмологических заболеваний, поражающих сетчатку, является макулодистрофия. Эту болезнь связывают со старением сетчатой оболочки глаза. До недавнего времени ее лечение считалось невозможным. Однако в 2017 году российские ученные провели клинические испытания по выращиванию сетчатки глаза. Новая медицинская методика позволяет «перепрограмировать» стволовые клетки и вырастить жизнеспособный трансплантат, который имеет все шансы прижиться у реципиента.
Суть методики
Генная инженерия — это технологии и методики, направленные на изменение структуры генома человека путем осуществления различных манипуляций с генами. В медицине она используется относительно недавно, однако, уже эффективно применяется для лечения некоторых видов бесплодия, а с 2016 года в США внедрен метод лечения нескольких видов рака с помощью технологий геномной модификации. Часто ученные проводят эксперименты со стволовыми клетками. Они являются незрелыми, поэтому после изменения генов способны дифференцироваться (превращаться) в клетки различных органов.
Ученый сделал прорыв в применении клеточных технологий в медицине.
В 2012 году японский ученый Синье Яманака стал лауреатом Нобелевской премии за исследование в области медицины. Он доказал, что после изменения генома первичных стволовых клеток эмбриона из них можно вырастить любые ткани организма. Из чужеродной эмбриональной ткани получается аллотрансплантат, который с большей вероятностью будет отторгнут организмом. Так что эта универсальная методика подходит только для двух органов, которые отличаются низкой иммунной реакцией.
В таких органах, как головной мозг и глаз пересадка чужих стволовых клеток не вызывает активного отторжения.
В 2017 году российские ученные федерального центра физико-химической медицины для проведения опытов взяли за основу этот метод. Путем репрограммирования генов плюрипотентных (первичных) клеток нежизнеспособных эмбрионов были проведены успешные клинические испытания по выращиванию здоровой сетчатки у кроликов. Успех эксперимента позволил говорить о дальнейшем использовании этой технологии у человека.
Вернуться к оглавлению
Эффективность метода и проведенные исследования
Методика позволит минимизировать риски отторжения.
Конечно, аутотрансплантация (трансплантат для пересадки берется от клеток кожи того же организма, куда пересаживается) позволила бы полностью исключить развитие нежелательных эффектов. Однако универсальность этого способа восстановления сетчатки, который подходит для большинства пациентов, упрощение технологии и снижение стоимости операции, а также повышение ее доступности говорит в пользу выращивания сетчатки глаза из генетического субстрата эмбриона.
Клинические исследования этой методики проводят во многих других странах: Германии, США, Японии. Первая успешная пересадка состоялась именно там, еще в 2014. Из-за изменений в законе испытания пока заморожены, однако анонсировалось их продолжение в 2018 году. В России вследствие отсутствия регулирующих процесс нормативных актов пересадка трансплантатов людям невозможна. Ученные настроены оптимистично, так как уже есть первые добровольцы для проведения экспериментальных операций.
Предполагается, что использование стволового эмбрионального трансплантата станет новым словом в лечении макулодистрофии. При этом заболевании дистрофия сетчатки развивается в связи с нарушением ее питания. Вследствие поражения центральной зоны (макулы) сетчатой оболочки наблюдается прогрессивное снижение зрения. Чаще всего встречается возрастная форма заболевания, поражающая людей старше 40 лет. Редкая наследственная форма болезни приводит к слепоте у трудоспособного населения. Считалось, что остановить запущенный процесс старения и дистрофии сетчатой оболочки нельзя, можно лишь замедлить его. Восстановление сетчатки путем ее выращивания из стволовых клеток с помощью достижений генной инженерии делает возможным полное излечение от этой болезни.
Источник
Humayun M.S., Kashani A.H.
Весной 2018 года в двух авторитетных научных журналах – Nature Biotechnology (da Cruz L. et al.) и Science Translantional Medicine (Kashani A.H. et al.) – появились публикации об первом опыте трансплантации слоя клеток ретинального пигментного эпителия (РПЭ), выращенных из стволовых клеток, при возрастной макулярной дегенерации (ВМД). В данной статье представлен краткий обзор литературных сведений об этом методе терапии.
До внедрения технологии трансплантации клеток или тканей в клиническую практику необходимо решить как минимум две проблемы. Во-первых, требуется найти коммерчески доступный источник стволовых клеток и получить одобрение контролирующих органов, например, Food and Drug Administration (FDA). Во-вторых, необходимо разработать и усовершенствовать методы дифференцировки и созревания клеток, а также методы их хирургической доставки. Этот путь может быть пройден только благодаря передовым достижениям науки, медицины и инженерии.
Источником получения клеток РПЭ в настоящее время могут быть эмбриональные человеческие стволовые клетки и индуцированные плюрипотентные стволовые клетки. Оба типа стволовых клеток могут самообновляться и дифференцироваться в различные типы клеток взрослого человека. Индуцированные плюрипотентные стволовые клетки получают из зрелых клеток взрослого человека путем их перепрограммирования и перевода в состояние, близкое к эмбриональному статусу. Эмбриональные человеческие стволовые клетки получают из эмбрионов человека, находящихся в стадии бластоцисты.
Эмбриональные человеческие стволовые клетки являются аллогенным материалом и, следовательно, обладают определенным потенциалом к отторжению вследствие несовпадения поверхностных белков комплекса гистосовместимости. Пациенты, которым была проведена имплантация клеток с отсутствием гистосовместимости, нуждаются в проведении длительной системной иммуносупрессии. Индуцированные плюрипотентные стволовые клетки, получаемые из собственных зрелых клеток, имеют отличную гистосовместимость, однако могут иметь мутации генетического материала, связанные с возрастом.
Получение подходящих аутологичных клеток РПЭ из индуцированных плюрипотентных стволовых клеток – это долгая и дорогая процедура. Кроме того, перепрограммирование клеток может усилить их потенциал к пролиферации и спровоцировать развитие онкологических заболеваний.
Субретинальное и интравитреальное введение суспензии клеток РПЭ, полученной из стволовых клеток, обладает некоторой эффективностью и достаточно безопасно (Shwartz S.D. et al., Park S.S. et al.). Однако при помощи этих методик восстановить утраченный пигментный эпителий в зоне географической атрофии не удалось. Предполагают, что некоторая эффективность данных методик связана в большей степени с паракринными механизмами, обеспечивающими поддержку оставшейся ткани сетчатки вне зоны географической атрофии.
Следующим шагом в эволюции клеточной терапии стала попытка восстановления зоны географической атрофии при помощи имплантации монослоя поляризованных клеток РПЭ, который смог бы имитировать природную структуру РПЭ и, возможно, его функции. Имплантация монослоя теоретически может иметь преимущества над введением суспензии клеток.
Для трансплантации монослоя клеток РПЭ требуется поддерживающая мембрана, подобная естественной мембране Бруха (Booij J.C. et al.). Такая мембрана должна быть полупроницаемой, чтобы удерживать клетки РПЭ и в то же время обеспечивать полноценную диффузию веществ между сетчаткой и хориоидеей. В литературе описаны попытки использования в качестве каркаса для размещения клеток различных натуральных субстанций – амниотической мембраны, гиалуроновой кислоты, желатина, фибриногена, шелка, коллагена и передней капсулы хрусталика.
Однако натуральные субстанции не всегда можно получить в больших производственных масштабах. Они могут иметь вариабельные физические характеристики, потенциально аллергогенны и кроме того, могут стать переносчиком различных заболеваний. Несмотря на это в литературе описан один клинический случай применения коллагеновой мембраны при лечении неоваскулярной ВМД. Mandai M. et al. выполнили трансплантацию слоя клеток РПЭ, полученного из индуцированных плюрипотентных стволовых клеток, одному пациенту. Клетки РПЭ были культивированы на коллагеновом каркасе, а затем непосредственно перед имплантацией каркас был разрушен при помощи коллагеназы.
Серьезных побочных эффектов операции не отмечалось в течение 25-месячного периода наблюдения. Ухудшения или улучшения максимальной корригированной остроты зрения не произошло. Трансплантация клеток РПЭ, запланированная второму пациенту, выполнена не была по причине выявления мутаций в ДНК клеток РПЭ, полученных из индуцированных плюрипотентных стволовых клеток. Набор участников для проведения данного исследования проводился в 2015 году.
Синтетические мембраны являются альтернативой натуральным субстанциям. Производство синтетических материалов легче поддается контролю, и продукты получаются более униформными, но их биосовместимость остается спорным моментом. В недавнем клиническом исследовании, проведенном London Project to Cure Blindness, использование полиэтилен терефталата (polyethylene terephthalate (PET)) в качестве каркаса для клеток РПЭ, полученных из эмбриональных человеческих стволовых клеток, привело к массивному субретинальному кровотечению у двух пациентов с неоваскулярной ВМД (da Cruz L. et al). PET – это наиболее часто используемый небиодеградируемый термопластический полимер семейства полиэстеров, используемый в том числе при производстве одежды и контейнеров. Тем не менее, хотя у одного из пациентов произошло развитие пролиферативной витреоретинопатии, потребовавшей проведения ревизии витреальной полости, у обоих пациентов было отмечено улучшение зрения и увеличение скорости чтения.
В другом исследовании, организованном California Institute of Regenerative Medicine, группе исследователей из University of Southern California, University of California-Santa Barbara и California Institute of Technology, удалось создать лист из парилена (parylene) субмикронной толщины, который смог обеспечить необходимую поддержку и поляризацию клеток РПЭ, выращенных из индуцированных плюрипотентных стволовых клеток (Koss M.J. et al., Brant Fernandes R.A. et al.).
Парилен – это небиодеградируемая субстанция, которая успешно используется in vitro, а также в исследованиях на животных и в клинических исследованиях. Недавно были опубликованы предварительные результаты фазы 1 исследования, в котором имплантация этой структуры была выполнена четырем пациентам с продвинутой стадией «сухой» формы ВМД и географической атрофией. После операции у одного пациента произошло улучшение зрения на 17 букв, а у двух других пациентов было отмечено улучшение зрительной фиксации. Эти обнадеживающие данные требуют проведения дальнейших исследований с большим периодом наблюдения и наличием контрольных групп.
В целом, результаты проведенных клинических исследований демонстрируют потенциал клеток РПЭ, выращенных из индуцированных плюрипотентных стволовых клеток и эмбриональных человеческих стволовых клеток, в замещении дегенеративной ткани при ВМД. Хотя все исследования проводились на малом количестве пациентов с продвинутыми стадиями заболевания, небольшое количество осложнений и побочных эффектов, а также улучшение остроты зрения и зрительных функций позволяет предположить, что технология замещения клеток в зоне потери РПЭ представляет собой перспективную терапевтическую технологию. Для уточнения эффективности различных клеточных технологий необходимы большие комплексные исследования. Полученные результаты дают надежду на то, что со временем проблема наиболее распространенной в Западном мире причины потери зрения в скором времени будет решена.
Humayun M.S., Kashani A.H. Stem cell-derived RPE sheet transplantation offers new hope for AMD treatment. Retina Times. 2018;Issue 74;36(2):6-7.
Источник


