Оптогенетика и протезирование дегенеративной сетчатки
Во всем мире множество людей страдает от дегенеративных поражений сетчатки, которые приводят к полной потере зрения. Однако современные научные достижения дают надежду на то, что в будущем создание кибернетических протезов этого «тонкого» органа станет повседневной операцией. Технологии оптогенетической инженерии позволяют сделать чувствительными к свету не деградировавшие клетки-фоторецепторы, а лежащие глубже ганглионарные клетки, а носимый микрокомпьютер с голографическим передатчиком будет транслировать им закодированный сигнал, имитирующий «выдачу» утерянной сетчатки.
Во всем мире около 20–25 миллионов людей страдают от потери зрения, вызванной дегенерацией желтого пятна (макулярной дистрофией) и пигментной дистрофией сетчатки. Особенность этих заболеваний в том, что поражаются главным образом фоторецепторы (клетки-«палочки» и «колбочки» ), а лежащие ниже ганглионарные клетки , «интегрирующие» информацию от светочувствительных клеток и передающие ее в мозг, остаются неповрежденными. Этот факт позволяет создать «протез» сетчатки, который передавал бы ганглионарным клеткам такие же сигналы, что и настоящая сетчатка. Интересно, что такие протезы уже созданы: американское ведомство FDA недавно одобрило для использования устройство Second Sight’s Argus II [1], состоящее из небольшой видеокамеры и передатчика, вмонтированных в очки, и имплантированного в глаз 60-электродного микрочипа, функционально замещающего дегенерировавшие клетки сетчатки. Но с помощью такого протеза зрение восстанавливается, конечно, лишь на малую долю от нормального: пациенты способны видеть свет, различать наиболее контрастные контуры предметов и слабо ориентироваться в пространстве. Но по общепринятым стандартам они лишь немногим отличаются от слепых людей.
Более продвинутый подход заключается не в имплантации микрочипа, а в придании световой чувствительности непосредственно тем клеткам, которые должны реагировать на сигналы, поступающие от сетчатки, — ганглионарным клеткам. В современной молекулярной биологии этот прием называется оптогенетикой и заключается во «встраивании» в нервные клетки светочувствительных белков. Наиболее часто в качестве такого белка используют каналородопсин — фоторецептор клеточной мембраны зеленых водорослей, который под действием света начинает пропускать в клетку ионы натрия — подобно тому, как это делают натриевые каналы мембраны нейронов, запуская в них потенциал действия. Подробнее о принципах оптогенетики можно прочесть в статье «Свет и генетика» [3].
Однако выясняется, что сделать ганглионарные клетки светочувствительными недостаточно для того, чтобы «реанимировать» сетчатку. Дело в том, что слой фоторецепторов (палочек и колбочек) не просто воспринимает световые импульсы и передает их далее на ганглионарный слой, но особым образом «кодирует» информацию, превращая ее в сложную последовательность импульсов, мало напоминающую «входной» сигнал. Поэтому одной из главных задач является не только совершенствование технических характеристик протеза, но и создание цифровой системы кодирования сигнала, чтобы ганглионарные клетки получали информацию в «привычном» для них виде (то есть, уже обработанную по алгоритму, заложенному в живую сетчатку).
Американские исследователи создали такую систему, включающую модуль кодирования, «натренированный» на сигналах, считанных со здоровых сетчаток, и мини-проектор, передающий закодированную информацию на слой ганглионарных клеток. Последние при этом несли в своих клеточных мембранах каналородопсин ChR2, что позволяет возбуждать клетки, просто посветив на них [4] . Принципиальная схема этой системы приведена на рисунке 1.
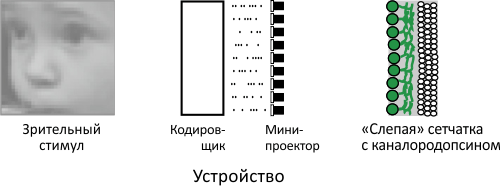
Рисунок 1. Принципиальная схема «протеза» сетчатки. Устройство (в центре) состоит из двух главных блоков: 1) «кодировщика» сигнала, который превращает зрительный стимул (слева) в последовательность импульсов, имитирующих электрическую активность сетчатки, и 2) «передатчика» (здесь — мини-проектора), посылающего «закодированные» сигналы в виде вспышек света на дефектную сетчатку (справа). Ганглионарный слой сетчатки воспринимает эти импульсы аналогично тому, как принимал бы сигнал от фоторецепторов — благодаря наличию каналородопсина.
Проверку «работоспособности» протеза сетчатки проводили в несколько этапов. Первым делом сравнили электрическую активность «выхода» ганглионарных клеток нормальной сетчатки со «слепой» сетчаткой, снабженной кодирующим сигнал протезом. В качестве контроля взяли, как это принято в рекламе стирального порошка, «обычный» протез сетчатки (рис. 2, сверху). «Обычность» заключается в том, что ганглионарные клетки здесь возбуждаются непосредственно зрительным стимулом, без кодирования сигнала в понятную им форму. Паттерн электрической активности в первых двух случаях почти совпал, тогда как на «обычном» протезе картина резко отличалась. Это подтверждает, что этап «кодирования» зрительного стимула совершенно необходим для адекватной имитации работы сетчатки.
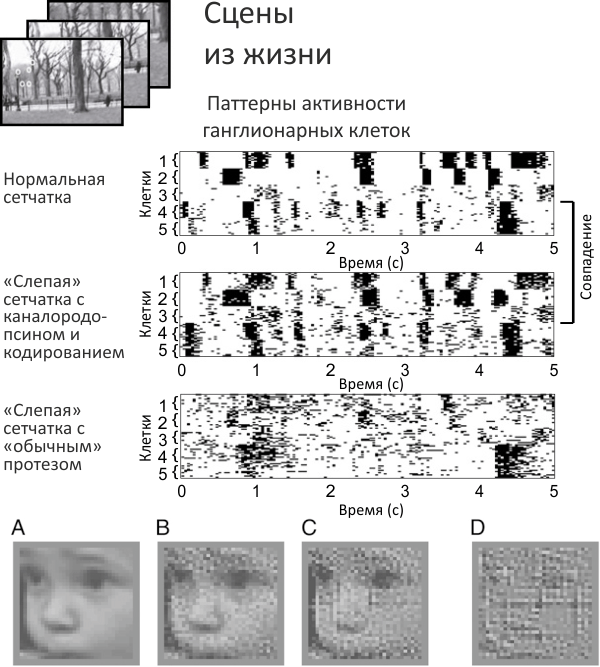
Рисунок 2. Работоспособность протеза сетчатки. Сверху: «Слепая» сетчатка с протезом, кодирующим зрительный стимул (график в центре), активирует ганглионарные клетки почти так же, как и нормальная сетчатка (вверху). При этом «обычный» протез, не включающий стадию кодирования сигнала, формирует аномальную картину активности ганглионарных клеток (внизу). На графиках показана электрическая активность пяти ганглионарных клеток в течение пяти секунд. Снизу: Реконструкция изображения на основе активности ганглиев сетчатки. А. Исходный зрительный стимул. B. Картинка, восстановленная по выдаче кодировщика. С. Картинка, восстановленная в случае протеза с «кодом сетчатки». D. Картина с «обычного» протеза сетчатки: отсутствие стадии кодирования сигнала искажает восстановленное изображение почти до неузнаваемости.
Потом провели более наглядную проверку, основанную на реконструкции изображения по «записанным» с ганглионарных клеток сигналам. Мозг, скорее всего, не занимается реконструкцией картинки как таковой, но для анализа адекватности передаваемой информации этот тест очень показателен. Результат оказался «на лицо» — протез сетчатки с кодированием зрительного стимула выдавал картину, в которой легко можно было установить первоначальное лицо ребенка, подаваемое системе на вход (рис. 2, внизу). В случае же «обычного» протеза в реконструированной картине едва ли можно узнать лицо вообще, не говоря уже про индивидуальные черты.
Последним провели тест на мышах, подтвердивший важность модуляции зрительного стимула «кодом сетчатки» при попытках восстановления зрения. Для эксперимента использовали таких же животных, из которых получали препараты сетчатки для изучения. Мышам фиксировали положение головы и использовали систему отслеживания движения глаз, чтобы определить, следит ли животное за происходящим на экране. Оказалось, что мыши с «кодированным» протезом обретали способность отслеживать объекты на экране, а вот «обычный» протез такой возможности, увы, не предоставлял.
На основе проделанных экспериментов ученые делают вывод, что будущие поколения протезов сетчатки должны предусматривать не только более высокое разрешение, но и блок цифрового кодирования зрительного импульса, переводящий обычное изображение на язык последовательностей импульсов, воспринимаемых ганглионарными клетками. Можно даже пофантазировать и представить себе различные «прошивки» такого блока, обеспечивающие лучшую остроту зрения или какие-нибудь особенные визуальные эффекты, недоступные истинно зрячим людям.
Однако совершенствовать можно не только систему генетической трансформации ганглионарных клеток фоточувствительными белками или способ кодирования сигналов для них. Исследователи из Израильского технологического института (Техниона) разрабатывают систему голографической стимуляции ганглионарных клеток, имеющую ряд преимуществ перед уже упомянутыми «мини-проекторами» [5]. Это высокая интенсивность, равномерность освещения (отсутствие необходимости в системах развертки), низкое энергопотребление, высокая разрешающая способность и возможность создавать трехмерную картину возбуждения. Ведь для передачи «кода сетчатки» на ганглионарные клетки нужно импульсно освещать очень маленькие области пространства (размером в считанные микрометры) с возможностью быстрого переключения и фокусировки на разных слоях клеток — в отличие от грызунов, у человека ганглионарный слой не плоский, а объемный. Кроме того, ганглионарные клетки с каналородопсином — это все-таки не природные фоторецепторы, и их чувствительность намного хуже, чем у наших палочек и колбочек. Поэтому высокая яркость и точность управления голографической системы — чрезвычайно важное преимущество перед мини-проектором или просто электронным дисплеем, встроенным в очки.
Ученые создали экспериментальную установку для голографической стимуляции ганглионарных клеток сетчатки, основанную на лазере, луч которого модулируется управляемым компьютером жидкокристаллическим ферроэлектрическим чипом. Это устройство позволяет контролировать дифракцию и одновременно «адресовать» от сотен до нескольких тысяч «пикселов» в ганглионарном слое, чтобы стимулировать зрительные импульсы. (Конечно, в этом случае тоже идет речь о ганглионарных клетках, экспрессирующих каналородопсин и возбуждаемых светом.) В результате мощность исходного луча лазера (≈700 мкВт) дробится на множество «пятен» с мощностью 1–10 мкВт, что как раз достаточно для активации каналородопсина и совершения элементарного акта зрения. Высокая скорость переключения голографической системы (2000 Гц) позволяет устранять дефекты голограммы и (в перспективе) использовать многоцветную стимуляцию в надежде восстановить зрение во всех его красках.
Руководитель разработок профессор Шай Шохам (Shy Shoham) вот как объясняет преимущества голографического подхода: «Электронные дисплеи могут стимулировать много клеток одновременно, но у них слишком низкая яркость и энергоэффективность. Лазеры дают высокую эффективность, но от них не получить параллельный пучок. Так вот голография — оптимальный способ использования преимуществ лазерного света в стимуляции нервных клеток сетчатки» [6].
И хотя создание протеза сетчатки, полностью устранившего бы проблему дегенеративных заболеваний глаза, пока находится где-то на горизонте, сегодня вполне можно вдохновиться научным прогрессом, способным обратить вспять потерю одного из самых главных наших органов чувств. Опираясь на это вдохновение, можно проникнуться пониманием футуристических идей трансгуманизма, сулящего человеку в будущем полный апгрейд его бренного тела с использованием более современных компонентов. Но можно этого и не делать.
- Greenemeier L. (2013). FDA Approves First Retinal Implant. Scientific American;
- Зрительный родопсин — рецептор, реагирующий на свет;
- Тулинов Д. (2012). Свет и генетика. «Наука и технологии России»;
- S. Nirenberg, C. Pandarinath. (2012). Retinal prosthetic strategy with the capacity to restore normal vision. Proceedings of the National Academy of Sciences. 109, 15012-15017;
- Inna Reutsky-Gefen, Lior Golan, Nairouz Farah, Adi Schejter, Limor Tsur, et. al.. (2013). Holographic optogenetic stimulation of patterned neuronal activity for vision restoration. Nat Commun. 4;
- Researchers Test Holographic Technique for Restoring Vision. (2013). ScienceDaily.
Источник
Статья на конкурс «био/мол/текст»: Многие из нас воспринимают зрение как должное — мы с легкостью можем найти нужный носок в шкафу и любоваться красками осени. А между тем, по данным ВОЗ, около 2,2 млрд человек в мире имеют нарушения зрения, около 39 млн — тотально незрячие, а более 1 млн из них — это необратимо слепые дети. В России около 100 тысяч незрячих, при этом примерно 20% инвалидов по зрению — молодежь. Незрячим приходится несладко, а потому ничего удивительного, что ученые активно ищут технологию для восстановления зрения. За последние годы создано многое: и бионические глаза, и генетическое восстановление зрения. Но почему до сих пор все слепые не прозрели?
1
Лидия Георгиева
26 ноября 2019
Статья на конкурс «био/мол/текст»: Слух кажется таким естественным, что мы никогда не задумываемся о нем. В статье вы узнаете не только о том, как работает ухо, но и познакомитесь с современными методами изучения молекулярных процессов передачи звука и передовыми технологиями коррекции патологий слуха с помощью оптогенетики.
2
Марина Слащева
09 ноября 2018
21–22 сентября 2017 г. прошла Международная конференция «ФизтехБиоМед-2017». Эксперты обсудили идеи, связанные с «активным долголетием», неврологией и биотехнологиями. Рассказываем о самых интересных лекциях: чего достигла современная инженерия в кардиологии, почему медицина фокусируется не на том и как сделать виртуального человека своими руками.
Мария Комарова
25 декабря 2017
Статья на конкурс «био/мол/текст»: Исследователи лаборатории перспективных исследований мембранных белков МФТИ открыли дополнительную возможность возбуждать нервные клетки с помощью света, и я расскажу вам об этом как соавтор. Я опишу, как работают белки, способные запускать и блокировать нервный импульс. Я объясню, каким образом можно целенаправленно изменять белок, чтобы он приобрел новые свойства, которых не имел в природном виде.
2
Виталий Шевченко
17 октября 2017
Пока не будет создан полноценный искусственный интеллект, мозг будет оставаться единственной мыслящей системой, способной хотя бы попытаться заглянуть внутрь себя и осознать свое устройство. Масштаб этой задачи обескураживает. Вряд ли какой-либо объект во Вселенной может сравниться по своей сложности с человеческим мозгом. Так какими же методами мы изучаем работу собственного мозга?
9
Дмитрий Лебедев
15 сентября 2017
Большая часть медико-биологических исследований проводится на клетках in vitro (то есть, не на живом организме, а на клетках «в пробирке»). Клетки используют в качестве модельного биологического объекта в научных исследованиях, при тестировании и производстве лекарств. Кроме этого, ученые научились исправлять генетические ошибки в клетках и наделять их способностью противостоять некоторым заболеваниям, что служит основой для медицинских технологий будущего — генной и клеточной терапий. Эта статья расскажет о методах работы с клетками, а также о возможностях и ограничениях, связанных с их использованием.
1
Георгий Шаронов
18 августа 2017
С помощью зрения человек воспринимает около 80% информации. Утрата любого канала восприятия окружающего мира — большая трагедия для человека, но потерять зрение — основного поставщика внешней информации — особенно неприятно. Ученые всего мира ломают головы над решением проблемы слепоты — над тем, как остановить потерю зрения и как вернуть его уже ослепшим людям. И они делают значительные успехи. В 2016 году компания RetroSense поставила эксперимент по восстановлению зрения у крыс — и у них получилось. Посмотрим, что же они придумали.
Современные биороботы создаются по образу и подобию — нет, не своих творцов-изобретателей, а животных. Вдохновившись природным «дизайном», ученые разрабатывают причудливые механизмы, копирующие походку гепарда или саламандры, движения змей и медуз. Недавно в Science вышла статья о мягком киборге — копии ската (надотряд Batoidea). Что за этим стоит — игры разума, праздно блуждающего в дебрях фундаментальной науки, или технологический прорыв будущего?
Статья на конкурс «био/мол/текст»: Фундамент учения дуализма серьезно пошатнулся еще во второй половине XIX века наблюдением за отклонениями психической деятельности у людей с повреждениями специфических областей коры головного мозга, а окончательно превратился в руины к середине XX века с первыми успешными опытами нейрохирургии. Однако по-настоящему прикоснуться к материальному субстрату высших психических функций позволил XXI век, принесший небывалый прогресс в разработке технологий для исследования клеточных механизмов высшей нервной деятельности. В статье предлагается краткий обзор технологий исследования долговременной памяти, основанных на современных достижениях генной инженерии. Речь пойдет о методиках визуализации нейронных сетей памяти и манипулирования ими с использованием явления активностно-зависимой генной экспрессии.
Статья на конкурс «био/мол/текст»: В инструментарии оптогенетики пополнение: обнаружены первые анионные канальные родопсины. Эти белки под действием света пропускают внутрь клетки ионы хлора, что приводит к гиперполяризации мембраны и, следовательно, подавлению электрической активности возбудимых клеток.
Источник
| Название | |
| Авторы | |
| Рубрики | |
| Ключевые слова | |
| Искать в тексте | |
| Специальность |
| Год издания | Раздел базы данных |
| с по |
| РЕЗУЛЬТАТЫ ПОИСКА в разделе <ПЕРИОДИЧЕСКИЕ ИЗДАНИЯ> по запросу { Ключевые слова: «оптогенетика» } Результаты 1 — 14 из 14 документов | Печать требований |
| ||
| Нейрогенез — сложный процесс, который определяет развитие головного мозга в эмбриональном периоде; он важен для процессов нейропластичности на протяжении всей жизни организма. Постнатальный нейрогенез происходит в нейрогенных нишах, которые обеспечивают регуляцию процессов пролиферации и дифференцировки стволовых и прогениторных клеток при действии стимулов, запускающих механизмы пластичности головного мозга. Клетки глиальной и эндотелиальной при… >> | ||
|
| ||
| Методы, базирующиеся на генетически кодируемых молекулярных конструкциях, такие как антисенс-нокдаун и РНК-интерференция, изменяющие экспрессию целевых генов, широко используются для анализа функции кодируемых этими генами белков, а также находят применение в медицинской практике. С помощью этих методов, например, было установлено, что даже кратковременное снижение экспрессии одного из рецепторов норадреналина в критический период развития мозга … >> | ||
|
| ||
| Современные исследования обогатились перспективными научно-технологическими направлениями, в которых свет играет ключевую роль как инструмент модуляции клеточной активности и инвазивного мониторинга внутриклеточных ионов и других компонентов. Основное преимущество этих подходов — возможность точного управления интенсивностью, спектральными характеристиками и длительностью световых сигналов в пространстве и времени. В обзоре кратко представлены ос… >> | ||
|
| ||
| Одним из вариантов оптогенетического протезирования дегенеративной сетчатки является подход, связанный с воссозданием ON/OFF рецептивного поля ганглиозных нейронов путем таргетированной экспрессии возбуждающего светоактивируемого белка в центральной части ганглиозной клетки, а тормозного — в периферической. В рамках данного подхода мы исследовали возможность использования различных заякоривающих мотивов для обеспечения соматической или дендритной… >> | ||
|
| ||
| Расширение и углубление наших представлений о том, как работает мозг, требует постоянного совершенствования не только методов регистрации нейронной активности, но и улучшения экспериментальных способов активации отдельных клеток и их компартментов. В последнее время большое распространение получили оптогенетические методы стимуляции нейронов с помощью тонко сфокусированного света, запускающего открытие фотоактивируемого деполяризующего катионного… >> | ||
|
| ||
| В статье представлена разработанная авторами принципиальная схема многоканального комбинированного опто-электродного микроимплантата с применением принципов обратной связи. Предложен алгоритм стимуляции и регистрации нейронального ответа с возможностью подстройки командных сигналов оптического источника и, опционально, системы введения фармакологических препаратов. Устройство позволит использовать адаптивную оптогене-тическую стимуляцию автономно… >> | ||
|
| ||
| Гетеросинаптическая пластичность — малоисследованный вид синаптической пластичности, в котором модификации подвергаются синапсы, которые не были активны во время процесса индукции пластичности. Основной методической проблемой при изучении механизмов гетеросинаптической пластичности традиционными методами является необходимость проведения большого количества экспериментов ввиду вероятностного характера развития пластических изменений синаптических… >> | ||
|
| ||
| Пигментная тапеторетинальная дегенерация (пигментный ретинит, retinitis pigmentosa, RP) — одна из наиболее тяжелых и одновременно распространенных форм наследственной дегенерации сетчатки. По механизмам возникновения RP существенно гетерогенен и объединяет целую группу болезней, вызываемых различными причинами, затрагивающих совершенно различные молекулярные механизмы и клеточные типы. Различные терапевтические подходы позволяют лишь в той или ин… >> | ||
|
| ||
| В обзоре рассмотрены новые возможности, которые открываются с развитием онтогенетических методов, преимущества их сочетания с традиционными электрофизиологическими подходами в экспериментальной работе для решения широкого круга нейрофизиологических задач. Обзор содержит описание основных трудностей и нюансов в работе с оптогенетическими методами, примеры технических решений для выполнения одновременной оптостимуляции и регистрации нейронной актив… >> | ||
|
| ||
| Канальные родопсины представляют собой ретинплнденовые белки, уникальные по своей способности генерировать фотоиндуцированные пассивные ионные токи через клеточную мембрану. Гетерологическая экспрессия генов канальных родопсинов в клетках животных, в первую очередь, нейронов — технология, получившая название «оптогенетики» — позволяет регулировать их активность с миллисекундным временным разрешением. В течение первых 15 лет развития в оптогенетик… >> | ||
|
| ||
| Технология оптогенетики (использование фоточувствительных белков микроорганизмов для контроля жизнедеятельности клеток животных) становится все более и более популярной в лабораториях всего мира. Особое место среди этих белков занимают родопсиновые пигменты, способные к трансмембранному переносу ионов и используемые в оптогенетике для регуляции светом мембранного потенциала клеток, в первую очередь нейронов. Если родопсиновые ионные помпы перенос… >> | ||
|
| ||
| ОБЗОРЫ ЛИТЕРАТУРЫ. Представлен обзор современного состояния нового направления в офтальмологии и физиологии зрения, основанного на использовании методов оптогенетики. Оптогенетика — междисциплинарное направление, обьединяюшее генную инженерию, оптику и физиологию. Она позволяет с помощью светоактивируемого белка, ген которого доставляется и экспрессируется в совершенно определенной клетке сетчатки, регулировать светом (активировать или тормозить)… >> | ||
|
| ||
| Путем внедрения генов опсинов в нейроны мозга исследователи получили возможность активировать эти нейроны с помощью вспышек света. Данная методика, называемая оптогенетикой, позволяет с исключительной точностью исследовать функцию определенных нейронов головного мозга животных в свободном поведении. Такая точность была недостижима с помощью прежних методов — в частности, электростимуляции. С помощью методики, называемой оптогенетикой, раскрываютс… >> | ||
|
| ||
| Усилия исследователей привели к рождению молодой области науки, называемой оптогенетикой, в которой методы генной инженерии сочетаются с оптикой. С ее помощью специалистам уже удалось увидеть функционирование некоторых групп нейронов. Более того, данный подход даже позволил им управлять нейронами с помощью света. Эти достижения рождают надежду, что когда-нибудь благодаря оптогенетике ученым удастся раскрыть работу мозга, а врачам — вылечить ряд з… >> | ||
|
Источник


