Новое в диагностике глаукомы
ГОУ ВПО «РГМУ Росздрава», Москва
Ведущая роль уровня внутриглазного давления (ВГД) в диагностике глаукомы в последние годы подвергается сомнению. Индивидуальная толерантность зрительного нерва определяет индивидуальный уровень офтальмотонуса, при котором сохраняется нормальная трофика нервных структур глаза. Определение же индивидуального уровня ВГД представляет известные трудности, поскольку требует учитывать уровень артериального давления, вид клинической рефракции, тип регуляции сосудистого тонуса, индивидуальные особенности кровоснабжения головки зрительного нерва. Отсюда становится очевидным, что для выявления начала развития оптической нейропатии и оценки динамики ее течения, в частности при глаукоме, более существенное значение имеет раннее выявление начальных изменений периферического зрения.
Наиболее ранние изменения в центральных отделах сетчатки выявляются различными методами компьютерной статической периметрии и кампиметрии, при которых определение снижения порога чувствительности сетчатки говорит о начале развития оптической нейропатии (4).
Особая чувствительность крайней периферии латеральных отделов сетчатки к нарушению трофики объясняется спецификой кровоснабжения этой зоны. При дихотомическом делении ветвей ЦАС во внутренней ее половине на крайней периферии отмечаются сосуды 2-3 порядка, а в наружной половине — 3-4 порядка. Соответственно калибр сосудов латеральной половины сетчатки значительно уже, что объясняет большую чувствительность этих отделов к нарушению гемодинамики на фоне, например, повышения внутриглазного давления или при прогрессировании осевой миопии, а также при артериальной гипотонии.
Для ранней диагностики нарушения чувствительности периферии латеральных отделов сетчатки, необходима аппаратура и методика, позволяющая получить ответ на раздражение светом самых крайних по своему месторасположению светочувствительных элементов.
Некоторые из имеющихся на вооружении офтальмологов современные периметры, позволяют методом статической (фиксированное положение световых объектов) или кинетической (движущийся в поле зрения объект) периметрии определить периферические границы в известных пределах, зависящих от анатомических естественных образований лицевого черепа. Поэтому верхняя, внутренняя и нижняя граница ограничена примерно 60 градусами, а наружная имеет максимальное значение в 90 градусов. Однако наиболее рано начинают сужаться при развитии оптической нейропатии именно внутренние границы полей зрения, отражающие состояние латеральных отделов сетчатки, что фиксируется как появление «назальной ступеньки». Это означает, что патогномоничным для глаукомного процесса будет выпадение нижне- или верхневнутреннего квадрантов поля зрения. Диагностика этих изменений запаздывает, поскольку увидеть световой объект, предъявляемый на сфере известных периметров, становится возможным только после «преодоления» механической преграды в виде носа, надбровья и скуловой кости. Определение стадии глаукомы по степени сужения поля зрения часто не соответствует более значительному изменению диска зрительного нерва. Поэтому стадия заболевания уточняется в сторону прогрессирования глаукомного процесса именно по состоянию зрительного нерва, что больше соответствует уровню нарушения трофики сетчатки и ее проводящих путей.
Известен способ ранней диагностики открытоугольной глаукомы, только частично решающий проблему увеличения поля зрения перемещением на поверхности сферы периметра точки фиксации взора и поворотом головы обследуемого пациента, что позволяет произвести некоторую коррекцию границ, суженных влиянием выдающихся отделов глазницы и носом (1).
Учитывая форму внутренней оболочки глаза — сетчатки, представляющую собой немногим более полусферы, правильно было бы получать отображение поля зрения в виде круга. На имеющихся же в практике приборах поле зрения выглядит в форме элипса. Начальные признаки поражения периферических отделов сетчатки, состояние которых оценивается по сужению границ поля зрения, впервые обнаруживаются только при сужении их более чем на 45-50 градусов в одном или более из трех (верхний, внутренний и нижний) квадрантов поля зрения. В связи с этим о начальных проявлениях нейропатии принято судить по выявлению парацентральных скотом в зоне Бьеррума, где кровоснабжение осуществляется сосудами такого же калибра, как и на крайней периферии.
Усовершенствование диагностической аппаратуры для исследования периферического зрения проводится последние годы в направлении разработки портативного прибора, который одновременно повысил бы диагностическую ценность метода периметрии.
Одно из таких устройств может фиксироваться на голове пациента, а регистрация полей зрения производится на схеме, нанесенной на свисающем перед его лицом прозрачном экране, по которому двигается предъявляемый объект. В этой конструкции не решается проблема разобщения глаз и расширения полей зрения, суженных выступающими частями орбиты и носом (5).
Другое устройство представляет собой шаровой сегмент. Установленный перед глазом больного, он позволяет методом статической периметрии определить периферические границы поля зрения также в известных традиционных размерах: кверху-55˚, книзу — 65˚, кнутри — 55˚ и кнаружи — 90˚. Метод предлагается использовать в военно-полевых условиях и у лежачих больных для обследования поля зрения каждого глаза в отдельности (2).
Портативный сферопериметр ПСП-01 (патент № 2285440 от 06.12.2004 г.) для исследования поля зрения, благодаря своим оптимальным конструктивным размерам (наружный диаметр сферы 9 см) и физиологически оптимальной форме корпуса и демонстрационного экрана со световыми точечными тест-объектами, позволяет использовать его для проведения как статической, так и кинетической периметрии. Опытная апробация устройства выявила определенные преимущества сферообразной формы корпуса прибора, которая максимально коррелирует с естественной физиологической конфигурацией и размерами лица человека и позволяет наилучшим образом размещать его относительно лица пациента.
Для проведения статической периметрии устройство содержит корпус сферообразной формы с ручкой, на которой расположена клавиша для ответа пациента «тест-объект виден». В центральной части корпуса выполнено смотровое окно для наблюдения пациентом световых точечных тест-объектов — диодов, расположенных за перфорациями во внутреннем сферообразном экране при фиксации взора в центре этого экрана. Размеры смотрового окна определены, исходя из естественных физиологических размеров глазницы человека (3) и с учетом геометрической формы и размеров сферического демонстрационного экрана. Через многоразрядную шину прибор соединяется с персональным компьютером и устройством, печатающим результаты исследования.
Преимущества предлагаемого нами прибора: 1. Прибор повторяет профиль сетчатки (немного более полусферы). 2. Исключается влияние выступающих отделов орбиты и носа. 3. Границы поля зрения расширяются и определяются со всех сторон по 90˚ 4. Возможна комплектация сфер с цветными тест-объектами (красный, зеленый, белый) для диагностики патологии зрительного анализатора и некоторых неврологических заболеваний. 5. Программа предусматривает измерение не только фактической светочувствительности сетчатки, но и ее порога чувствительности при изменении яркости тест-объектов (статическая периметрия). 6. Момент появления тест-объекта в поле зрения фиксируется пациентом нажатием кнопки на рукоятке сферы. 7. Возможно подключение к домашнему компьютеру при наличии программы исследования. 8. Возможна проверка полей зрения у лежачих больных и при проведении профосмотров (скрининг-исследование). 9. В модификации прибор ПСП-1 может производить кинетическую периметрию для выявления явного сужения полей зрения и его выпадения (скотом). 10. Прибор может быть дополнен фиксатором для удержания перед глазом коррегирующей очковой линзы в случаях резко сниженной остроты зрения на фоне выраженной аномалии рефракции, что не является обязательным, поскольку метод периметрии оценивает светочувствительность сетчатки.
Значительным достоинством прибора ПСП-1 является его портативность, удобство использования и экономичная цена, что делает его доступным практически для всех медицинских учреждений и частных пользователей.
Периметр ПСП-1 может найти себе применение в программе «Домашний доктор» для динамического контроля за течением глаукомного процесса в сочетании с «Индикатором ВГД».
Список литературы
1. Ахметшин Р.Ф., Булгар С.Н. «Способ ранней диагностики первичной открытоугольной глаукомы», патент № 2220644 С1 от 10.01.2004 г.
2. Немцев Г.И., Манукян С.Г., Амирбекян Г.Г., Казарян Ф.А., Амарян С.А. «Способ исследования поля зрения», патент № 1528434 А1 от 15.12.1989 г.
3. Пономаренко В.Н., Басинский С.Н. «Клиническая анатомия органа зрения», Благовещенск, 1989 г., стр.7
4. Шамшинова А.М., Волков В.В. «Функциональные методы исследования в офтальмологии», Москва, 1999, стр.89-105
5. Эниня Г.И., Годлевска М.А., Смелтере Э.С. «Устройство для определения границ поля зрения», патент (дополнение) № 950305А61 В 3/02 от 15.08.1982 г.
Источник
Некоторые полагают, что данную болезнь можно вылечить на любой стадии. Эффективность лечения глаукомы зависит, в первую очередь, от своевременного, правильно поставленного диагноза. Глаукомная атрофия зрительного нерва – процесс необратимый, но существуют методы, которые позволяют замедлить его течение и значительно улучшить состояние глаза. Основная цель лечения глаукомы – нормализация повышенного внутриглазного давления и улучшение кровоснабжения глаза.
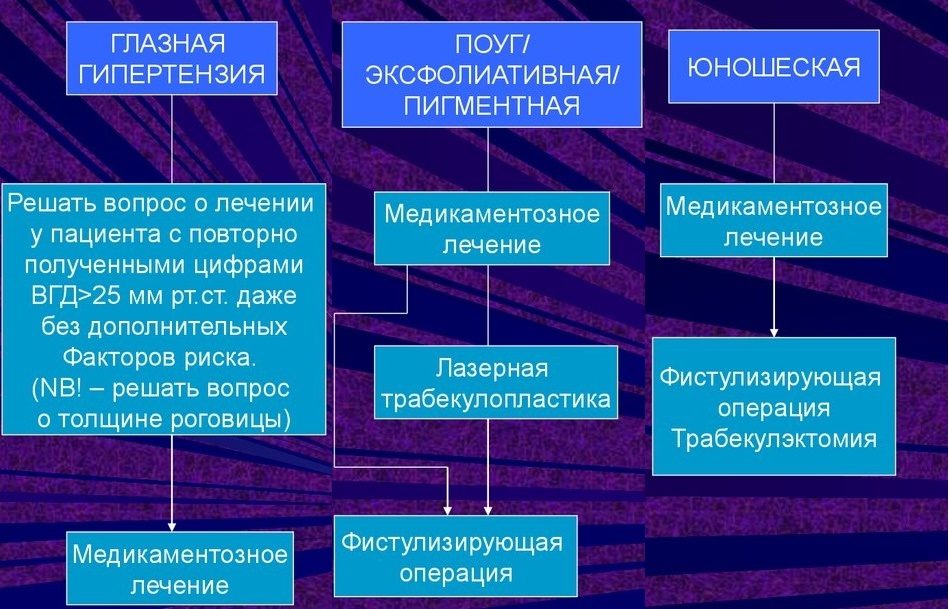
Консервативное лечение глаукомы включает несколько методик, позволяющих улучшить кровообращение в сосудах, нормализовать обменные процессы в глазу. Также проводят нейропротекторную терапию, защищающую сетчатку и зрительный нерв от дальнейшего разрушения. Помимо медикаментозного, в офтальмологии широко применяются и другие методы лечения глаукомы более поздних стадий: лазер, воздействующий на отток жидкости из глаза, и хирургическое вмешательство (микрохирургия глаза).

Лечение открытоугольной глаукомы
При постановке такого диагноза назначается лечение открытоугольной глаукомы медикаментозно, а в некоторых случаях показано хирургическое вмешательство. Методы лечения выбираются в зависимости от стадии заболевания.
- Начальная стадия. Рекомендовано медикаментозное снижение внутриглазного давления в среднем на 25%. Может быть применима лазерная трабекулопластика. Лазерное лечение первичной глаукомы в сочетании с эффективными в каждом конкретном случае медикаментозными препаратами является эффективной, безопасной и сравнительно бюджетной методикой снижения ВГД.
- Развитая стадия. Первостепенная задача: снижение давления в среднем на 25-50%. На данной стадии заболевания применяется несколько методов лечения и коррекции одновременно. Помимо фармакологических препаратов и лазера может быть назначено шунтирование (удаление катаракты и трансплантация искусственного хрусталика глаза). В некоторых случаях при глаукоме выполняют циклофотокоагуляцию. Эта разновидность лазерной микрохирургии обеспечивает минимальное повреждение тканей при хирургическом вмешательстве и позволяет избежать многих послеоперационных осложнений. Оперативное вмешательство осуществляется современными видео-эндоскопическими системами, позволяющими проводить операцию максимально точно и щадяще.
- Терминальная стадия. Лечение при рефрактерной глаукоме включает применение лекарственных препаратов в сочетании с лазерной хирургией (или криотерапией).
При глаукоме применяют глазные капли, снижающие внутриглазное давление (тимолол, латанопрост, бринзоламид и другие), а также для купирования острых приступов возможно применение осмотических диуретиков и ингибиторов карбоангидразы — маннитола, диакарба.
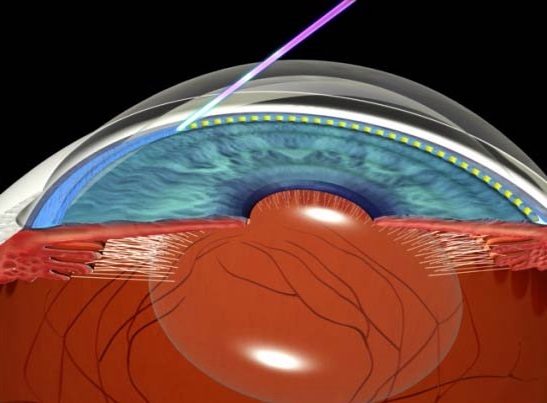
Лазерное лечение глаукомы (трабекулопластика)
При первичной открытоугольной глаукоме широко применяют методику лечения лазером. Этот метод может продуктивно сосуществовать наряду с медикаментозной терапией либо же полностью ее заменить, если пациент не в состоянии в полной мере выполнять рекомендации врача и применять препараты в форме глазных капель. Селективная лазерная трабекулопластика позволяет значительно снизить уровень ВГД. Сама операция относится к простым, не грозит серьезными осложнениями, проводится в амбулаторных условиях на протяжении не более 5 минут. Такую процедуру можно проводить повторно в силу ее мягкого нетравматичного воздействия на глаз.
В основе метода лежит воздействие на пораженные участки глаза лазерными импульсами — только на клетки дренажной системы глаза, в которых происходят дегенеративные процессы, не затрагивая тех структур и тканей глаза, которые не содержат пигмента меланина. После лазерного воздействия запускается процесс естественного восстановления клеток дренажной системы. После проведения процедуры СЛТ наблюдается значительное снижение внутриглазного давления до верхних норм и улучшается отток внутриглазной жидкости.
Перед операцией пациенту закапывают препараты для местного обезболивания. Далее через микроскоп лазерные импульсы поступают точно в ткани дренажной системы глаза и воздействуют на клетки на протяжении нескольких минут. Пациент при этом обычно не испытывает ощутимого дискомфорта.
Лазерная микрохирургия данного типа рекомендована пациентам с глаукомой определенных видов (открытоугольной, пигментной), гипертензией, аллергическими реакциями на антиглаукомные фармакологические препараты. А также при отсутствии эффекта от других методов лечения глаукомы.
Плюсы и минусы лазерного лечения глаукомы зависят от каждого конкретного случая. Общими преимуществами применения данного метода можно считать отсутствие серьезной подготовки к вмешательству, помимо общих рекомендаций врача, безболезненность при минимальном обезболивании, неинвазивность метода, быстрое проведение процедуры и возможность ее повторного выполнения, сравнительно невысокая цена и минимальный срок реабилитации после вмешательства. К минусам можно отнести ряд противопоказаний, включая возраст, недолгое сохранение результата, редкое, но все же возможное развитие послеоперационных осложнений (воспалительные процессы, нарушение целостности роговицы глаза).
Лечение глаукомы без операции
На начальных стадиях открытоугольную глаукому можно лечить медикаментозно без хирургического вмешательства. Эффективными антиглаукомными каплями признаны:
- Тимолол. Этот препарат считается эффективным средством, уменьшающим выработку внутриглазной жидкости и снижающим внутриглазное давление в среднем на 25%. Действие препарата становится ощутимым уже спустя 20 минут после приема. Эффект длится до суток.
- Бетоптик. Относится к той же группе, что и тимолол, и обычно применяется при глаукоме нормального давления или при небольшом повышении внутриглазного давления., Эффект препарата наступает в течении 20 минут после применения и длится до 12 часов. В отличие от тимомола, рактически не вызывает побочных эффектов.
- Дорзоламид. Действует на выработку внутриглазной жидкости, обычно хорошо переносится пациентами..
- Пилокарпин. Быстро снижает внутриглазное давление до 20%. Эффективен при неотложной помощи во время острого приступа глаукомы. Сужает зрачок и при длительном применении может вызывать катаракту..
- Траватан. В течении двух часов после приема способен снижать ВГД в среднем на 30%. Высокоэффективный препарат, который применяют всего один раз в сутки (перед сном). Вызывает активный рост ресниц (аналоги траватана даже входят в состав некоторых косметических средств, стимулирующих рост ресниц). Часто применение траватана сопровождается покраснением глаз, неприятными ощущениями и зудом.
К безрецептурным препаратам, дополняющим лечение глаукомы, относятся витаминные комплексы, которые позволяют улучшить состояние внутренних структур глаза, в том числе зрительных нервов. Препараты на основе ретинола улучшают передачу нервных импульсов и замедляют процессы ухудшения зрения. Рибофлавин (витамин В2) защищает сетчатку глаза от вредного воздействия ультрафиолета. Повысить иммунитет и уменьшить вероятность появления осложнений после лечения глаукомы поможет прием витамина С. Для улучшения состояния глаза при глаукоме, существуют комплексы витаминов и минералов, благотворно влияющих на состояние всех зрительных систем.
Медикаментозное лечение глаукомы у пожилых людей, равно как и в детском возрасте до 18 лет, имеет свои особенности. В таком случае рекомендованы дополнительные обследования и более тщательный подбор щадящих антиглаукомных препаратов.
Лечение закрытоугольной глаукомы
Лечение закрытоугольной глаукомы проходит в несколько этапов, включая подготовительный. Основной метод лечения заболевания такого типа – хирургический.
- Острая форма. Лечение включает применение препаратов, сужающих зрачок, снижающих внутриглазное давление, а также выполнение лазерного или хирургического вмешательства. При таком диагнозе лазерное вмешательство могут выполнить и на второй, менее поврежденный глаз, для предотвращения прогрессирования заболевания и снижения зрения. Хирургическое вмешательство выполняют для улучшения оттока внутриглазной жидкости
- Закрытоугольная форма. При глаукоме с закрытым углом передней камеры рекомендована та же схема лечения, что и при других формах глаукомы закрытоугольного типа.
Эффективность лазера в данном случае многократно подтверждена клинической практикой. Суть метода – искусственное формирование отверстия в радужке глаза, что приводит к нормализации внутриглазного давления. Такой метод позволяет предотвратить последующие острые приступы глаукомы. Лазерное вмешательство также выполняют и при глаукоме у людей с сахарным диабетом. Методика позволяет проводить лечение с учетом особенностей состояния глаза при этом тяжелом сопутствующем заболевании.
Если в сочетании с глаукомой диагностирована катаракта, что нередко встречается у людей пожилого возраста, то наиболее эффективное лечение будет заключаться в удалении помутневшего хрусталика с его заменой на интраокулярную линзу (искусственный хрусталик). Современные модели искусственных хрусталиков настолько совершенны, что в некоторых случаях возможно полное устранение закрытия угла передней камеры глаза.
В более запущенных случаях не обойтись без классической операции.
Хирургические методы лечения глаукомы
Если медикаментозные и малоинвазивные методы лечения глаукомы не эффективны для конкретного пациента, а также если их применение невозможно, выполняют хирургическое вмешательство. Хирургическое лечение глаукомы является наиболее эффективным методом снижения ВГД и сохранения функций зрения, при этом, оно бывает следующих видов:
- Проникающие оперативные вмешательства (трабекулэктомия). Проводится для снижения внутриглазного давления. Суть операции заключается в формировании канала для прохождения внутриглазной жидкости. Операцию выполняют под местной анестезией. После трабекулэктомии назначают противовоспалительные средства и антибактериальные препараты.
- Непроникающее оперативное вмешательство (синусотомия). Суть такой операции – восстановление оттока внутриглазной жидкости (ВГЖ) без непосредственного воздействия на внутриглазные структуры.. Чаще всего рекомендован метод при первичной открытоугольной глаукоме. Операция является сравнительно безопасной, но требующей сложного оборудования и опыта проведения подобных манипуляций со стороны специалиста. Еще одним недостатком метода является отсутствие стабильного послеоперационного эффекта. Для предотвращения избыточного рубцевания протоков ВГЖ и последующего снижения терапевтического эффекта используют различные дренажные системы, наибольшее распространение среди которых получили коллагеновые и гидрогелевые разновидности. Гидрогелевые дренажи совместимы с тканями глаза, не токсичны, биологически инертны.Также широко используют дренаж Ахмеда, и многие офтальмологи справедливо считают его лучшей дренажной системой.
- Криоциклодеструкция. Суть метода – воздействие холодом на цилиарные отростки, вырабатывающие внутриглазную жидкость. Быстрое замораживание и медленное оттаивание целевых клеток ведет к достижению стойкого терапевтического эффекта. Возможно проведение нескольких криогенных аппликаций в зависимости от возраста пациента, типа глаукомы и анамнеза заболевания.
Менее популярные, но также применяющиеся в микрохирургии методы – лазерная, аргоновая, эндоскопическая, ультразвуковая, микроволновая циклодеструкция.
Хирургический метод лечения глаукомы предполагает применение различных имплантов, позволяющих закрепить эффект от инвазивного лечения.
- Аутодренажи позволяют расширить угол передней камеры склеры. Недостатком такого дренажа является быстрое чрезмерное рубцевание и сужение путей оттока жидкости.
- Аллодренажи создаются из материала донора, то есть являются биологическими единицами. Наиболее известным является аллогенный биоматериал «Аллоплант».
- Эксплантодренажи создают из полимерных материалов. Чаще всего в хирургии применяются дренажи из гидрогеля и силикона. Однако по последним исследованиям применение силиконовых дренажей приводит к повторному повышению ВГД.
В целом хирургическое вмешательство направлено на искусственное создание нового канала для оттока ВГЖ, что способствует стойкому снижению внутриглазного давления и замедлению деструктивных процессов в склере и зрительном нерве.
Лечение вторичной глаукомы
Вторичную глаукому лечат в несколько этапов. Проводят терапию заболевания, которое вызвало развитие глаукомных процессов. Острое первичное заболевание купируют кортикостероидами, антибактериальными препаратами, а при хроническом течении к терапии добавляют иммуностимулирующие препараты. При необходимости проводят медикаментозное, малоинвазивное или хирургическое лечение осложнений. Далее разрабатывают схему лечения вторичной глаукомы:
- Для улучшения оттока внутриглазной жидкости применяют альфа- и бета-адреноблокаторы (тимолол, проксодолол), комбинированные препараты (проксофелин, фотил форте).
- Для устранения воспалительных процессов иногда назначают кортикостероиды, нестероидные противовоспалительные препараты, антигистаминные средства.
При вторичной глаукоме использование только медикаментозного метода лечения малоэффективно и фармакотерапию проводят только как вспомогательный способ лечения до устранения основной причины заболевания.
Лазерные и микрохирургические методы лечения вторичной глаукомы включают использование терапевтических и хирургических лазеров, а в более сложных случаях – пластику радужки, замену хрусталика, установление дренажной системы, склеропластические вмешательства.
Лечение пигментной глаукомы
Довольно редкой формой глаукомы является пигментная, но ее лечение в целом не отличается от методик, применяемых при других типах глаукомы. Для лечения пигментной глаукомы часто назначают препараты, сужающие зрачок(пилокарпин, карбохолин и другие). В данном случае миотики являются препаратом первого ряда при выборе медикаментозных средств, снижающих ВГД. Также применяют ингибиторы карбоангидразы и простагландины. При неэффективности консервативных методов лечения выполняют хирургическое вмешательство. При начальных стадиях пигментной глаукомы эффективна лазерная иридотомия, то есть создание микроскопических отверстий в радужке глаза…Из микрохирургических вмешательств при пигментной глаукоме широкое распространение получила непроникающая глубокая склерэктомия.
Лечение неоваскулярной глаукомы
На ранних этапах глаукомы с рубеозом радужки проводят панретинальную фотокоагуляцию (то есть воздействие лазером на все области сетчатки), которая устраняет новообразованные сосуды и препятствует дальнейшему развитию патологии. У пациентов с сахарным диабетом или диагностированной отслойкой сетчатки выполняют ретинальную хирургию в некоторых случаях с лазерной коагуляцией.
Лечение врожденной глаукомы
Существуют медикаментозные методы лечения врожденной глаукомы, направленные на снижение внутриглазного давления (гипотензивные препараты). Однако устранить полностью врождённую глаукому одними лишь таблетками и каплями невозможно. Лекарственные препараты применяют во время постоперационного периода для профилактики чрезмерного рубцевания, сохранения зрения (нейротрофики), общего укрепления организма. Лечение детской глаукомы другой этиологии осуществляется максимально щадящими малоинвазивными методами. Традиционную операцию назначают лишь в самых запущенных случаях, а также, если другие методы являются неэффективными или запрещены по медицинским показаниям.
Сколько стоит лечение глаукомы?
Одной из самых дорогих видов операции является глубокая склерэктомия, а также операции с установкой дренажей (в связи со стоимостью самих дренирующих устройств). Затраты на лечение глаукомы включают проведение необходимой диагностики, анестезии, собственно операции и послеоперационной реабилитации. Современные методы лечения глаукомы малоинвазивны и позволяют минимизировать стоимость вмешательств.
Новые методы лечения глаукомы
Наука не стоит на месте, постоянно разрабатываются новые методы лечения этого опасного заболевания. Так, ученые из Новосибирска разработали первый в мире биопротез. Этот биодренаж состоит из искусственных и биологических материалов и максимально схож с тканями глаза. Ученые проводят активные клинические испытания многообещающей чудо-новинки.
Еще один новый метод лечения глаукомы уже прошел испытания и начал активно использоваться в микрохирургии глаза. Система Ex-PRESS – трехмиллиметровый дренаж, который имплантируют посредствам сверхтонкого проникновения, равного объему инсулиновой иглы. Это делает методику максимально безопасной и менее травматичной, позволяет избежать перепадов давления внутри глаза во время хирургических манипуляций. Имплантация системы обеспечивает образование стабильно функционирующего канала оттока избыточной внутриглазной жидкости. Таким образом, система Ex-PRESS сочетает в себе безопасность непроникающих операций и эффективность классических хирургических методик.
 Автор: врач-офтальмолог Курьянова Ирина Валентиновна
Автор: врач-офтальмолог Курьянова Ирина Валентиновна
Дата публикации: 22.04.2019 9:40
Читайте также
- Глаукома: что это за болезнь. Что нужно знать о глаукоме
- Эффективное лечение глаукомы народными средствами и методами -упражнения, травы, пиявки и масла
- Как распознать глаукому-симптомы на ранних стадиях у взрослых и детей
- Почему возникает глаукома глаза: причины развития заболевания у взрослых и детей
- Как проводят диагностику глаукомы. Современные методы исследования
Источник

