Максимальная гипотензивная терапия при глаукоме
Еричев В.П.
ФГБУ «НИИГБ» РАМН, Москва
Глаукома – одно из основных заболеваний органа зрения, приводящее к необратимой слепоте и слабовидению. По прогнозам Всемирной Организации Здравоохранения к 2020 году значительно возрастет число больных глаукомой, увеличится и число слепых вследствие этого заболевания. Сейчас в России на диспансерном учете находится чуть более 1 065 тыс. больных глаукомой и около 600 тыс. не знают о своем заболевании. Для глаукомы характерно чаще всего бессимптомное течение, что создает большие трудности в ее ранней диагностике, а лечение в далекозашедших стадиях не всегда эффективно.
***
За более чем полуторавековой период существования глаукомы как медицинской проблемы изменилось наше представление об этом заболевании. Раньше глаукома ассоциировалась исключительно с повышенным внутриглазным давлением (ВГД). И это представление доминировало более века, определяя цель лечения: снижение внутриглазного давления. Теперь же под глаукомой понимают нейропатию, и, по версии Европейского глаукомного общества, ПОУГ трактуется как хроническая прогрессирующая оптическая нейропатия, которая объединяет группу заболеваний с характерными морфологическими изменениями головки зрительного нерва (экскавация) и слоя нервных волокон сетчатки при отсутствии другой офтальмопатологии и врожденных аномалий. Для данного заболевания характерны прогрессирующая гибель нейронов сетчатки и возникновение дефектов поля зрения. Как видно, в этом определении нет даже упоминания о внутриглазном давлении. Но парадокс заключается в том, что при формулировании новой цели лечения – сохранение зрительных функций – снижение внутриглазного давления остается единственно доказанной эффективной стратегией в лечении этого заболевания. И все усилия, направленные на реализацию этой стратегии, следует считать вполне оправданными до тех пор, пока мы не будем знать действительную причину возникновения глаукомы и все звенья патогенеза этого тяжелейшего заболевания.
Основная цель лечения глаукомы – сохранение и поддержание зрительных функций на протяжении всего периода жизни пациента при приемлемом качестве жизни. Зрительные функции, качество жизни, лекарственная терапия и приверженность больного лечению – взаимосвязанные и взаимозависимые понятия. В значительной мере на степень реализации поставленных перед врачом задач могут оказать влияние стадия и скорость прогрессирования заболевания, возраст пациента, адекватность избранной терапии. В любом случае предусматривается комплексный подход к терапии этого заболевания. Эффективной и доказанной стратегией в лечении глаукомы является снижение внутриглазного давления до уровня индивидуальной нормы, при которой создаются условия для сохранения зрительных функций.
Как правило, лечение больных глаукомой начинают с назначения препаратов местного гипотензивного действия. При этом следует учитывать ряд общепринятых принципов, выполнение которых позволит сделать лекарственную терапию наиболее эффективной и безопасной.
После верификации диагноза глаукомы врач делает выбор в пользу того или иного лекарственного средства, снижающего внутриглазное давление, принимая во внимание ряд факторов: длительность заболевания, возраст пациента, скорость прогрессирования глаукомной оптической нейропатии, исходный уровень офтальмотонуса, стадию заболевания, соматический статус. Правильная оценка клинической ситуации очень важна, так как она поможет врачу добиться максимальной эффективности и безопасности. Под эффективностью в данном случае следует понимать снижение офтальмотонуса до уровня индивидуальной нормы (давление цели) с минимальными суточными колебаниями его значений. Безопасность предполагает минимум нежелательных явлений местного и системного характера.
Лекарственные препараты, применяемые для гипотензивной терапии, делят на препараты первого и второго выбора. К препаратам первого выбора относят: простагландины/простамиды (латанопрост, травопрост, тафлупрост, биматопрост), неселективный бетаадреноблокатор тимолол малеат. К препаратам второго выбора относят: селективный бета-адреноблокатор бетаксолол, бинарный альфа-бета-адреноблокатор проксодолол, ингибиторы карбоангидразы (дорзоламид, бринзоламид), селективный альфа2-адреномиметик бримонидин, М-хилиномиметик пилокарпин. Это деление условно, и препаратом первого выбора может стать любой из перечисленных, если врач посчитает его наиболее предпочтительным для достижения максимального снижения внутриглазного давления, исходя из конкретной клинической ситуации.
Все лекарственные средства, применяемые для местной гипотензивной терапии, делят на две основные группы в зависимости от механизма действия:
– лекарственные средства, улучшающие отток внутриглазной жидкости;
– лекарственные средства, уменьшающие продукцию внутриглазной жидкости.
Препараты, улучшающие отток внутриглазной жидкости
К препаратам этой группы относятся простагландины и М-холиномиметики (парасимпатомиметики).
Простагландины: синтетические аналоги простагландина F2α латанопрост 0,005% и полный агонист простагландиновых FP-рецепторов травопрост 0,004%, тафлупрост 0,0015%, биматопрост 0,03%. Фармакологическое действие препаратов этой группы заключается в стимулировании FP-рецепторов, расположенных в данном случае в цилиарном теле. Это приводит к снижению внутриглазного давления, в основном за счет улучшения увеосклерального оттока. Максимальный гипотензивный эффект отмечен через 8-12 часов после инстилляции, сохраняется в течение 24 часов и может нарастать в течение 3-4 недель при регулярном применении препарата. На основании метаанализа, препараты этой группы обладают самым выраженным гипотензивным эффектом в сравнении с другими лекарственными средствами, применяемыми в качестве монотерапии.
Режим дозирования – 1 капля 1 раз в сутки, предпочтительно перед сном.
Местные нежелательные явления. Чувство жжения, усиление роста ресниц; при длительном применении препарата возможна обратимая пигментация кожи век; усиление пигментации радужной оболочки; гиперемия слизистой, в большинстве случаев проходящая (чаще встречается при применении травопроста и в случае хорошей гипотензивной эффективности не является поводом для отмены препарата). Роль простагландинов в развитии макулярного отека не доказана.
Системные нежелательные явления крайне редки.
С осторожностью следует применять при уже имеющихся факторах риска: макулярный отек, увеит, экстракция катаракты, выполненная с осложнениями, бронхиальная астма.
Лекарственное взаимодействие. Совместное применение с бета-блокаторами и ингибиторами карбоангидразы усиливает гипотензивный эффект. Нежелательна комбинация с пилокарпином, но если она неизбежна, целесообразно добавлять простагландин к пилокарпину.
М-холиномиметики (парасимпатомиметики)
Пилокарпин 1%, 2%, 4% и 6%.
Фармакологическое действие. Стимулирует М-холинорецепторы вегетативной нервной системы, сокращая волокна цилиарной мышцы. Вызывает миоз, что делает доступ внутриглазной жидкости к дренажной зоне угла передней камеры более свободным и, как следствие, улучшение оттока камерной влаги. Максимальный гипотензивный эффект наступает через 1-1,5 часа после инстилляции, продолжительность его составляет 4-10 часов и зависит от лекарственной формы (длительность гипотензивного эффекта увеличивается в случае использования в качестве пролонгатора таких растворителей, как метилцеллюлоза, карбоксиметилцеллюлоза, поливиниловый спирт).
Режим дозирования. Как правило, используют 1-2% раствор до 4 раз в сутки. Пролонгированные формы позволяют сократить число инстилляций до 2-3 раз в сутки.
Местные нежелательные явления. Вызываемый пилокарпином миоз может сопровождаться спазмом аккомодации с возможными болевыми ощущениями в височной и периорбитальной областях; миопизацией (иногда значительной); сужением поля зрения; снижением остроты зрения у пациентов с центральными помутнениями в хрусталике. При длительном применении могут образовываться пигментные кисты по зрачковому краю, аллергический дерматит век, конъюнктивит. Длительный миоз создает неблагоприятные условия для нормального функционирования периферических отделов сетчатки.
Системные нежелательные явления. Возникают нечасто и связаны с воздействием на М-холинорецепторы. Среди них – бронхоспазм, усиление перистальтики кишечника, потливость, слюноотделение.
Противопоказания. Воспалительные заболевания (иридоциклит, увеит, увеоподобный синдром Познера-Шлоссмана), миопия, сопровождающаяся дистрофическими изменениями сетчатки; ядерная катаракта; заболевания роговицы; бронхоспастические явления; нарушение мочеиспускания; заболевания желудочно-кишечного тракта.
Лекарственное взаимодействие. Возможно усиление гипотензивного эффекта при совместном применении с бета-блокаторами, но при этом возможно и усиление нежелательных явлений системного характера.
Лекарственные средства, снижающие продукцию внутриглазной жидкости
К препаратам, механизм гипотензивного действия которых обусловлен снижением продукции внутриглазной жидкости, относят:
– адреноблокаторы (бета-адреноблокаторы, альфа- и бета-адреноблокаторы);
– ингибиторы карбоангидразы;
– альфа2-адреномиметики.
Адреноблокаторы по характеру действия на бета-адренорецепторы делят на: неизбирательные (неселективные) и избирательные (селективные).
Неселективный бета-адреноблокатор – тимолола малеат 0,25% и 0,5%.
Фармакологическое действие. Блокирует расположенные в цилиарном теле бета-адренорецепторы, уменьшая продукцию внутриглазной жидкости, что и приводит к снижению внутриглазного давления. Максимальный гипотензивный эффект наступает через 2-3 часа и сохраняется в течение 12-24 часов после инстилляции. Необходим особо тщательный контроль за гипотензивным действием препаратов этой фармакологической группы, так как нередко возможно развитие привыкания (тахифилаксии) в разные сроки после начала лечения.
Режим дозирования. С учетом длительности гипотензивного эффекта после одной инстилляции оптимальный режим – по 1 капле 2 раза в день. Рекомендации уменьшить число инстилляций в случае стойкой нормализации офтальмотонуса необоснованны.
Местные нежелательные явления. Непродолжительное жжение, резь, ощущение сухости. При длительном применении редко точечная субэпителиальная кератопатия.
Системные нежелательные явления. Брадикардия; аритмия; бронхоспазм; системная артериальная гипотензия, особенно в ночное время, что может быть дополнительным фактором риска прогрессирования глаукомной оптической нейропатии. При длительном применении повышает уровень сывороточных липидов, что создает риск развития кардиоваскулярных осложнений. Возможно появление сонливости и депрессии.
Противопоказания. Обструктивные заболевания дыхательной системы, бронхиальная астма, сердечно-легочная недостаточность, нарушение сердечного ритма, брадикардия, устойчивая системная гипотензия.
Лекарственное взаимодействие. Сочетанное применение адреноблокаторов с простагландинами F2α, ингибиторами карбоангидразы, М-холиномиметиками и симпатомиметиками гипотензивный эффект усиливает. В случаях одновременного приема пациентами блокаторов кальциевых каналов, препаратов наперстянки, сердечных гликозидов возможно аддитивное действие, сопровождающееся гипотензией, нарушением сердечного ритма, брадикардией.
Страницы: 1 2 3
Источник
Статья посвящена эффективности максимальной гипотензивной терапии с применением фиксированных комбинаций при лечении первичной открытоугольной глаукомы
DOI: 10.21689/2311-7729-2016-16-4-181-184
Введение
ПОУГ остается одной из ведущих причин слабовидения и неизлечимой слепоты и в настоящее время является главным инвалидизирующим заболеванием глаз у взрослых [1, 2]. Традиционно большинство пациентов с ПОУГ получают местное гипотензивное лечение. Известно, что для достижения компенсации уровня ВГД, стабилизации процесса и сохранения зрительных функций нередко возникает необходимость использовать комбинации нескольких препаратов [3, 4]. В частности, максимальная медикаментозная терапия (ММТ) включает применение как минимум 3-х компонентов из разных классов, причем для этого наиболее целесообразно использовать фиксированные комбинации. Последние способствуют повышению эффективности и комплаентности лечения, уменьшению числа и степени выраженности осложнений и НЯ, в т. ч. из-за отсутствия эффекта вымывания, уменьшения воздействия консервантов и т. д. [5, 6].
ММТ может быть рекомендована больным, у которых не достигнута нормализация ВГД (с учетом давления цели) как альтернатива лазерному лечению или хирургическому вмешательству. Кроме того, она может быть полезной и у пациентов с прогрессирующим течением заболевания для максимального снижения офтальмотонуса, несмотря на его контролируемый среднестатистический уровень.
Появление на фармацевтическом рынке Российской Федерации новых оригинальных гипотензивных препаратов обусловливает необходимость собственной их оценки. В связи с этим наше внимание привлекли комбинации неселективного бета-адреноблокатора тимолола с альфа-2 высокоселективным адреномиметиком – бримонидином (препарат Комбиган) и простамидом – биматопростом (Ганфорт). Гипотензивное действие тимолола 0,5%, входящего в состав указанных препаратов, обеспечивается снижением продукции внутриглазной жидкости (ВГЖ) посредством блокады бета-адренорецепторов в цилиарном теле. Бримонидин тартрат 0,2% не только снижает продукцию ВГЖ, стимулируя альфа-2 адренорецепторы, но и увеличивает увеосклеральный отток. Биматопрост 0,03%, помимо увеличения последнего, повышает отток и через чувствительную к давлению трабекулярную сеть [7, 8].
Цель: изучение эффективности и переносимости применения одновременно 2-х фиксированных комбинаций оригинальных гипотензивных препаратов – 0,03% биматопроста / 0,5% тимолола и 0,2 % бримонидина / 0,5% тимолола у больных ПОУГ.
Материал и методы
ММТ в связи с отсутствием компенсации ВГД была назначена 31 больному (37 глаз) с развитой (13 глаз, 35,1%) и далеко зашедшей (24 глаза, 64,9%) стадиями ПОУГ (в т. ч. 7 пациентам с прогрессированием заболевания, которые по тем или иным причинам отказались от предложенной операции). По сути, все больные были потенциальными кандидатами на хирургическое лечение. Возраст пациентов – от 58 до 75 лет (в среднем – 65,9±6,5 года). Среди пациентов было 14 женщин (45,2%) и 17 мужчин (54,8%). Указанное местное лечение включало использование 2-х фиксированных комбинаций: 0,03% биматопроста / 0,5% тимолола и 0,2% бримонидина / 0,5% тимолола с кратностью инстилляций 1 р./сут утром и вечером соответственно. До назначенной ММТ пациенты получали как моно-, так и нефиксированную и фиксированную гипотензивную терапию. В частности, непосредственно до ММТ больные закапывали Ксалатан (6 глаз), Траватан (2), Глаупрост (2), Ксалаком (5), Дуотрав (2), Дорзопт + и Глаупрост (4), Ксалаком и Азаргу (2), Ксалаком и Косопт (2), Ксалаком и Дорзопт (1), Дорзопт + и Траватан (2), Дуотрав и Дорзопт (3), Траватан и Азаргу (3), Косопт и Глаупрост (1) Дорзопт и Глаупрост (2). Следует отметить, что никто из пациентов никогда раньше не применял (не назначали) препараты, содержащие биматопрост и/или бримонидин.
Средний уровень исходного офтальмотонуса на фоне указанной местной гипотензивной терапии составил 33,9±3,5 мм рт. ст. (с колебаниями офтальмотонуса на фоне указанной терапии от 30 до 40 мм рт. ст.). Эффективность назначенной терапии оценивали через 1 сут, и если достигалась нормализация ВГД, то через 1, 3 и 6 мес. У всех пациентов использовали стандартное офтальмологическое обследование, кроме того, у 12 больных применяли компьютерную периметрию (Autoperimetr Dicon LD 400 (США) по пороговой программе 30-2) и у 8 пациентов – конфокальную лазерную сканирующую офтальмоскопию с использованием HRT-III Heidelberg Engineering (Германия). Девять пациенток осуществляли более или менее регулярный самоконтроль АД с фиксацией его показателей в динамике лечения. Сроки диагностирования глаукомы у пациентов до назначения ММТ варьировали от 1 до 7,3 года и в среднем оказались равными 4,1±0,9 года. Псевдоэксфолиативный синдром имел место у 15 (48,4%) больных. Из сопутствующих общесоматических заболеваний все больные имели кардиоваскулярную патологию (ишемическую болезнь сердца, гипертоническую болезнь, преимущественно II стадии, но без инфаркта или инсульта в анамнезе), заболевания желудочно-кишечного тракта (гастрит, колит, холецистит, язву 12-перстной кишки вне обострения и т. п.), а 3 пациента – артрозы коленных суставов обменного характера.
Статистическую обработку данных проводили с помощью программы Statistica 6.1. Рассчитывали групповые показатели суммарной статистики – среднюю арифметическую величину (М) и ошибку средней (m). Различия считались статистически значимыми при р<0,05.
Результаты и обсуждение
Через 1 сут на фоне инстилляций 2-х фиксированных комбинаций гипотензивных капель были обследованы все больные, через 1 мес. – 29 пациентов (35 глаз), через 3 мес. – 27 (32 глаза), через 6 мес. – 22 (26 глаз). Уровень среднего снижения офтальмотонуса через 1 сут после назначенной ММТ (табл. 1) составил 10,2 мм рт. ст., до 23,7±2,5 (35,3%), спустя 1 мес. (без учета не явившихся на обследование 2-х пациентов с ПОУГ на обоих глазах) – 10,4 мм рт. ст., до 23,5±2,1 (36,0%), через 3 мес. (без учета 2-х больных, у которых через 1,5 и 2,5 мес. была все же проведена операция в связи с рецидивом повышенного ВГД и прогрессированием глаукомной оптической нейропатии на фоне ММТ, а также 2-х пациентов, не присутствовавших на обследовании) – 9,3 мм рт. ст., до 24,6±2,3 (32,2%), через 6 мес. (без учета еще 3-х прооперированных глаз спустя 4–5 мес. после назначенной ММТ и 4-х не явившихся на обследование больных) – 8,4 мм рт. ст., до 25,5±2,4 (29,1%). При этом спустя 6 мес. в 19 глазах офтальмотонус находился в пределах среднестатистических значений, т. е. не превышал 26 мм рт. ст. (в т. ч. в 31,6% случаев был достигнут уровень целевого ВГД – ниже 21 мм рт. ст.). В остальных 7 случаях он был стабильно незначительно повышен в пределах 27–29 мм рт. ст. (табл. 2).


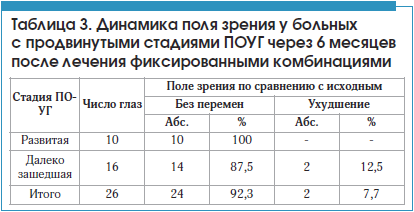
Таким образом, гипотензивная эффективность назначенной ММТ постепенно снижалась и к концу исследования составила 73,1%. При этом необходимо указать, что только в ранние сроки (до 3 мес.) после назначения ММТ в 51,4% случаев удалось добиться снижения офтальмотонуса до рекомендованного уровня соответственно стадии заболевания. Тем не менее зрительные функции подавляющего большинства (в 92,3% случаев) пациентов (за исключением прооперированных и выбывших из исследования) в течение всего срока наблюдения оставались достаточно стабильными (табл. 3), о чем свидетельствовали данные остроты и поля зрения, а также автоматизированной периметрии (табл. 4) на фоне среднестатистической нормы компенсации ВГД или даже слегка повышенного (до 27–29 мм рт. ст.) офтальмотонуса. Кроме того, не было отмечено достоверных отрицательных изменений морфометрических параметров состояния диска зрительного нерва (ДЗН) – в частности, соотношения площади экскавации к площади ДЗН, объема неврального пояска за указанный период лечения.

Что касается переносимости назначенной ММТ, комбинация Ганфорта и Комбигана удовлетворительно оценивалась больными и существенно не влияла на АД. Из побочных эффектов необходимо отметить небольшой кратковременный дискомфорт, жжение, изменение вкуса, на которые обратили внимание 12 больных (38,7%) после закапывания указанных капель. Сухость в глазах, появившаяся спустя примерно 1 мес. после инстилляций назначенных капель у 3-х больных (9,6%), как правило, сочеталась с таковой во рту и была купирована назначением дополнительной слезозаместительной терапии. У 1 пациентки (3,2%) через 5 мес. после указанной терапии был отмечен небольшой отек век, сопровождавшийся незначительным зудом и нерезко выраженными явлениями блефароконъюнктивита, который был купирован инстилляциями Опатанола и Индоколлира. Кроме того, из НЯ назначенного местного гипотензивного лечения следует указать на следы или незначительную (в 17 глазах, 45,9%), умеренную (в 8 глазах, 21,6%) и достаточно выраженную (в 1 случае (2,7%) – у больного ПОУГ, на фоне которой 1 год назад тот перенес тромбоз верхневисочной ветви ЦВС и был все же прооперирован в связи с декомпенсацией ВГД), в основном в глазах со светлой радужкой, невоспалительную конъюнктивальную реакцию. Последняя, на наш взгляд, возникла за счет сосудорасширяющего действия биматопроста в составе Ганфорта. Именно синдром «красного глаза», помимо достаточно высокой стоимости лечения, больше всего беспокоил больных на протяжении всего срока наблюдения. Это, однако, не послужило поводом для отказа пациентов от назначенного лечения (за исключением 5 больных, которые были прооперированы, и 2 пациентов с прогрессированием ГОН на фоне нормализованного или слегка повышенного офтальмотонуса, которые были направлены на селективную лазертрабекулопластику), поскольку ВГД у них все же нормализовалось, а зрительные функции оставались сохранными.
Вывод
ММТ с использованием одновременно 2-х оригинальных фиксированных комбинаций бримонидина/тимолола и биматопроста/тимолола у больных ПОУГ при отдаленных сроках наблюдения (до 6 мес.) обеспечила гипотензивную и функциональную эффективность 73,1%. Отмечено постепенное уменьшение со временем показателя среднего снижения офтальмотонуса: с 35,3% через 1 сут после назначения ММТ до 29,1% спустя 6 мес., что, возможно, было связано с развитием привыкания к тимололу и/или бримонидину. Достаточно серьезным побочным эффектом данной ММТ, на наш взгляд, явилась конъюнктивальная реакция, обусловленная, главным образом, влиянием биматопроста, которая в той или иной степени имела место у большинства больных и вызывала их беспокойство.
Источник


