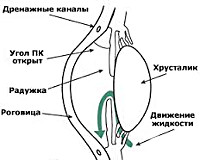
Лазерная иридотомия пигментная глаукома
method of pigment glaucoma
A.G. Schuko, T.N. Yur’eva,
O.P. Mischenko, E.L. Vetarova, O.F. Hantakova
Irkutsk department of FGU «MNTK «Eye Microsurgery» named after acad. Fedorov S.N. Rosmedtechnology»
Purpose: to evaluate effectiveness of laser iridectomy in various stages of pigment dispersion syndrome (PDS).
Materials and methods: Firstly the retrospective analysis of PDS extent among patients of MNTK from 1991 to 2006 was performed. In period from 1991 to 1998 there were 24 of such patients.
Next step was carrying out the prospective randomized ophthalmologic study which included 23 patients with PDS. Average age was 32, 5±4,1 years old. Beside standard examination methods ultrasound biomicroscopy, tonography, stress testing with mydriatics, gonioscopy, diafanoscopy and OCT of optic nerve were made.
All patients had laser iridectomy in anamnesis with reconstructive effect which maintained during the observation period.
Results and conclusion: zsLaser iridectomy in early clinical signs of PDS leads to complete anatomic and reconstructive functional result in 100% of cases.
Пигментная глаукома согласно российской классификации, предложенной А.П. Нестеровым в 1975 г. [1], относится к первичной открытоугольной глаукоме. Европейское общество глаукоматологов в 2002 г. [4] классифицирует пигментную глаукому, как вторичную открытоугольную, обусловленную синдромом пигментной дисперсии (СПД).
Как известно, СПД является латентной стадией пигментной глаукомы [3] и определяется как состояние, когда экзопигмента еще недостаточно для формирования необратимых изменений трабекулы, которые приводят к стойким нарушениям гидродинамики глаза, развитию глаукомной нейрооптикопатии и формированию собственно пигментной глаукомы.
СПД развивается в юношеский период, характеризующийся завершением морфофункционального развития глаза, когда радужка и ресничное тело приобретают окончательную структуру и функциональную организацию. При этом миопический глаз, а миопия является одним из главных факторов риска СПД, достигает максимального размера, и в определенных условиях (мидриаз, физические упражнения, прыжки и т.д.), то есть при любой механической деформации радужки, ведущей к вогнутости ее периферической зоны, появляется кратковременный контакт между пигментным листком радужки и зонулярными связками. Это сопровождается выбросом гранул меланина из поврежденного пигментного эпителия радужки в переднюю камеру, приводит к увеличению объема передней камеры, усугубляет пролапс радужки кзади и вызывает формирование обратного зрачкового блока.
Диагностика СПД строится на выявлении типичных клинических признаков. Это: глубокая передняя камера, распыление пигмента на эндотелии роговицы в виде веретена Крукенберга, мелкодисперсная насыпь пигмента на передней поверхности радужки и задней поверхности хрусталика, в стекловидном теле (пигмент по ходу Клокетова канала) и на глазном дне (пигмент перипапиллярно). С использованием диафаноскопии можно выявить периферические щелевидные дефекты радужки в виде радиальных зон трансиллюминации, при проведении гониоскопии?–?прикорневой пролапс радужки, иридодонез и открытый «канавообразный» угол передней камеры с высокой степенью пигментации всех его структур.
СПД в процессе своего развития проходит ряд стадий [2]. Латентная стадия представлена только морфологическими изменениями глаза: глубокая передняя камера, прикорневой пролапс радужки, иридодонез, иридозонулярный контакт, выявляемый при ультразвуковой биомикроскопии. В стадии первых клинических признаков наряду с вышеперечисленными типичными морфологическими изменениями в камерах глаза появляется экзопигмент. В стадии манифестации уже имеют место гидродинамические нарушения – это положительная нагрузочная проба с мидриатиками и снижение коэффициента легкости оттока ниже возрастной нормы (0,28–0,45 мм3/мин мм рт.ст.). При пигментной глаукоме ВГД стойко повышено, имеются признаки глаукомной нейрооптикопатии.
Основным патогенетически обоснованным принципом лечения СПД и пигментной глаукомы является ликвидация обратного зрачкового блока, которая на современном этапе достигается проведением лазерной иридэктомии.
Поэтому целью работы было оценить эффективность лазерной иридэктомии при разных стадиях СПД.
Материал и методы
На первом этапе работы был проведен ретроспективный анализ распространенности СПД среди пациентов ИФ МНТК «Микрохирургия глаза», обратившихся в период с 1991 по 2006 гг. Выявлено, что в период с 1991 по 1998 год число пациентов с СПД составило всего 24 человека. Причем это были больные пигментной глаукомой на одном глазу и СПД в стадии манифестации всех клинических признаков – на другом. Диагностика синдрома была попутной при лечении глаукомы. Начиная с 1999 года, в связи с появлением доступной информации по данной патологии, выявляемость больных СПД резко выросла. Так, за последние 10 лет СПД был диагностирован у 180?пациентов. Средний возраст составил 27,2±3,4 года. Соотношение мужчин и женщин 1:1,3. От числа впервые выявленной глаукомы СПД составил 2,1%. Соотношение СПД с глаукомой, возникшей в данной возрастной группе за этот же период времени (юношеские формы, увеальные, посттравматические, развившиеся на фоне различных синдромов), составило 2:1.
Необходимо обратить внимание на то, что СПД в 99% случаев был выявлен у пациентов, обратившихся за медицинской помощью в отделение рефракционной лазерной хирургии. От общего числа больных с близорукостью, обратившихся в данное отделение за 2005 г., число пациентов с СПД составило 1,4%. Эти данные еще раз подчеркивают социальную значимость данной патологии.
На следующем этапе было проведено проспективное рандомизированное офтальмологическое обследование 23?пациентов, длительно наблюдающихся с диагнозом СПД в глаукомном кабинете ИФ МНТК «МГ». Средний возраст пациентов – 32,5±4,1 года, соотношение мужчин и женщин 1:1,3. Кроме стандартных методов обследования, проводилась ультразвуковая биомикроскопия с целью исключения иридозонулярного контакта, тонография, нагрузочные пробы с мидриатиками, гонио– и диафаноскопия, ОСТ диска зрительного нерва.
Первично, от 1,5 до 17 лет назад (средний срок наблюдения 6,5 лет), СПД в стадии первых клинических признаков был диагностирован в 50% случаев (21 глаз), в стадии манифестации в 28,5 % (12 глаз), пигментная глаукома на 9 глазах (21,5%).
Всем пациентам, принявшим участие в исследовании, ранее была выполнена лазерная иридэктомия (ЛИЭ) с полным анатомо–реконструктивным эффектом (рис. 1), который сохранялся в течение всего срока наблюдения.
Результаты
В результате лазерного лечения пациентов с СПД в стадии первых клинических признаков были достигнуты следующие анатомо–морфологические изменения (табл.?1): произошло достоверное уменьшение глубины передней камеры глаза, что можно объяснить ликвидацией обратного зрачкового блока и возвращением иридо–хрусталиковой диафрагмы в первоначальное положение. У каждого второго пациента появились зоны очищения трабекулы, показатели гидродинамики были стабильными и соответствовали возрастной норме, то есть в 100% случаев была достигнута стабилизация и регресс патологического процесса.
При обследовании пациентов с СПД в стадии манифестации были получены следующие результаты (табл.?2). Так же, как и в первой группе, после проведения ЛИЭ уменьшается глубина передней камеры и снижается ВГД. В 100% случаев появляются зоны очищения, что сопровождается достоверным снижением пигментации трабекулы. Но несмотря на достигнутые в ходе лечения положительные анатомо–морфологические изменения, в 14% случаев наблюдалась отрицательная динамика гидродинамических показателей. В 7% случаев значимое снижение коэффициента легкости оттока внутриглазной жидкости обусловило необходимость назначения медикаментозной гипотензивной терапии. Еще в 7% случаев появились признаки глаукомной нейропатии в виде расширения экскавации зрительного нерва и изменения полей зрения: расширение «слепого» пятна, появление скотом в зоне Бьерума. Такие результаты при данной стадии СПД можно объяснить более глубоким повреждением путей оттока на интратрабекулярном уровне, когда очищение претрабекулярной зоны от меланина не гарантирует восстановления адекватного оттока внутриглазной жидкости. То есть стадию манифестации СПД можно с уверенностью отнести к латентной стадии глаукомы, в которой, кроме лечебных мероприятий, уже необходима грамотная диспансеризация пациента.
При первичном обследовании 5 пациентов (9 глаз) с пигментной глаукомой на 8 глазах диагностирована начальная стадия заболевания, на 1 глазу – развитая стадия. У больных с I стадией глаукомы толерантное ВГД было достигнуто проведением лазерной иридэктомии и дополнительным назначением гипотензивной терапии, у пациента с глаукомой II стадии была проведена гониотрабекулопластика, через 2 года после лазерной хирургии потребовалось проведение НГСЭ. Срок наблюдения за пациентами с пигментной глаукомой в среднем составил 5?лет. В результате проведенных исследований установлено, что с течением времени происходит достоверное уменьшение экзопигмента на эндотелии роговицы и в углу передней камеры (табл.?3), снижение уровня ВГД и улучшение показателей легкости оттока внутриглазной жидкости.
Но несмотря на это у каждого четвертого пациента наблюдалось утяжеление стадии глаукомного процесса, что во всех случаях объяснялось несоблюдением постоянного гипотензивного режима. Патологический процесс протекал бессимптомно, и люди молодого возраста в своем большинстве не понимали цели регулярного применения глазных капель. Поэтому отрицательная динамика глаукомного процесса у данной группы пациентов потребовала проведения длительных разъяснительных бесед и усиления гипотензивной терапии. В 29% случаев медикаментозная терапия не обеспечила нормализации ВГД, что явилось показанием к лазерному (гониотрабекулопластика) и хирургическому лечению.
На основании вышесказанного можно сделать следующие выводы:
1) СПД является актуальной и социально–значимой проблемой офтальмологии в связи с его распространенностью среди населения молодого и трудоспособного возраста.
2) Лазерная иридэктомия при СПД в стадии первых клинических признаков приводит к достижению полного анатомо–реконструктивного и функционального результата в 100% случаев.
3) При СПД в стадии манифестации лазерная иридэктомия приводит к положительным морфологическим изменениям в 100% случаев, стабилизации глаукомного процесса в 86% случаев.
4) При пигментной глаукоме лазерная иридэктомия необходима как 1–й этап лечебных мероприятий для ликвидации обратного зрачкового блока.
Таким образом, лазерную иридэктомию можно считать методом профилактики пигментной глаукомы, которая приводит к выздоровлению пациентов в стадии первых клинических признаков и к стабилизации процесса в большинстве случаев в стадии манифестации.
Источник
Вопрос обзора
Каковы эффекты периферической лазерной иридотомии в сравнении с другими методами лечения или отсутствием лечения у пациентов с синдромом пигментной дисперсии или пигментной глаукомой?
Актуальность
Глаукома — хроническое заболевание глаз, ассоциированное с потерей зрения с течением времени. Одним из основных факторов риска глаукомы является повышенное давление в глазу, известное как глазная гипертензия. При синдроме пигментной дисперсии (СПД) частицы радужки (окрашенная часть глаза) отрываются от радужки и оседают на других частях внутри глаза. Иногда эти частицы блокируют отток жидкости из передней части глаза, что приводит к глазной гипертензии. Пигментная глаукома представляет собой специфическую форму глаукомы, которая может быть обнаружена у пациентов с СПД. Местная медикаментозная терапия, как правило, является терапией первой линии; вместе с тем в качестве альтернативного лечения предложена периферическая лазерная иридотомия.
Периферическая иридотомия — это процедура, которая выполняется с помощью лазера. Лазерный луч света используют, чтобы выжечь небольшое отверстие в радужке для свободного перемещения жидкости внутри передней части глаза. Цель этой процедуры заключается в снижении давления внутри глаза, снижая тем самым вероятность глаукомы и/или потери зрения. Однако неизвестно, уменьшает ли периферическая иридотомия развитие или прогрессирование пигментной глаукомы на практике.
Детали исследования
Мы провели поиск по различным электронным базам данных для выявления рандомизированных контролируемых испытаний, оценивающих эффективность периферической иридотомии у людей с СПД или пигментной глаукомой. Мы включили пять испытаний с общим числом 260 глаз у 195 участников. Доказательства актуальны на 2 ноября 2015.
Основные результаты
Мы не нашли очевидной пользы от проведения периферичекой лазерной иридотомии в сравнении с её отсутствием при СПД или пигментной глаукоме при измерении эффекта в единицах — предотвращение потери поля зрения. Доказательства очень низкого качества позволяют предполагать, что лазерная иридотомия может быть более эффективной в снижении давления внутри глаза по сравнению с отсутствием лазерной иридотомии в течение периода длительностью до 10 лет после лечения. У участников этих испытаний было отмечено небольшое число неблагоприятных эффектов; наиболее частыми побочными эффектами были легкое послеоперационное воспаление и катаракта.
Качество доказательств
Мы оценили качество доказательств как очень низкое в результате плохого представления методов исследования, неполной информации для содержательного анализа данных, а также вариаций в исходах, оцениваемых в разных испытаниях. В заключение, недостаточно доказательств, чтобы поддержать использование периферической иридотомии как способа лечения пигментной глаукомы. Необходимы хорошо спланированные рандомизированные контролируемые испытания для оценки эффективности и безопасности периферической иридотомии при СПД и пигментной глаукоме.
Заметки по переводу:
Перевод: Кораблева Анна Александровна. Редактирование: Зиганшина Лилия Евгеньевна. Координация проекта по переводу на русский язык: Cochrane Russia — Кокрейн Россия (филиал Северного Кокрейновского Центра на базе Казанского федерального университета). По вопросам, связанным с этим переводом, пожалуйста, обращайтесь к нам по адресу: lezign@gmail.com
Источник
При лечении глаукомы лазерную иридэктомию используют в тех же случаях, что и другие методики хирургического вмешательства.

Показания
Чаще операцию ЛИЭ назначают при смешанном типе глаукомы и при закрытоугольной глаукоме первичной и вторичной этиологии. Лазерная иридэктомия является дополнительной мерой, которую применяют после основной операции в случае неполной эксцизии радужки или же при закрытии колобомы отложением пигмента и спайками. Кроме того, лазерную иридэктомию можно выполнить в качестве профилактической меры при односторонней глаукоме закрытоугольного типа первичного генеза. Это позволит предотвратить развитие внутриглазной гипертензии с противоположной стороны. Лазерная иридэктомия иногда является предварительным этапом перед проведением трабекулопластики пациентам с открытоугольной глаукомой и относительно узким профилем угла передней камеры.
Противопоказания
Противопоказано выполнение лазерной операции при помутнении роговицы, отеке ее вещества и недостаточной глубине передней камеры глаза.
Характеристики лазеров
Для выполнения операции используют лазеры различных типов (непрерывного действия аргоновые или короткоимпульсные). Чтобы облегчить проведение манипуляции, можно использовать контактную линзу Абрахама, которая имеет антирефлектирующее покрытие, а также специальный оптический элемент плоско-выпуклой формы с оптической силой +66 диоптрий. После прохождения через этот элемент на уровне роговицы диаметр лазерного луча удваивается вдвое. Далее на уровне радужки диаметр луча становится в четыре раза меньше (в два раза меньше по сравнению с исходной величиной). Таким образом, повреждающее влияние лазерного луча на вещество роговицы значительно уменьшается, а на радужки возрастает в четыре раза.
Суть иридэктомии
Перед проведением манипуляции глаз пациента обезболивают при помощи эпибульбарной анестезии. Также необходимо сузить зрачок путем закапывания 1% раствора пилокарпина.
Местом нанесения лазерного отверстия может быть любой квадрат радужки. При этом зона на 12 часов является не желательной, потому что в этой области могут скапливаться пузырьки газа, связанные с работой лазера. Лучше найти истонченный участок радужной оболочки или же крупную крипту.
Техника лазерной иридэктомии может быть различной. Эффективность каждой из них определяется цветом радужки, ее толщиной и структурой.
Видео, как проходит операция
Послойная иридэктомия
Послойная методика эффективна у пациентов с карим цветом глаз. При этом лазерные аппликации имеют мощность 700-1500 мВт, продолжительность 0,2 с, а диаметр 50 мкм. Строму радужки выжигают путем формирования постепенно углубляющегося кратера. Для вскрытия пигментного слоя радужной оболочки используют аргоновый (50-100 мкм, 0,1-0,2 с, 500-600 мВт) или короткоимпульсный YAG-лазер (30 мкм, 5-15 мДж).
Поэтапная иридэктомия
Для выполнения поэтапной иридэктомии необходимо провести 2-5 сеансов, перерыв между которыми составляет 2-3 недели. Эта методика обычно применяется у пациентов со светлой радужкой. После каждого сеанса истонченная строма радужной оболочки постепенно пигментируется. Всего нужно нанести около 30-60 аппликаций с параметрами мощности 600-1000 мВт, времени 0,2-0,5 с, диаметра 50-100 мкм. Недостатком методики является высокая вероятность формирования синехий, развития вялотекущего увеита и длительность процедуры.

Одномоментная иридэктомия
Для выполнения одномоментной иридэктомии используют импульсный YAG-лазер. Количество аппликаций составляет от 1 до 3 при мощности 5-15 мДж. Эффективность методики не зависит от цвета радужки.
Несмотря на техническое развитие, не всегда при лазерной иридэктомии удается получить сквозное отверстие в радужке. В ряде случаев происходит закрытие отверстия за счет формирования синехий или отложения пигмента, тогда необходимо провести повторное лазерное лечение.
Стоимость лазерной операции
Цена периферической лазерной иридэктомии в нашем офтальмологическом центре составляет 8 500 рублей (за 1 глаз). Со стоимостью других лазерных методов лечения глаукомы и возможностями нашей клиники в лечении и диагностике глаукомы Вы можете ознакомиться в разделе ЦЕНЫ.
Источник
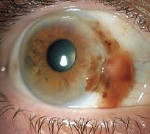
Пигментная глаукома – это чаще бинокулярная патология органа зрения, в основе развития которой лежит дегенерация пигментного эпителия. Симптомами данной патологии являются появление «кругов радуги» или «тумана» перед глазами, нарушение аккомодации, головная боль, распространяющаяся на глазницу и надбровные дуги. Диагностика включает в себя сбор анамнеза, проведение биомикроскопии, офтальмоскопии, тонометрии, визиометрии, гониоскопии и периметрии. Консервативная терапия сводится к приему миотиков. В зависимости от тяжести пигментной глаукомы возможно проведение лазерной трабекулопластики, иридотомии, иридэктомии или трабекулэктомии.
Общие сведения
Пигментная глаукома – это одна из форм открытоугольной глаукомы, при которой повышение ВГД является следствием отложения гранул меланина в переднем сегменте глаза. Первое описание пигментной глаукомы было представлено в 1949 году ученым С. Шугаром. Распространенность среди других форм составляет 1-1,4%. Лица мужского пола более подвержены риску развития данной патологии (около 85% случаев), чем женщины. Как правило, пигментной глаукомой страдают люди трудоспособного возраста (от 16 до 65 лет). Пик заболеваемости среди мужчин наблюдается в возрасте 35 лет, среди женщин – в возрасте 50 лет. Заболевание более распространено среди лиц со светлой кожей, чем среди темнокожего населения. В числе пациентов преобладают больные с миопической рефракцией.

Пигментная глаукома
Причины пигментной глаукомы
Триггером пигментной глаукомы является дегенерация пигментного эпителия радужки и цилиарного тела. При этом в основе повышения внутриглазного давления (ВГД) лежит отложение гранул меланина в области переднего сегмента глазного яблока (угол передней камеры, строма радужной оболочки и задняя поверхность роговой оболочки, трабекулярный аппарат). Поражение трабекулярного аппарата усугубляет прогрессирование патологии, т. к. нарушение оттока водянистой влаги стимулирует нарастание ВГД. Кроме того, на фоне дегенеративных процессов происходит репарация пигментного эпителия, который в последующем отторгается.
Механизм развития пигментной глаукомы в ряде случаев неразрывно связан с синдромом пигментной дисперсии (СПД). Вначале СПД протекает как бессимптомная стадия глаукомы. Повышения ВГД не происходит, т. к. имеющееся количество пигмента является недостаточным для провоцирования патологических изменений в трабекулярном аппарате. Пока дегенеративные процессы затрагивают небольшую площадь пигментного слоя, гидродинамика органа зрения находится в пределах нормы, глаукомная нейрооптикопатия не наступает. При выраженной дегенерации развивается клиническая картина пигментной глаукомы. В то же время, у ряда пациентов с СПД в анамнезе показатели ВГД не превышают толерантные значения, декомпенсация данного состояния не наблюдается.
Более высокому риску развития пигментной глаукомы подвержены молодые люди с СПД на фоне миопии в анамнезе. При механических предпосылках к нарушению структуры радужки (занятия спортом, мидриаз, перенапряжение) пигментный слой радужной оболочки контактирует со связочным аппаратом органа зрения, что приводит к отторжению гранул меланина. Гранулы пигмента попадают в переднюю камеру и стимулируют превышение ВГД толерантных значений.
Симптомы пигментной глаукомы
Пигментная глаукома в большинстве случаев поражает одновременного оба глаза. На ранних стадиях заболевание протекает бессимптомно. В последующем пациенты предъявляют жалобы на снижение остроты зрения, появление «тумана», «пелены» или «мушек» перед глазами. Симптомом превышения ВГД толерантных показателей становится развитие головной боли. Боли могут иррадиировать в область глазницы или надбровных дуг. Специфическим симптомом пигментной глаукомы является частое появление кругов «радуги» при взгляде на яркий свет. Это связано с отложением гранул меланина на задней поверхности роговой оболочки. В связи с этим пациенты отмечают появление кругов вне зависимости от уровня ВГД.
Резкое повышение внутриглазного давления при пигментной глаукоме проявляется клинической симптоматикой кратковременного криза. При этом больные жалуются на затуманивание зрения, сопровождающееся резко выраженным усилением всех симптомов болезни. Провоцировать криз может расширение зрачков, физические нагрузки, т. к. данные состояния приводят к отторжению пигмента с его последующим накоплением в передней камере. Значительная часть пациентов с разной частотой ощущает дрожание радужки при движениях зрачка.
Диагностика пигментной глаукомы
Диагностика пигментной глаукомы основывается на анамнестических данных, результатах биомикроскопии, офтальмоскопии, тонометрии, визиометрии, гониоскопии и периметрии. Методом тонометрии определяется повышение ВГД (выше 20 мм. рт. ст.). Однако при нормальных значениях ВГД в случае однократного измерения у пациентов с клиническими проявлениями заболевания исключить диагноз пигментной глаукомы нельзя. При проведении визиометрии у большинства больных выявляется снижение остроты зрения. Периметрия позволяет диагностировать незначительное сужение полей зрения.
Методом биомикроскопии с использованием щелевой лампы обнаруживается распыленный пигмент в области эндотелиального слоя роговицы в форме веретена Крукенберга, отложения меланина в области передней поверхности радужной оболочки и на задней стенке хрусталика. В стекловидном теле пигмент определяется в зоне гиалоидного канала. При проведении офтальмоскопии на глазном дне пигментные отложения имеют перипапиллярную локализацию. Гониоскопия при пигментной глаукоме позволяет определить степень увеличения глубины передней камеры глаза (более 3,5 мм), диагностировать пролапс радужки, проявления иридодонеза, обширную пигментацию в области угла передней камеры.
Вспомогательными методами исследования пигментной глаукомы являются ультразвуковая биомикроскопия, оптическая когерентная томография, проба с мидриатиками. Метод ультразвуковой биомикроскопии позволяет выявить иридозонулярный контакт. При проведении медикаментозной пробы с препаратами, расширяющими зрачок, отмечается положительный результат. Коэффициент легкости оттока ниже нормы (0,28-0,45 мм3/мин). В офтальмологии при помощи оптической когерентной томографии можно более детально визуализировать структурные аномалии органа зрения.
Дифференциальную диагностику пигментной глаукомы необходимо проводить с заболеваниями органа зрения, которые сопровождаются гиперпигментацией и повышением ВГД. При псевдоэксфолиативной глаукоме пигмент может накапливаться только в трабекулярном аппарате, а дефекты радужки локализируются по зрачковому краю. У пациентов преклонного возраста патология часто поражает один глаз. При артифакии возможен контакт структур глаза с поверхностью интраокулярной линзы, что может приводить к дегенерации пигментного слоя и нарушать отток водянистой влаги. Подобная клиническая картина характерна для переднего увеита. В случае подострой закрытоугольной глаукомы повышение ВГД стимулирует гиперпигментацию трабекулярной сети. Для дифференциальной диагностики необходимо провести гониоскопию, которая в случае закрытоугольной глаукомы позволит диагностировать закрытый угол передней камеры глаза в отличие от пигментной глаукомы.
Лечение пигментной глаукомы
Тактика лечения пигментной глаукомы зависит от тяжести заболевания. Пациентам на ранней стадии патологии без сопутствующей миопии в анамнезе показана медикаментозная терапия, заключающаяся в приеме миотиков (холиномиметики и препараты антихолинэстеразного действия). Препараты данной группы снижают степень иридозонулярного соприкосновения и, тем самым, способствуют оттоку водянистой влаги. При отсутствии эффекта от консервативной терапии рекомендовано проведение хирургического вмешательства. В молодом возрасте выполняется лазерная трабекулопластика. Мощность лазерного воздействия определяют в зависимости от выраженности пигментной глаукомы. Для предотвращения деструкции пигментного слоя и устранения клинической симптоматики смещения радужки проводится лазерная иридотомия.
Больным с пигментной глаукомой на фоне синдрома пигментной дисперсии при условии развития зрачкового блока осуществляется лазерная иридэктомия. Данное хирургическое вмешательство можно выполнять в дебюте заболевания. При применении на этапе появления первых симптомов операция показана с профилактической целью. Трабекулэктомия проводится пациентам с трабекулопластикой в анамнезе и резистентностью ко всем методам оперативного и медикаментозного лечения. В послеоперационном периоде рекомендован прием нейропротекторов (витамин Е, флавоноиды).
Прогноз и профилактика пигментной глаукомы
Специфических мер по профилактике пигментной глаукомы не разработано. При развитии первых клинических проявлений заболевания у пациентов с СПД рекомендовано проведение профилактической иридэктомии. Всем больным с подозрением на пигментную глаукому необходимо проходить осмотр у офтальмолога 2 раза в год с обязательным проведением тонометрии, визиометрии, гониоскопии, офтальмоскопии. Все лица с синдромом пигментной дисперсии также должны своевременно проходить обследование для раннего выявления и лечения данной патологии.
Прогноз пигментной глаукомы при своевременной диагностике и лечении для жизни и трудоспособности благоприятный. При отсутствии лечебных мероприятий возможна тотальная потеря зрения с последующей инвалидизацией.
Источник