Глаукома врожденная и приобретенная течение исход
Глаукома – хроническая патология глаз, характеризующаяся повышением внутриглазного давления, развитием оптической нейропатии и нарушениями зрительной функции. Клинически глаукома проявляется сужением полей зрения, болью, резью и ощущением тяжести в глазах, затуманиванием зрения, ухудшением сумеречного зрения, в тяжелых случаях слепотой. Диагностика глаукомы включает в себя периметрию, тонометрию и тонографию, гониоскопию, оптическую когерентную томографию, лазерную ретинотомографию. Лечение глаукомы требует использования антиглаукомных капель, применения методов лазерной хирургии (иридотомии (иридэктомии) и трабекулопластики) или проведения антиглаукоматозных операций (трабекулэктомии, склерэктомии, иридэктомии, иридоциклоретракции и др.).
Общие сведения
Глаукома – одно из самых грозных заболеваний глаз, приводящих к потере зрения. Согласно имеющимся данным, глаукомой страдают около 3 % населения, а у 15% незрячих людей во всем в мире глаукома послужила причиной слепоты. В группе риска по развитию глаукомы находятся люди старше 40 лет, однако в офтальмологии встречаются такие формы заболевания, как юношеская и врожденная глаукома. Частота заболевания значительно увеличивается с возрастом: так, врожденная глаукома диагностируется у 1 из 10-20 тыс. новорожденных; в группе 40-45-летних людей – в 0,1% случаев; у 50-60-летних – в 1,5% наблюдений; после 75 лет – более чем в 3% случаев.
Под глаукомой понимают хроническое заболевание глаз, протекающее с периодическим или постоянным повышением ВГД (внутриглазного давления), расстройствами оттока ВГЖ (внутриглазной жидкости), трофическими нарушениями в сетчатке и зрительном нерве, что сопровождается развитием дефектов поля зрения и краевой экскавации ДЗН (диска зрительного нерва). Понятием «глаукома» сегодня объединяют около 60 различных заболеваний, имеющих перечисленные особенности.
Глаукома
Причины развития глаукомы
Изучение механизмов развития глаукомы позволяет говорить о мультифакторном характере заболевания и роли порогового эффекта в ее возникновении. То есть для возникновения глаукомы необходимо наличие ряда факторов, которые в сумме вызывают заболевание.
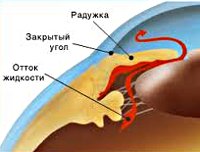
Патогенетический механизм глаукомы связан с нарушением оттока внутриглазной жидкости, играющей ключевую роль в обмене веществ всех структур глаза и поддержании нормального уровня ВГД. В норме вырабатываемая ресничным (цилиарным) телом водянистая влага скапливается в задней камере глаза – щелевидном пространстве, расположенным позади радужки. 85-95% ВГЖ через зрачок перетекает в переднюю камеру глаза – пространство между радужкой и роговицей. Отток внутриглазной жидкости обеспечивается особой дренажной системой глаза, расположенной в углу передней камеры и образованной трабекулой и шлеммовым каналом (венозным синусом склеры). Через эти структуры ВГЖ оттекает в склеральные вены. Незначительная часть водянистой влаги (5-15%) оттекает дополнительным увеосклеральным путем, просачиваясь через ресничное тело и склеру в венозные коллекторы сосудистой оболочки.
Для поддержания нормального ВГД (18-26 мм рт. ст.) необходим баланс между оттоком и притоком водянистой влаги. При глаукоме это равновесие оказывается нарушенным, в результате чего в полости глаза скапливается избыточное количество ВГЖ, что сопровождается повышением внутриглазного давления выше толерантного уровня. Высокое ВГД, в свою очередь, приводит к гипоксии и ишемии тканей глаза; компрессии, постепенной дистрофии и деструкции нервных волокон, распаду ганглиозных клеток сетчатки и в конечном итоге – к развитию глаукомной оптической нейропатии и атрофии зрительного нерва.
Развитие врожденной глаукомы обычно связано с аномалиями глаз у плода (дисгенезом угла передней камеры), травмами, опухолями глаз. Предрасположенность к развитию приобретенной глаукомы имеется у людей с отягощенной наследственностью по данному заболеванию, лиц, страдающих атеросклерозом и сахарным диабетом, артериальной гипертонией, шейным остеохондрозом. Кроме этого, вторичная глаукома может развиваться вследствие других заболеваний глаз: дальнозоркости, окклюзии центральной вены сетчатки, катаракты, склерита, кератита, увеита, иридоциклита, прогрессирующей атрофии радужки, гемофтальма, ранений и ожогов глаз, опухолей, хирургических вмешательств на глазах.
Классификация глаукомы
По происхождению различают первичную глаукому, как самостоятельную патологию передней камеры глаза, дренажной системы и ДЗН, и вторичную глаукому, являющуюся осложнением экстра- и интраокулярных нарушений.
В соответствии с механизмом, лежащим в основе повышения ВГД, выделяют закрытоугольную и открытоугольную первичную глаукому. При закрытоугольной глаукоме имеет место внутренний блок в дренажной системе глаза; при открытоугольной форме – угол передней камеры открыт, однако отток ВГЖ нарушен.
В зависимости от уровня ВГД глаукома может протекать в нормотензивном варианте (с тонометрическим давлением до 25 мм рт. ст.) или гипертензивном варианте с умеренным повышением тонометрического давления (26-32 мм рт. ст.) либо высоким тонометрическим давлением (33 мм рт. ст. и выше).
По течению глаукома может быть стабилизированной (при отсутствии отрицательной динамики в течение 6 месяцев) и нестабилизированной (при тенденции к изменениям поля зрения и ДЗН при повторных обследованиях).
По выраженности глаукомного процесса различают 4 стадии:
- I (начальная стадия глаукомы) – определяются парацентральные скотомы, имеется расширение оптического диска, экскавация ДЗН не доходит до его края.
- II (стадия развитой глаукомы) – поле зрения изменено в парцентральном отделе, сужено в нижне- и/или верхневисочном сегменте на 10° и более; экскавация ДЗН носит краевой характер.
- III (стадия далеко зашедшей глаукомы) – отмечается концентрическое сужение границ поля зрения, выявляется наличие краевой субтотальной экскавации ДЗН.
- IV (терминальная стадия глаукомы) – имеет место полная утрата центрального зрения либо сохранность светоощущения. Состояние ДЗН характеризуется тотальной экскавацией, деструкцией нейроретинального пояска и сдвигом сосудистого пучка.
В зависимости от возраста возникновения выделяют глаукому врожденную (у детей до 3-х лет), инфантильную (у детей от 3-х до 10-ти лет), ювенильную (у лиц в возрасте от 11-ти до 35-ти лет) и глаукому взрослых (у лиц старше 35-ти лет). Кроме врожденной глаукомы, все остальные формы являются приобретенными.
Симптомы глаукомы
Клиническое течение открытоугольной глаукомы, как правило, бессимптомное. Сужение поля зрения развивается постепенно, иногда прогрессирует в течение нескольких лет, поэтому нередко пациенты случайно обнаруживают, что видят только одним глазом. Иногда предъявляются жалобы на затуманивание взгляда, наличие радужных кругов перед глазами, головную боль и ломоту в надбровной области, снижение зрения в темноте. При открытой глаукоме обычно поражаются оба глаза.
В течении закрытоугольной формы заболевания выделяют фазу преглаукомы, острого приступа глаукомы и хронической глаукомы.
Преглаукома характеризуется отсутствием симптоматики и определяется при офтальмологическом обследовании, когда выявляется узкий или закрытый угол передней камеры глаза. При преглаукоме больные могут видеть радужные круги на свету, ощущать зрительный дискомфорт, кратковременную потерю зрения.
Острый приступ закрытоугольной глаукомы обусловлен полным закрытием угла передней камеры глаза. ВГД может достигать при этом 80 мм. рт. ст. и выше. Приступ может провоцироваться нервным напряжением, переутомлением, медикаментозным расширением зрачка, длительным пребыванием в темноте, долгой работой со склоненной головой. При приступе глаукомы появляется резкая боль в глазу, внезапное падение зрения вплоть до светоощущения, гиперемия глаз, потускнение роговицы, расширение зрачка, который приобретает зеленоватый оттенок. Именно поэтому типичному признаку заболевание получило свое название: «glaucoma» переводится с греческого как «зеленая вода». Приступ глаукомы может протекать с тошнотой и рвотой, головокружением, болями в сердце, под лопаткой, в животе. На ощупь глаз приобретает каменистую плотность.
Острый приступ закрытоугольной глаукомы является неотложным состоянием и требует скорейшего, в течение нескольких ближайших часов, снижения ВГД медикаментозным или хирургическим путем. В противном случае больному может грозить полная необратимая потеря зрения.
Со временем глаукома принимает хроническое течение и характеризуется прогрессирующим увеличение ВГД, рецидивирующими подострыми приступами, нарастанием блокады угла передней камеры глаза. Исходом хронической глаукомы служит глаукомная атрофия зрительного нерва и потеря зрительной функции.
Диагностика глаукомы
Раннее выявление глаукомы имеет важное прогностическое значение, определяющее эффективность лечения и состояние зрительной функции. Ведущее значение в диагностике глаукомы играет определение ВГД, детальное изучение глазного дна и ДЗН, исследование поля зрения, обследование угла передней камеры глаза.
Основными методами измерения внутриглазного давления служит тонометрия, эластотонометрия, суточная тонометрия, отражающая колебания ВГД в течение суток. Показатели внутриглазной гидродинамики определяются с помощью электронной тонографии глаза.
Неотъемлемой частью обследования при глаукоме является периметрия – определение границ поля зрения с помощью различных методик – изоптопериметрии, кампиметрии, компьютерной периметрии и др. Периметрия позволяет выявить даже начальные изменения полей зрения, которые не замечаются самим пациентом.
С помощью гониоскопии при глаукоме офтальмолог имеет возможность оценить строение угла передней камеры глаза и состояние трабекулы, через которую происходит отток ВГЖ. Информативные данные помогает получить УЗИ глаза.
Состояние ДЗН является важнейшим критерием оценки стадии глаукомы. Поэтому в комплекс офтальмологического обследования включается проведение офтальмоскопии — процедуры осмотра глазного дна. Для глаукомы характерно углубление и расширение сосудистой воронки (экскавации) ДЗН. В стадии далеко зашедшей глаукомы отмечается краевая экскавация и изменение цвета диска зрительного нерва.
Более точный качественный и количественный анализ структурных изменений ДЗН и сетчатки проводится с помощью лазерной сканирующей офтальмоскопии, лазерной поляриметрии, оптической когерентной томографии или гейдельбергской лазерной ретинотомографии.
Лечение глаукомы
Существует три основных подхода к лечению глаукомы: консервативный (медикаментозный), хирургический и лазерный. Выбор лечебной тактики определяется типом глаукомы. Задачами медикаментозного лечения глаукомы служат снижение ВГД, улучшение кровоснабжения внутриглазного отдела зрительного нерва, нормализация метаболизма в тканях глаза. Антиглаукомные капли по своему действию делятся на три большие группы:
- Препараты, улучшающие отток ВГЖ: миотики (пилокарпин, карбахол); симпатомиметики (дипивефрин); простагландины F2 альфа – латанопрост, травопрост).
- Средства, ингибирующие продукцию ВГЖ: селективные и неселективные ß-адреноблокаторы (бетаксолол, бетаксолол, тимолол и др.); a- и β-адреноблокаторы (проксодолол).
- Препараты комбинированного действия.
При развитии острого приступа закрытоугольной глаукомы требуется незамедлительное снижение ВГД. Купирование острого приступа глаукомы начинают с инстилляции миотика — 1% р-ра пилокарпина по схеме и р-ра тимолола, назначения диуретиков (диакарба, фуросемида). Одновременно с лекарственной терапией проводят отвлекающие мероприятия – постановку банок, горчичников, пиявок на височную область (гирудотерапию), горячие ножные ванны. Для снятия развившегося блока и восстановления оттока ВГЖ необходимо проведение лазерной иридэктомии (иридотомии) или базальной иридэктомии хирургическим методом.
Методы лазерной хирургии глаукомы довольно многочисленны. Они различаются типом используемого лазера (аргонового, неодимового, диодного и др.), способом воздействия (коагуляция, деструкция), объектом воздействия (радужка, трабекула), показаниями к проведению и т. д. В лазерной хирургии глаукомы широкое распространение получили лазерная иридотомия и иридэктомия, лазерная иридопластика, лазерная трабекулопластика, лазерная гониопунктура. При тяжелых степенях глаукомы может выполняться лазерная циклокоагуляция.
Не потеряли своей актуальности в офтальмологии и антиглаукоматозные операции. Среди фистулизирующих (проникающих) операций при глаукоме, наиболее распространены трабекулэктомия и трабекулотомия. К нефистулизирующим вмешательствам относят непроникающую глубокую склерэктомию. На нормализацию циркуляции ВГЖ направлены такие операции, как иридоциклоретракция, иридэктомия и др. С целью снижения продукции ВГЖ при глаукоме проводится циклокриокоагуляция.
Прогноз и профилактика глаукомы
Необходимо понимать, что полностью излечиться от глаукомы невозможно, однако данное заболевание можно держать под контролем. На ранней стадии заболевания, когда еще не произошли необратимые изменения, могут быть достигнуты удовлетворительные функциональные результаты лечения глаукомы. Бесконтрольное течение глаукомы приводит к необратимой потере зрения.
Профилактика глаукомы заключается в регулярных осмотрах окулистом лиц групп риска — с отягощенным соматическим и офтальмологическим фоном, наследственностью, старше 40 лет. Пациенты, страдающие глаукомой, должны находиться на диспансерном учете у офтальмолога, регулярно каждые 2-3 месяца посещать специалиста, пожизненно получать рекомендуемое лечение.
Источник
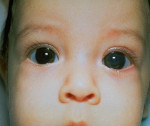
Врожденная глаукома – чаще наследственное заболевание, сопровождающееся постепенным увеличением внутриглазного давления и обусловленными этим сопутствующими зрительными нарушениями. К основным симптомам данной патологии относят увеличение размеров глаз (у грудных детей), болезненность, которая приводит к беспокойству и плаксивости ребенка, светобоязнь, миопию или астигматизм. Диагностика врожденной глаукомы производится на основании данных офтальмологического осмотра, изучения наследственного анамнеза пациента и течения беременности, генетических исследований. Лечение только хирургическое, причем оно должно быть выполнено как можно ранее до развития необратимых вторичных нарушений в органе зрения.
Общие сведения
Врожденная глаукома – генетическое, реже — приобретенное внутриутробно заболевание, которое характеризуется недоразвитием угла передней камеры глаза и трабекулярной сети, что в конечном итоге приводит к повышению внутриглазного давления. Это состояние считается в офтальмологии относительно редким и встречается примерно в одном случае на 10000 родов. Некоторые исследователи полагают, что данная статистика не совсем корректно отражает действительность, ведь некоторые формы врожденной глаукомы могут не проявлять себя вплоть до подросткового возраста. Несмотря на то, что патология наследуется по аутосомно-рецессивному механизму, среди больных несколько превалируют мальчики – половое распределение составляет примерно 3:2. По возрасту развития основных симптомов, а также наличию или отсутствию генетических дефектов выделяют несколько клинических форм этого заболевания. Важность своевременного обнаружения врожденной глаукомы обусловлена тем, что без проведенного лечения ребенок может ослепнуть через 4-5 лет после развития первых проявлений патологии.
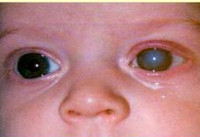
Врожденная глаукома
Причины врожденной глаукомы
Подавляющее большинство случаев врожденной глаукомы (не менее 80%) сопровождаются мутацией гена CYP1B1, который локализован на 2-й хромосоме. Он кодирует белок цитохром Р4501В1, функции которого на сегодняшний момент изучены недостаточно. Предполагается, что данный протеин каким-то образом участвует в синтезе и разрушении сигнальных молекул, которые принимают участие в формирование трабекулярной сети передней камеры глаза. Дефекты структуры цитохрома Р4501В1 приводят к тому, что метаболизм вышеуказанных соединений становится аномальным, что и способствует нарушению формирования глаза и развитию врожденной глаукомы. Сейчас известно более полусотни разновидностей мутаций гена CYP1B1, достоверно связанных с развитием этого заболевания, однако выявить взаимосвязь между конкретными дефектами гена и определенными клиническими формами пока не удалось.
Помимо этого, имеются указания на роль в развитии врожденной глаукомы другого гена – MYOC, расположенного на 1-й хромосоме. Продукт его экспрессии, протеин под названием миоциллин, широко представлен в глазных тканях и тоже участвует в формировании и функционировании трабекулярной сети глаза. Ранее было известно, что мутации этого гена являются причиной открытоугольной ювенильной глаукомы, однако при одновременном повреждении MYOC и CYP1B1 развивается врожденная разновидность этой патологии. Некоторые исследователи в области генетики полагают, что обнаружение мутации гена миоциллина на фоне дефекта CYP1B1 не играет особой клинической роли в развитии врожденной глаукомы и является просто совпадением. Мутации этих обоих генов наследуются по аутосомно-рецессивному механизму.
Кроме наследственных форм данной патологии примерно в 20% случаев диагностируется врожденная глаукома при отсутствии, как случаев заболевания, так и патологических генов у родителей. В таком случае причиной развития глазных нарушений могут выступать либо спонтанные мутации, либо же повреждение тканей глаза во внутриутробном периоде. Последнее может быть обусловлено заражением матери во время беременности некоторыми инфекциями (например, токсоплазмозом, краснухой), внутриутробными травмами плода, ретинобластомой, воздействием тератогенных факторов. Так как в такой ситуации не имеется генетического дефекта, такая патология носит название вторичной врожденной глаукомы. Кроме того, подобные нарушения органа зрения могут иметь место при некоторых других врожденных заболеваниях (синдром Марфана, ангидроз и другие).
Какой бы ни была причина врожденной глаукомы, механизм развития нарушений при этом состоянии практически одинаков. Из-за недоразвития угла передней камеры глаза и трабекулярной сети водянистая влага не может нормально покидать полость, происходит ее накопление, что сопровождается постепенным повышением внутриглазного давления. Особенностью врожденной глаукомы является тот факт, что ткани склеры и роговицы у детей обладают большей эластичностью, нежели у взрослых, поэтому при накоплении влаги происходит увеличение размеров глазного яблока (чаще всего двух сразу, очень редко только одного). Это несколько снижает внутриглазное давление, однако со временем и этот механизм становится недостаточным. Происходит уплощение хрусталика и роговицы, на последней могут появиться микроразрывы, ведущие к помутнению; повреждается диск зрительного нерва, истончается сетчатка. В конечном итоге может произойти ее отслоение – помутнение роговицы и отслойка сетчатой оболочки глаза являются ведущими причинами слепоты при врожденной глаукоме.
Классификация врожденной глаукомы
В клинической практике врожденную глаукому в первую очередь разделяют на три разновидности – первичную, вторичную и сочетанную. Первичная обусловлена генетическими нарушениями, наследуется по аутосомно-рецессивному механизму и составляет около 80% от всех случаев заболевания. Причина вторичной врожденной глаукомы заключается во внутриутробном нарушении формирования органов зрения различной негенетической природы. Сочетанная разновидность, как следует из названия, сопровождается наличием врожденной глаукомы на фоне иных наследственных заболеваний и состояний. Первичная форма, обусловленная генетическими дефектами, в свою очередь подразделяется на три клинические формы:
- Ранняя врожденная глаукома – при этой форме признаки заболевания выявляются при рождении, или они проявляются в первые три года жизни ребенка.
- Инфантильная врожденная глаукома – развивается в возрасте 3-10 лет, ее клиническое течение уже мало похоже на ранний тип и приближается к таковому у взрослых людей при других формах глаукомы.
- Ювенильная врожденная глаукома – первые проявления этой формы заболевания регистрируются чаще всего в подростковом возрасте, симптоматика очень схожа с инфантильным типом патологии.
Такой значительный разлет в возрасте развития врожденной глаукомы напрямую связан со степенью недоразвития трабекулярной сети глаза. Чем более выражены нарушения в этих структурах, тем ранее начинается накопление водянистой влаги с повышением внутриглазного давления. Если же недоразвитие угла передней камеры глаза не достигает значительных величин, то в первые годы жизни ребенка отток происходит вполне нормально, и нарушения развиваются намного позже. Попытки связать определенные клинические формы врожденной глаукомы с конкретными типами мутаций гена CYP1B1 на сегодняшний день не увенчались успехом, и механизмы развития того или иного типа заболевания до сих пор неизвестны.
Симптомы врожденной глаукомы
Наиболее своеобразными проявлениями характеризуется ранняя форма первичной врожденной глаукомы, что обусловлено анатомическими особенностями строения глаза у ребенка в возрасте до 3-х лет. В очень редких случаях глаукомные изменения можно заметить уже при рождении, чаще всего в первые 2-3 месяца жизни заболевание ничем себя не проявляет. Затем ребенок становится беспокойным, плохо спит, очень часто капризничает – это обусловлено неприятными и болезненными ощущениями, с которых дебютирует врожденная глаукома. Через несколько недель или месяцев начинается медленное увеличение размеров глазных яблок (реже — одного). Повышение внутриглазного давления и эластичность тканей склеры могут привести к значительному увеличению глаз, что внешне создает ложное впечатление красивого «большеглазого» ребенка. Затем к этим симптомам присоединяется отек, светобоязнь, слезотечение, иногда возникает помутнение роговицы.
Инфантильная и ювенильная формы врожденной глаукомы во многом очень схожи, различается только возраст развития первых проявлений заболевания. Увеличения размеров глазных яблок при этом, как правило, не происходит, патология начинается с ощущения дискомфорта и болезненности в глазах, головных болей. Ребенок может жаловаться на ухудшение зрения (появление ярких ореолов вокруг источников света, «мошки» перед глазами). Эти типы врожденной глаукомы часто сопровождаются другими нарушениями зрительного аппарата – косоглазием, астигматизмом, миопией. Со временем происходит сужение поля зрения (теряется возможность видеть предметы боковым зрением), нарушение темновой адаптации. Светобоязнь, отек и инъецирование сосудов склеры, характерные для ранней формы заболевания, при этих формах чаще всего не наблюдаются. При отсутствии лечения любая разновидность врожденной глаукомы со временем приводит к слепоте по причине отслойки сетчатки или атрофии зрительного нерва.
Диагностика врожденной глаукомы
Выявление врожденной глаукомы производится врачом-офтальмологом на основании данных осмотра, офтальмологических исследований (тонометрии, гониоскопии, кератометрии, биомикроскопии, офтальмоскопии, УЗ-биометрии). Также немаловажную роль в диагностике этого состояния играют генетические исследования, изучение наследственного анамнеза и течения беременности. При осмотре обнаруживаются увеличенные (при ранней форме) или нормальные размеры глаз, может также наблюдаться отек окружающих глазное яблоко тканей. Горизонтальный диаметр роговицы увеличен, на ней возможны микроразрывы и помутнение, склера истончена и имеет голубоватый оттенок, поражается при врожденной глаукоме и радужная оболочка – в ней возникают атрофические процессы, зрачок вяло реагирует на световые раздражители. Передняя камера глаза углублена (в 1,5-2 раза больше возрастной нормы).
На глазном дне длительное время не возникает никаких патологических изменений, так как за счет увеличения размеров глазного яблока внутриглазное давление поначалу не достигает значительных величин. Но затем довольно быстро развивается экскавация диска зрительного нерва, однако при снижении давления выраженность этого явления также уменьшается. По причине увеличения размеров глаз при врожденной глаукоме происходит истончение сетчатки, что при отсутствии лечения может привести к ее разрыву и регматогенной отслойке. Часто на фоне таких изменений обнаруживается миопия. Тонометрия показывает некоторое увеличение внутриглазного давления, однако этот показатель следует сопоставлять с передне-задним размером глаза, так как растяжение склеры сглаживает показатели ВГД.
Изучение наследственного анамнеза может выявить аналогичные изменения у родственников больного, при этом нередко удается определить аутосомно-рецессивный тип наследования – это свидетельствует в пользу первичной врожденной глаукомы. Наличие в ходе беременности инфекционных заболеваний матери, травм, воздействия тератогенных факторов указывает на возможность развития вторичной формы заболевания. Генетическая диагностика осуществляется посредством прямого секвенирования последовательности гена CYP1B1, что позволяет выявить его мутации. Таким образом, однозначно доказать наличие первичной врожденной глаукомы может только врач-генетик. Кроме того, при наличии такого состояния у одного из родителей или их родственников можно производить поиск патологической формы гена до зачатия или пренатальную диагностику путем амниоцентеза или других методик.
Лечение и прогноз врожденной глаукомы
Лечение врожденной глаукомы только хирургическое, возможно применение современных лазерных технологий. Консервативная терапия с использованием традиционных средств (капли пилокарпин, клонидин, эпинефрин, дорзоламид) является вспомогательной и может использоваться некоторое время в ходе ожидания операции. Хирургическое вмешательство сводится к формированию пути оттока водянистой влаги, что снижает внутриглазное давление и устраняет врожденную глаукому. Метод и схема проведения операции избирается в каждом конкретном случае строго индивидуально. В зависимости от клинической картины и особенностей строения глазного яблока могут выполняться гониотомия, синустрабекулэктомия, дренажные операции, лазерная циклофотокоагуляция или циклокриокоагуляция.
Прогноз врожденной глаукомы при своевременной диагностике и проведении операции чаще всего благоприятный, если же лечение произведено с опозданием, возможны различные по выраженности нарушения зрения. После устранения глаукомы необходимо не менее трех месяцев диспансерного наблюдения у офтальмолога.
Источник


