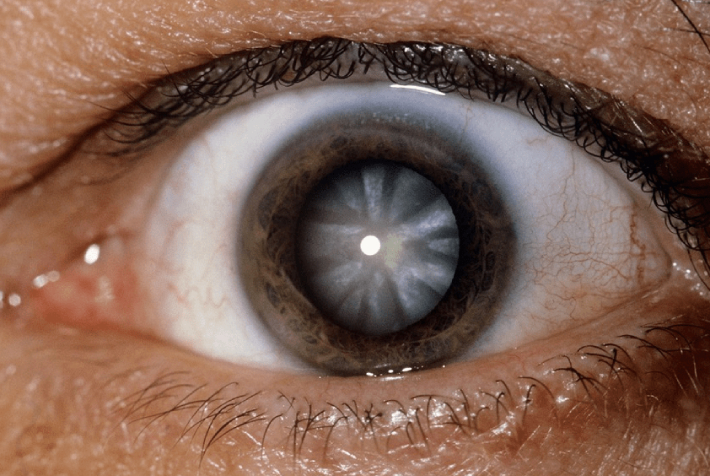
Глаукома и соматические заболевания
Авторы:
Алексеев В.Н.
1
,
Запорожец Л.А.
2
,
Ал-Майсам Р.
3
1 ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России, Санкт-Петербург, Россия
2 Ленинградская областная клиническая больница, Санкт-Петербург
3 ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» МЗ РФ, Санкт-Петербург
В данной работе оценивается зависимость снижения зрительных функций от наличия сопутствующей соматической патологии: гипертонической болезни (ГБ), дисциркуляторной энцефалопатии (ДЭ), сахарного диабета (СД), аутоиммунного тиреоидита (АИТ).
Цель: определить особенности течения глаукомного процесса у больных с различной соматической патологией.
Материал и методы: проведен анализ базы данных 2250 пациентов. Выделена группа больных первичной открытоугольной глаукомой (ПОУГ), состоящая из 174 человек (348 глаз, включая глаза с терминальной глаукомой). Диагноз глаукомы был поставлен на основании анализа данных биомикрогониоскопии, офтальмоскопии, гейдельбергской ретинальной томографии, оптической когерентной томографии, кинетической и статической периметрии, тонометрии и диагностических проб. Все больные этой группы имели сопутствующую соматическую патологию. У каждого пациента в соответствии с задачами исследования было только одно заболевание из заданных (ГБ, ДЭ, СД или АИТ). Выбор соматической патологии определялся ее распространенностью в популяции. Параллельно создана контрольная группа больных, которая также включала 174 человека (348 глаз). Больные из контрольной группы не страдали глаукомой, но имели сопутствующую соматическую патологию.
Результаты: анализ распределения глаукомы у больных с сопутствующей соматической патологией в зависимости от возраста позволил выделить группы риска прогрессирования глаукомы. Наиболее подверженной риску прогрессирования глаукомы оказалась группа пациентов старше 70 лет, страдающих ГБ (50,3%) и ДЭ (48,5%). Высокий риск прогрессирования глаукомы был у пациентов в возрасте от 40 до 49 лет, страдающих СД (29,1%) и АИТ (16,6%). Пациенты смежных возрастных групп имели более низкие показатели распределения глаукомы в зависимости от возраста и наличия сопутствующей соматической патологии.
Выводы: анализ общего соматического состояния больных с ПОУГ выявил достоверную связь между распространенностью ГБ, ДЭ, СД, АИТ и первичной глаукомы. Наиболее подверженными риску прогрессирования глаукомы оказались группа пациентов до 60 лет, имеющих в анамнезе СД и АИТ, и группа пациентов старше 60 лет, имеющих сопутствующую патологию – ГБ и ДЭ. Рекомендуется учитывать эту особенность течения первичной глаукомы при длительном диспансерном наблюдении за больными и контролировать соматический статус пациентов совместно с профильными специалистами.
Ключевые слова: первичная глаукома, гипертония, сахарный диабет, дисциркуляторная энцефалопатия, аутоиммунный тиреоидит, группы риска, динамическое наблюдение.
Для цитирования: Алексеев В.Н., Запорожец Л.А., Ал-Майсам Р. Первичная глаукома у больных с различной соматической патологией: особенности наблюдения и течения // РМЖ. Клиническая офтальмология. 2016. № 2. С. 79–82.
Для цитирования: Алексеев В.Н., Запорожец Л.А., Ал-Майсам Р. Первичная глаукома у больных с различной соматической патологией: особенности наблюдения и течения. РМЖ. Клиническая офтальмология. 2016;2:79-82.
Primary glaucoma in patients with various somatic diseases: main features of monitoring and disease course
Alexeev V.N., Zaporozhetc L.A., Rindgibal Al-Maisam
North-Western State Medical University named after I.I. Mechnikov, Saint-Petersburg, Russia,
Regional hospital of Saint-Petersburg, Russia
Treatment of primary glaucoma is determined by a number of factors: the appropriate diagnosis, adequate treatment regimen, competent medical observation, as well as a number of social and economic reasons. Strict implementation of the leading clinics recommendations, aimed at correction of intraocular pressure and neuroprotective treatment of the optic nerve can not guarantee long-term maintenance of visual function in patients with primary glaucoma.
Purpose: In this study the dependence of decrease of visual function in the presence of concomitant somatic diseases — hypertension, vascular encephalopathy, diabetes mellitus, autoimmune thyroiditis was evaluated.
Methods: To determine the peculiarities of the glaucoma process in patients with various somatic diseases – hypertension, dyscirculatory encephalopathy, diabetes mellitus, autoimmune thyroiditis. A database analysis of 2250 patients was done. Selected group of patients with primary open-angle glaucoma, consisting of 174 patients (348 eyes, including eyes with terminal glaucoma). The diagnosis of glaucoma was made on the basis of the data analysis of biomicroscopy, оphthalmoscope, Heidelberg retinal tomography, optical coherence tomography, kinetic and static perimetry, tonometry and diagnostic tests. All patients of this group had concomitant somatic pathology. In each patient, in accordance with the objectives of the study, there was only one set of disease (hypertension, encephalopathy, diabetes or autoimmune thyroiditis). The choice of somatic pathology was determined by the prevalence of this disease in the population. Simultaneously created the second, control, group of patients, which also included 174 patients (348 eyes). Patients from the control group did not suffer from glaucoma, but had the concomitant somatic pathology.
Results: The analysis of the distribution of glaucoma in patients with concomitant somatic pathology according to age allowed us to identify groups at risk of progression of glaucoma. Most at risk of progression of glaucoma was the group of patients older than 70 years, suffering from hypertension (50,3%) and dyscirculatory encephalopathy (48,5 %). High risk of progression of glaucoma was in patients from 40 to 49 years of age with diabetes (29,1%) and autoimmune tireo-dieth also (16,6 %). Patients adjacent age groups had a lower incidence indicators of glaucoma depending on the age and presence of concomitant somatic pathology.
Сonclusions: The analysis of the general somatic state of patients with primary glaucoma showed a significant relationship between the prevalence of hypertension, dyscirculatory encephalopathy, diabetes mellitus, autoimmune thyroiditis and primary glaucoma. Most at risk of progression of glaucoma was the group of patients 60 years of age, have a history of diabetes mellitus and autoimmune thyroiditis, and the group of patients older than 60 years with comorbidities – hypertension and dyscirculatory encephalopathy. It is recommended to take into account this feature of primary glaucoma in the prolonged course of medical observation of patients and monitor the somatic status of the patients in cooperation with the relevant experts.
Keywords: primary glaucoma, hypertension, diabetes, encephalopathy, autoimmune thyroiditis, risk groups, dynamic monitoring.
For citation: Alexeev V.N., Zaporozhetc L.A., Rindgibal Al-Maisam Primary glaucoma in patients with various somatic diseases: main features of monitoring and disease course // RMJ. Clinical ophthalmology. 2016. № 2. P. 79–82.
Статья посвящена особенностям наблюдения и течения первичной глаукомы у больных с различной соматической патологией:
DOI: 10.21689/2311-7729-2016-16-2-79-82
Обсуждение вопросов течения первичной глаукомы сохраняет свою актуальность. Строгое выполнение рекомендаций ведущих мировых клиник, направленных на коррекцию внутриглазного давления (ВГД) и нейропротекторную защиту зрительного нерва, не гарантирует длительное сохранение зрительных функций у больных с первичной глаукомой. Опытный врач часто не может информировать пациента о дальнейшем течении его заболевания. Не удается учитывать все факторы, влияющие на исход глаукомы: физиологический и психологический статус пациента, социальные и экономические причины [1–6]. В данной работе прогноз течения глаукомы определяется, исходя из ее сочетания с распространенной соматической патологией [7–10] и возрастным фактором.
В проведенном исследовании предлагается изучить влияние на течение глаукомы ГБ [3], ДЭ, СД [8, 9] и АИТ [10] как наиболее распространенных в популяции патологий.
Цель: определить особенности течения глаукомного процесса у больных с различной соматической патологией.
Материал и методы
В работе была проанализирована база данных 2250 пациентов. Эта группа является базовой статистической группой в данном исследовании. Все пациенты, включенные в базовую статистическую группу, имели верифицированную глаукому различных форм (открыто-, закрытоугольную, смешанную) и стадий. Диагноз был поставлен на основании анализа данных биомикрогониоскопии, офтальмоскопии, гейдельбергской ретинальной томографии, оптической когерентной томографии, кинетической и статической периметрии, тонометрии и диагностических проб.
Всем пациентам проводилось лечение по различным схемам в соответствии с формой, стадией процесса, наличием или отсутствием стабилизации глаукомы. Стабильность глаукомного процесса оценивалась по общепринятым методикам: оценка состояния диска зрительного нерва (ДЗН) с помощью различных методов, оценка полей зрения с помощью кинетической периметрии и стандартной автоматической периметрии, а также состояния ВГД (тонометрия по Маклакову).
В процессе наблюдения особое внимание обращалось на наличие сопутствующей соматической патологии: ГБ, ДЭ, СД, АИТ. Из базовой статистической группы была сделана выборка больных ПОУГ, состоящая из 174 человек (348 глаз, включая глаза с терминальной глаукомой). Отбор больных для этой подгруппы, условно названной подгруппой А, определялся полнотой собранного соматического статуса.
Параллельно сделана вторая выборка (подгруппа В), которая также включала 174 человека (348 глаз) из числа тех, кто был на приеме невролога, эндокринолога, кардиолога. Больные из подгруппы В не страдали глаукомой.
Подгруппы А и В были сопоставимы по возрасту и полу (табл. 1, 2).
Результаты
По данным проведенных исследований изучалась корреляционная связь между показателями в сформированных подгруппах больных. В подгруппах А и В число больных составило 348 человек (696 глаз). Предварительный анализ показал наличие статистически значимых различий с учетом распространенности изучаемых заболеваний: ГБ, ДЭ, СД, АИТ.
В таблице 3 представлены распространенность заболеваний в изучаемых подгруппах А и В и их процентные соотношения.
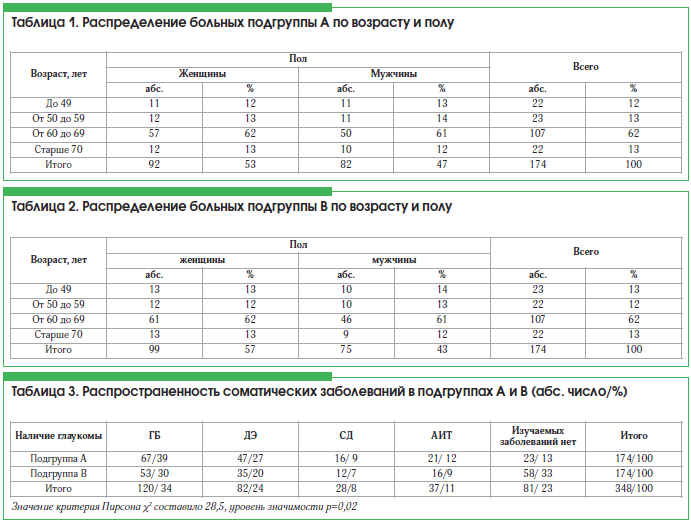
Видно, что в количественном и процентном соотношениях преобладают больные подгруппы А, страдающие глаукомой и сопутствующей соматической патологией. Имеются достоверные статистические различия – в группе больных глаукомой распространены оцениваемые заболевания.
Проведен анализ распределения глаукомы у больных с разной соматической патологией: ГБ, ДЭ, СД, АИТ в зависимости от возраста.
Преобладание ГБ в группах лиц старше 60 лет является достоверным (табл. 4).
Преобладание ДЭ в группах лиц старше 60 лет является достоверным (табл. 5).
Преобладание СД в группе лиц от 40 до 49 лет является достоверным (табл. 6).
Преобладание АИТ в группе лиц от 40 до 49 лет является достоверным (табл. 7).
В сводной таблице 8 продемонстрированы статистические связи между глаукомой и сопутствующей соматической патологией.

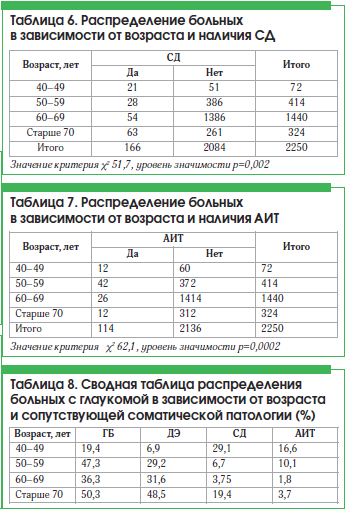
Данные таблиц 4–7 позволяют сделать вывод о наличии статистической связи между распространенностью АИТ и СД у пациентов с глаукомой более молодого возраста (до 60 лет). После 60 лет такая статистическая связь имеется для ГБ и ДЭ.
Выводы
1. Анализ общего соматического состояния больных с ПОУГ выявил достоверную связь между распространенностью ГБ, ДЭ, СД, АИТ и ПОУГ.
2. Наиболее подвержены риску прогрессирования группы пациентов до 60 лет, имеющих в анамнезе СД и АИТ, и группа пациентов старше 60 лет, имеющих сопутствующую патологию: ГБ и ДЭ.
3. Необходимо учитывать эту особенность течения ПОУГ при длительном диспансерном наблюдении за больными и контролировать соматический статус пациентов совместно с профильными специалистами.
Источник
Руднева Л.Ф., Датских Е.О., Коновалова Н.А., Пономарева Е.Ю., Починок Е.М.
Актуальность. В связи с тем, что у больных с глаукомой после первичных и повторных оперативных вмешательств развиваются осложнения, необходимо выявление прогностических факторов риска и совершенствование тактики лечения глаукомы у больных пожилого и старческого возраста.
Цель – установить прогностические факторы риска неблагоприятного клинического течения и исходов хирургического лечения у больных пожилого и старческого возраста с псевдоэксфолиативной глаукомой (ПЭГ) на фоне соматической патологии, и дать рекомендации по тактике лечения.
Материалы и методы. Объектом исследования послужили 554 больных с ПЭГ на фоне соматической патологии, находившихся на лечении в офтальмологическом отделении ГБУЗ ТО «Областная клиническая больница № 1» г. Тюмени в течение трех лет (2012-2014 гг.). По гендерным признакам и возрасту больные распределились следующим образом: 253 мужчины (45,7 %) и 301 женщина (54,3 %) в возрасте от 76 до 89 лет, средний возраст составил 80,8±1,5.
Проводилось обследование: клиническое, лабораторное, функциональное, рентгенологическое, стандартное офтальмологическое. Всем больным проведены: предоперационная подготовка (в течение 1-2 мес.) и хирургическое лечение глаукомы методами – СТЭ или НГСЭ – с последующим послеоперационным комплексным лечением в зависимости от вида операции. Проведен клинический анализ: частоты нозологии соматической патологии, вида оперативного вмешательства, частоты повторных операций и послеоперационных осложнений при ПЭГ. Изучались факторы риска предрасположенности к повторному хирургическому лечению пациентов. Статистическую обработку материала проводили с помощью программы Statistica (версия 6.0).
Результаты и обсуждение. Изучение характера соматических заболеваний у больных с глаукомой продемонстрировало частоту сочетанной патологии: сердечно-сосудистой и эндокринной (86,7 %). У больных диагностирована ишемическая болезнь сердца (ИБС) и артериальная гипертензия (АГ) в сочетании с сахарным диабетом (СД) 1 типа в 28,2 %, с СД 2 типа – в 58,5 % случаев, ожирение наблюдалось у большинства больных (86,6 %). Проанализирована частота соматических заболеваний при первичных и повторных оперативных вмешательствах. У пациентов выявлена значительная частота сочетанной сердечно-сосудистой и эндокринной патологии при первичном и повторном оперативном лечении (76,3 % и 97,4 % соответственно). Значительно реже больные оперировались первично и повторно с «изолированной» сердечно-сосудистой патологией (ИБС, АГ) (9,2 % и 0,8 %; р<0,05) или при сочетании сердечно-сосудистых заболеваний с ХОБЛ (14,5 % и 1,8 %; р<0,05 соответственно). Соматические заболевания у всех больных осложнялись хронической недостаточностью мозгового кровообращения (ХНМК) с дисциркуляторной энцефалопатией (ДЭП) преимущественно II – III ст., причем ДЭП III ст. наблюдалась с большей частотой (86,6 %). На выбор метода оперативного вмешательства пациентов влияли характер соматической патологии и первичного или повторного оперативного вмешательств. При первичных оперативных вмешательствах выполнялась СТЭ или НГСЭ (53,2 % и 46,8 % соответственно), при повторных оперативных вмешательствах использовался преимущественно метод СТЭ (93,7 %), в том числе с дренажем (6,3 %). Частота послеоперационных осложнений при первичных оперативных вмешательствах составила 11,0 %, тогда как при повторных операциях частота их была в 2 раза выше – 43,0 %. В развитии глаукомы важную роль играют общие и локальные факторы: анатомические, генетические, возрастные – и соматические заболевания. На основании проведенного исследования установлено, что среди оперированных больных по поводу ПЭГ наибольший удельный вес составляли больные с сочетанной соматической патологией: сердечно-сосудистой (ИБС, АГ) и эндокринной (СД, ожирение) с проявлениями ХНМК (ДЭП II – III ст.) пожилого и старческого возраста.
Основное патологическое звено ХНМК: атеросклероз церебральных сосудов, ИБС, АГ, СД – сопровождается изменениями в мелких внутримозговых артериях, и поражением подкорковых ядер белого вещества, и гидроцефалией. Это наиболее частые причины ДЭП. Ожирение оказывает системное воздействие на организм. Гормонально-обменные нарушения при сердечно-сосудистом и эндокринном соматическом «квартете» (АГ, ИБС, СД, ожирение) взаимосвязаны подобно порочному кругу. Не вызывает сомнения их способность отрицательно влиять на сосудистую систему в целом, в том числе на регионарное церебральное и глазное кровообращение. Изменения общего характера (сосудистые, эндокринные, обменные) воздействуют на регуляцию ВГД, процессы гемостаза, выраженность дистрофических нарушений в различных структурах глаза, прежде всего в дренажном, а также на толерантность зрительного нерва к повышению ВГД. Таким образом, ПОУГ, возникшую на фоне сочетанной соматической патологии, можно рассматривать как системную патологию.
Выводы
К факторам риска предрасположенности к повторному хирургическому лечению пациентов отнесены: пожилой и старческий возраст, сердечно-сосудистый и эндокринный (ИБС, АГ, СД, ожирение) соматический «квартет» с ХНМК (ДЭП II – III ст.).
Источник
23 апреля 201840113 тыс.
До ХVIII века катаракта и глаукома не разделялись как самостоятельные заболевания; они были широко распространены с незапамятных времен и хорошо известны медикам древности, – в частности, Гиппократу Асклепиаду, – которые веками и тысячелетиями искали способы предотвращения полной слепоты, лечения или хотя бы замедления патологического процесса. Само слово «глаукома», следуя логике древнегреческого словообразования, можно перевести как «опухоль цвета морской волны» (по сей день можно услышать также просторечные диагнозы «морская вода» или «зеленая катаракта»), хотя прямого отношения к опухолям глаукома не имеет. Чаще всего суть глаукомы кратко и упрощенно сводят к повышенному внутриглазному давлению; это, конечно, столь же недостаточно для понимания сложных этиопатогенетических закономерностей, как и свести катаракту к одному лишь помутнению хрусталика. Вообще, глаукома насчитывает несколько десятков существенно разных форм, типов и клинических вариантов, поэтому термин часто рассматривают как собирательный.
Несмотря на революционные сдвиги в развитии офтальмологии, распространенность глаукоматозной патологии продолжает расти; на сегодняшний день она составляет, по разным источникам, от 60 до 100 млн человек в мире. Из них свыше миллиона человека стоят на офтальмологическом учете в России. В структуре заболеваемости прослеживаются достоверные расовые, половые, возрастные тенденции: так, негроидная раса страдает значительно чаще, женщин среди заболевающих втрое больше, чем мужчин, а по достижении зрелого или преклонного возраста риск развития глаукомы повышается с каждым годом.
Упомянутый выше прогресс офтальмологии, – прежде всего, офтальмохирургии как наиболее эффективной сегодня отрасли медицины вообще, по оценке ВОЗ, – действительно мог бы кардинально изменить ситуацию. Однако такие факторы, как ухудшение экологической обстановки в развитых странах и низкий уровень здравоохранения в развивающихся, пока не позволяют ни обратить вспять, ни хотя бы замедлить тревожную эпидемиологическую динамику.
Причины
Процессы обмена веществ и тканевого питания в глазу обеспечиваются циркуляцией внутриглазной жидкости. Передняя и задняя камеры глазного яблока в норме сообщаются между собой; строение глаза включает несколько путей отвода внутриглазной жидкости (трабекулярная сеть, увеосклеральный путь, шлеммов канал). Ключевое значение имеет дренажная система в месте сопряжения роговицы и склеры в углу передней камеры. Две основные формы глаукомы, – открытоугольная и закрытоугольная, – различаются именно тем, сохранны ли дренажные функции угла передней камеры, либо он блокирован. На долю открытоугольной глаукомы приходится свыше 90% всех регистрируемых случаев (в других источниках эта доля оценивается как 80%).
Вопрос об этиопатогенезе глаукомы остается открытым. Так, повышенное давление внутриглазной жидкости является и следствием глаукоматозного процесса, и его причиной. Если по каким-то причинам давление повышается (например, при системной артериальной гипертензии, при органических изменениях в хрусталике вследствие катаракты, при избыточной секреции и пр.), это приводит к избыточной нагрузке на ткани дренажных структур и вскоре запускает в них дегенеративно-дистрофические процессы, что, в свою очередь, деформирует отводящие каналы и прогрессивно снижает их проходимость.
К основным причинам и факторам риска относят возрастные изменения (нарастающее склерозирование тканей и сосудистых стенок), наличие выраженной близорукости или дальнозоркости, нарушения трофики глазных тканей (обусловленные, в том числе, диетологическими факторами), наследственную предрасположенность, офтальмотравмы, особенности анатомического строения глаза (в частности, сравнительно малые размеры глазного яблока и его передней камеры у монголоидов повышают риск развития глаукомы), интоксикации некоторыми органическими ядами, профессиональная деятельность в ночную смену или в монотонно-наклонной позе. Глаукома может быть вторичным следствием множества разнородных заболеваний, причем не только офтальмологических, но и эндокринных, онкологических и сосудистых, а также развиваться после офтальмохирургического вмешательства по другому поводу. Подтвержденными факторами риска являются также курение, злоупотребление алкоголем и длительный прием гормональных средств.
Симптоматика
Первыми признаками глаукомы чаще всего становятся дискомфортные ощущения распирания, тяжести в глазном яблоке, а также сужение поля зрения от периферии к центру, по типу закрывающейся диафрагмы или фотографической виньетки. Типичными проявлениями являются также периодически появляющиеся радужные круги или пелена перед глазами, постепенно снижающаяся насыщенность и избыточная контрастность цвето- и световосприятия. Однако начинается глаукоматозный процесс, как правило, задолго до появления первых ощутимых и клинически значимых симптомов.
Острый приступ характеризуется резким повышением ВГД (внутриглазное давление), нарушениями кровообращения, болью в глазу и его необычной «каменной» твердостью, мигренозной головной болью, нередко тошнотой и даже рвотой, слабостью, общим недомоганием, болями в груди и верхней части живота – в совокупности такая разнородная симптоматика может приниматься за проявления совершенно других заболеваний. Острый приступ глаукомы, вовремя не купированный, может привести к необратимым изменениям в зрительном нерве и полной слепоте.
Впрочем, такой же исход весьма вероятен при нелеченной хронической глаукоме: нарастающие дегенеративно-дистрофические изменения в оптических тканях глазного яблока, сетчатке, диске зрительного нерва формируют характерную внешнюю картину глаукоматозного глаза и обусловливают прогрессирующую утрату зрительных функций вплоть до полной их утраты, причем в самых тяжелых случаях зрения утрачивается вместе с глазом как таковым: во избежание еще более тяжких, жизнеугрожающих осложнений приходится производить энуклеацию (полное удаление глазного яблока из орбиты).
Диагностика
Глаукома диагностируется клинически, анамнестически и инструментально. Первыми и наиболее информативными исследованиями обычно оказывается глазная тонометрия (измерение ВГД), стандартная офтальмоскопия, измерение параметров рефракции и анатомических пропорций внутриглазных структур, гониоскопия, УЗИ и другие применяемые в современной офтальмологии методы.
Лечение
Терапия глаукомы включает четыре основные направления: медикаментозное лечение, физиотерапию, офтальмохирургическую коррекцию и обязательные профилактические меры. Так, разработан и успешно применяется ряд препаратов, способствующих оттоку глазной жидкости и, если это показано, снижению ее секреции. Достоверно эффективны физиотерапевтические процедуры – такие, например, как электростимуляция, магнитотерапия, низкоэнергетическая стимуляция лазерным излучением и т.п.
Методология хирургического лечения глаукомы на сегодняшний день хорошо развита и отработана; практикуется множество конкретных техник коррекции и восстановления дренажных функций, включая собственно хирургические методы, лазерную хирургию, имплантацию искусственных глаукомных клапанов и т.д.
Наконец, профилактика рецидивирующих приступов и дальнейшего прогрессирования болезни подразумевает широкий спектр рекомендаций и противопоказаний: сюда входит нормализация рациона питания и режима потребления жидкости, лечение соматических заболеваний (которые нередко являются первопричиной и фоном развития глаукомы); в некоторых случаях приходится ставить вопрос о смене профессии, ограничении физических нагрузок и пр.
Следует особо подчеркнуть, что многообразие причин, форм, вариантов течения, тканевых и анатомических изменений при глаукоме настолько велико, что любое самолечение, – будь то покупка безрецептурных лекарств в аптеке или т.н. народные методы, – становится уже не просто нежелательным, а в ряде случаев опасным: эффект от такого рода деятельности может оказаться прямо противоположным ожидаемому. Любая терапевтическая схема разрабатывается исключительно офтальмологом, для конкретного случая с его бесчисленными индивидуальными нюансами, и должна соблюдаться неукоснительно во всех деталях – от дозировок и времени приема лекарств до коррекции образа жизни. Лишь при этом условии удается сохранить зрение, затормозив и остановив дальнейшее прогрессирование этой сложной многофакторной патологии.
Источник