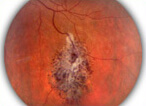
Дистрофия пигментного слоя сетчатки
Пигментная дистрофия сетчатки – заболевание, имеющее генетический характер. Процесс болезни протекает без проявления явных симптомов, однако его завершающие стадии проводят к полной потере зрения.
Причины развития
Пигментная дегенерация сетчатки глазного яблока — болезнь, в результате которой происходит постепенное сужение зрительных полей. Один из явных симптомов болезни — это потеря зрения в сумеречное время. Болезнь может быть вызвана сбоем работы определенного гена. В редких случаях происходит нарушение взаимодействия нескольких геномов. Заболевание носит наследственный характер и передается по мужской линии. Болезнь может сопровождаться нарушением работы слухового аппарата.
Причины сбоев в работе генной системы человеческого организма до сих пор не выявлены. Заокеанскими исследователями выявлено, что нарушения в ДНК не являются стопроцентной причиной развития пигментной дистрофии. По мнению специалистов, болезнь провоцирует возникновение нарушений в сосудистой системе глазного яблока.
Несмотря на то что причины возникновения заболевания остаются загадкой медицины, специалисты достаточно достоверно изучили вопрос его развития.
 Пигментная дегенерация сетчатки – довольно редкое заболевание, приводящее к ухудшению зрения в темноте
Пигментная дегенерация сетчатки – довольно редкое заболевание, приводящее к ухудшению зрения в темноте
На начальном этапе болезни происходит процесс сбоя метаболизма в сетчатой оболочке глазного яблока. Также нарушения затрагивают и сосудистую систему. В результате развития заболевания начинает разрушаться слой сетчатки, в котором находится пигмент. В этом же слое расположены чувствительные фоторецепторы, палочки и колбочки. На первых этапах процессы дегенерации затрагивают лишь периферийные участки ретины. Именно поэтому пациент не испытывает дискомфорта и болезненных ощущений. Постепенно измененный участок начинает увеличиваться в размерах до того момента, пока не охватит всю зону сетчатой оболочки. Когда ретина поражена полностью, начинают проявляться первые серьезные симптомы заболевания, ухудшение восприятия цветов и их оттенков.
Болезнь может распространиться лишь на одном глазу, однако нередки случаи, когда заболевание затрагивает сразу два зрительных органа. Первые симптомы заболевания проявляются еще в раннем детстве, а уже к двадцати годам человек может потерять трудоспособность. Тяжелые стадии пигментной дистрофии сетчатой оболочки могут сопровождаться такими осложнениями, как катаракта и глаукома.
Симптоматика
Вялое развитие болезни приводит к тому, что большинство пациентов обращаются за помощью специалистов, когда патологические изменения начали своё бурное развитие. Первым серьезным симптомом заболевания является сложность ориентирования в условиях низкого освещения. Патологии, происходящие на периферийной части сетчатой оболочки, приводят к тому, что сужаются зрительные поля.
Учитывая особенность болезни, основная группа пациентов — это дети, не достигшие школьного возраста. В таком возрасте мелкие проблемы со зрением не замечаются, а значит, родители могут не знать о развитии заболевания.
Первые этапы развития могут протекать длительно — до пяти лет. Впоследствии начинает прогрессировать дегенерация периферической области сетчатой оболочки. Зрительные поля к этому моменту сильно сужены, у некоторых пациентов наблюдается полное отсутствие бокового зрения. Осмотр офтальмолога может выявить участки с патологическими изменениями, однако если бездействовать, то в скором времени они распространяться по всей ретине. На данном этапе, в некоторых частях сетчатой оболочке, могут появиться просветы. Стекловидное тело начинает терять свою прозрачность, становясь мутно желтым. На этой стадии центральное зрение не затрагивается.
 Точная причина заболевания не установлена, но врачи-офтальмологи называют лишь версии развития пигментной дегенерации сетчатки
Точная причина заболевания не установлена, но врачи-офтальмологи называют лишь версии развития пигментной дегенерации сетчатки
Заболевание в запущенной стадии может быть осложнено возникновением таких заболеваний, как глаукома и катаракта. При осложнениях центральное зрение очень резко теряет свою остроту, а со временем может быть безвозвратно потерянно. Осложнения приводят к тому, что начинает развитие атрофия стекловидного тела.
Существует еще одна форма дегенерации сетчатки — атипичная. В результате заболевания изменяется внешний вид и строение сосудистой системы. Пациент испытывает затруднение ориентирования, в условиях недостаточной освещенности.
Одним из редчайших видов дегенерации сетчатки является односторонняя форма, при этом у пациента обязательно развивается катаракта.
Лечение пигментной дистрофии
Лечение пигментной денегенерации сетчатки глаза, находящейся в стадии развития, чаще всего осуществляется при помощи медикаментов. Действия лекарств должны быть направлены на нормализацию кровообращения и обмена питательных веществ в сетчатой оболочке и сосудистой системе. В большинстве случаев специалистами назначаются следующие препараты:
- «Эмоксипин». Данный препарат корректирует микроциркуляцию в организме.
- «Тауфон». Капли для глаз стимулирующие процессы регенерации в глазных тканях.
- «Ретиналамин». Препарат, назначающийся при дистрофии сетчатой оболочки, обладает регенеративным действием.
- Никотиновая кислота. Витамин, стимулирующий обмен полезных веществ в организме и циркуляцию крови.
- Но-шпа с папаверином. Спазмолитик, который снимает давление в сосудистой системе.
Данные препараты могут быть назначены врачом как в виде таблеток, так и в виде инъекций или глазных капель.
 При развитии заболевания определяется потеря периферического зрения
При развитии заболевания определяется потеря периферического зрения
Очень часто помимо лечения медикаментами назначается курс физиотерапии для стимулирования процессов восстановления и регенерации сетчатки. Прохождение этого курса способно активировать работу фоторецепторов. Одними из популярных методик на сегодняшний день являются стимуляция электрическими импульсами, магниторезонансная и озонотерапия. Если в результате заболевания была поражена сосудистая оболочка глаза, имеет смысл проведения хирургического вмешательства.
С помощью операции специалисты нормализуют циркуляцию крови в сетчатом слое глазного яблока. Для достижения этой цели может понадобиться пересадка определенных тканей глазного яблока, под перихориоидальное пространство.
Применение аппаратов, корректирующих зрение
Некоторые специалисты рекомендуют лечение пигментной дистрофии сетчатки глаза с помощью аппаратов фотостимуляции. В основе их работы лежит методика, вызывающая возбуждение в определенных областях глазного яблока и замедление процесса развития болезни.
Излучение, испускаемое аппаратурой, стимулирует циркуляцию крови в сосудистой системе глазного яблока, а также нормализует обмен питательных веществ. С помощью данной методики также можно снять отечность с сетчатой оболочки глазного яблока. Фотостимуляция сетчатой оболочки зрительных органов может благоприятно сказаться на укреплении ретины и улучшении циркуляции полезных веществ во внутренних слоях глазного яблока.
 Повреждение начинается на периферии и распространяется в течение нескольких десятков лет к центральной зоне сетчатки
Повреждение начинается на периферии и распространяется в течение нескольких десятков лет к центральной зоне сетчатки
Прогноз
К сожалению, сегодня медицина еще достаточно далека от решения вопроса, когда заболевание находится в запущенном состоянии. Очень часто поступают новости о том, что зарубежные исследователи нашли способ восстановления определенных генов, отвечающих за возникновение болезни. Уже сегодня, проходят завершающую стадию тестирования специальные имплантаты, способные заменить сетчатую оболочку.
Другой подход специалистов выявил, что полностью восстановить потерянное зрение можно с помощью инъекций специального вещества, содержащего в себе клетки чувствительные к свету. Однако эта методика еще находится на стадии экспериментов, и получится ли у ученых добиться необходимого результата пока неизвестно.
Многие из тех, кто столкнулся с данным заболеванием, знают, что прогноз успешности лечения в большинстве случаев неблагоприятный. Но если заболевание выявлено в начальной стадии, используя определенные методики лечения, можно остановить его прогрессию. В некоторых случаях специалисты добивались действительно ощутимых результатов. Людям, у которых диагностировано заболевание, необходимо избегать длительных физических нагрузок, а также нагрузок на зрительные органы.
Источник
Пигментная дистрофия сетчатки представляет собой дегенеративное расстройство на внутренней оболочке глаза. Сама сетчатка имеет так называемые палочки, вследствие которых зрительный орган работает правильно. При данной патологии происходит их нарушение. По этой причине получается изменение нейроэпителия сетчатки, пигментного эпителия.
Дистрофическое нарушение является опасным и редким недугом, так как способно привести к слепоте и инвалидности. Болезнь имеет не одно название, также недуг называется ретинит и тапеторетинальная абиотрофия. Есть ещё одно понятие – возрастная макулярная дистрофия сетчатки, здесь происходит поражение кровеносных капилляров в районе макулы и клеток. Болезнь носит наследственный характер и наблюдается у людей свыше 40 лет.
В чем причины заболевания
Точной причины, почему образуется дистрофия сетчатки глаза, нет, поскольку до сих пор этиология не установлена. Но известно однозначно, что болезнь передаётся генетическим путём. Отмечается уменьшение степени питания фоторецепторов, потому и происходит разрушение клеток.
Предрасполагающими факторами являются:
- склероз сосудов сетчатки глаза – здесь нарушается капиллярная пластина;
- нарушение внутриутробного развития – вредные привычки, приём сильнодействующих медикаментов, стрессовые ситуации ведут к отклонению роста плода;
- возраст – постепенно сосуды изнашиваются, клетки начинают отмирать;
- патологические расстройства в эндокринной системе, обусловленные недостатком витамина А;
- травмы головного мозга – из-за чего происходит обмен веществ и изменение кровоснабжения;
- слабая иммунная система;
- отравляющие вещества, радиация нарушают структуру ДНК.
Вне зависимости от причины появления заболевания, пациенты ощущают почти одни и те же симптомы. Чем раньше они станут замечены, тем эффективней будет лечение.
Как классифицируют патологию
По типу пигментная дистрофия глаза делится на:
- Периферическую – повреждается боковое зрение, в зону риска попадают люди с близорукостью.
- Центральную – зрительная функция ухудшается, чаще встречается как раз-таки данный тип отклонения. Человек не может читать, водить автомобиль.
- Генерализованная – нарушение работы клубочковой системы.
По роду образования различают:
- приобретённую;
- врождённую: подразделяется на точечную – полное отсутствие видимости в темноте; пигментную – появляется по причине нарушения фоточувствительных рецепторов.
Виды дистрофии:
- Пигментная – восстановить зрение помогут витамины и специальная гимнастика.
- Точечная белая – нередко приводит к косоглазию.
- Беста – создаёт пелену перед глазами.
- Дистрофия пятна Штаргардта – наследственный недуг, снижение зрения происходит медленно.
Тяжёлое течение болезни опасно атрофией зрительного нерва, впоследствии чего развивается слепота.
Какими симптомами проявляется
Пигментная дегенерация сетчатки протекает вяло, не имея выраженных признаков. В этом и есть вся опасность. Начальным сигналом отклонения становится снижение возможности человека распознавать предметы в слабоосвещённом пространстве. В случае генетического фактора болезнь проявляется ещё в маленьком возрасте. На что родители не сразу обращают внимание, считая, что малыш боится темноты.
Симптомы пигментной дистрофии:
- моментальная усталость глаз в ночное время;
- ослабление или отсутствие периферического зрения;
- расстройство координации движения, находясь в тёмном коридоре, улице;
- сужение поля зрения;
- неспособность верно отличить движущийся объект от покоящегося;
- нарушение распознавания цветов;
- образования мушек перед глазами.
При наличии подобной клинической картины важно вовремя обратиться к офтальмологу. Замедление лечебных действий способно к прогрессированию патологии и отслоению сетчатки.
Как диагностируют
В первую очередь врач расспрашивает пациента об имеющихся симптомах и их продолжительности. Внимательно изучается генетика больного. Затем выполняются следующие диагностические действия:
- анализ крови, мочи – с их помощью устанавливается наличие инфекции, паразитарных заболеваний, воспалительного процесса в организме; тут же изучаются онкомаркеры на отсутствие онкологии;
- проверка зрительной остроты – применяются специальные линзы, таблицы;
- электрофизиологическое исследование – манипуляция позволяет справедливо оценить функциональные возможности сетчатки;
- осмотр глазного дна – внимательно изучаются пятна; уровень повреждения органа устанавливается присутствием костных телец, отмечается побледнение диска глазного нерва;
- тест на дальтонизм – если человек путает цвета на картинках, это является признаком пигментной дистрофии;
- оценка ориентации больного в плохо освещённом помещении.
Если вовремя не начать лечение дистрофии сетчатки, возможно образование некроза, воспаления или, что ещё хуже, слепота.
Как лечат
Поскольку точной причины пигментной дегенерации сетчатки нет, то и определённого лечения не существует. Однако имеются поддерживающие методики, вследствие которых получается остановить прогрессирование недуга.
Медикаментозная терапия
Если патология появилась у ребёнка, то к 25-летнему возрасту видимость человека уменьшается аж до потери трудоспособности.
Зачастую лечение дистрофии сетчатки производится путём комплексного использования медикаментов, разрешающих наладить кровообращение в органе, предоставить сетчатке нужное питание.
Назначаются следующие лекарства:
- Эмоксипин, Милдронат, Тауфон – это капли и уколы, питающие клетки органа и нацеленные на ускорение процесса кровоснабжения.
- Аллоплант, Ретиналамин – биорегулирующие препараты предусмотрены для регенерации и возобновления сетчатки.
- Витамины А, В – обязательные средства для восстановления органа зрения.
- Тиклодипин, Ацетилсалициловая кислота – антиагреганты влияют на причину развития и тромбы.
- Компламин, Никотиновая кислота – поскольку изменяется кровообращение и нарушается кровеносная система, сосудорасширяющие медикаменты просто необходимы.
- Экстракт алоэ – стимуляторы биогенного процесса.
- Но-шпа, Папаверин – данные спазмолитики понижают давление в сосудах.
Все лекарства назначаются офтальмологом исходя из индивидуальных особенностей человека и клинической картины.
Физиотерапия
Физиотерапевтические процедуры на сегодняшний момент не менее действенны, нежели использование медикаментов.
Наиболее эффективными считаются:
- Генная терапия – посредством модификаций с ДНК специалистам удаётся возобновлять нарушенные гены. Вследствие чего болезненные процессы останавливаются, у пациента улучшается зрение.
- Стимулирующие мероприятия (электростимуляция, магнитотерапия) – усиливают ещё живые фоторецепторы. У уцелевших тканей повышается функциональность, они заменяют омертвлённые клетки.
- Подсоединение электронных имплантатов – такие микроскопические частицы позволяют совершенно слепым пациентам без преграды ориентироваться в пространстве, полностью за собой ухаживать без чьей-либо помощи. Но не избавляет от самого недуга.
- Аппарат «Очки Сидоренко» — устройство направлено на предотвращение прогрессирования пигментной дистрофии, налаживает кровоснабжение. Метод обладает 4-кратным воздействием.
- Вазореконструктивное лечение – оперативное вмешательство, с помощью которого нормализуется правильный уровень кровоснабжения, а также питание фоторецепторов.
Такой лечебный подход позволяет нормализовать обмен веществ в патологическом органе, завести механизм возобновления нервных клеток. Оперативный способ разрешает частично улучшить зрение, потерянное вследствие генных мутаций, инфекционных патологий, травм.
Дополнительно можно использовать и народные методы, например, производить примочки из лечебных трав, принимать приготовленные отвары, настойки внутрь.
Аппаратное воздействие
Заболевание устраняется посредством фотостимуляции. Метод состоит в будораживании зрительного аппарата в определённых участках. В итоге развитие недуга замедляется. Под влиянием излучения кровообращение улучшается, налаживаются обменные процессы. Процедура убирает отёчность с оболочки глаз, укрепляет сетчатку.
Лечение возрастной дистрофии
Обязательно употребляются витамины. Взрослому человеку назначают лазерную коррекцию. Способ помогает разрушению повреждённых сосудов, уменьшающих зрительную остроту.
Офтальмолог помимо этого прописывает антиангиогенные лекарства и использование очков с линзами, снабжённые электронной системой. Может потребоваться субмакулярное оперативное вмешательство, где устраняются патологические сосуды. Выполняется транслокация глазной сетчатки, которую как бы слегка передвигают с области поражения сосудов, затем лазером производят операцию.
В некоторых случаях используется витрэктомия, операция предполагает иссечение стекловидного тела, рубцовой ткани.
Какие могут быть последствия
Симптоматика при пигментной дегенерации появляется в момент, когда сетчатка уже нарушена, поэтому распознать повреждение на первом этапе развития очень трудно. Истощение тканей способно привести к следующим осложнениям:
- глаукома, катаракта;
- понижение зрительной остроты;
- полная слепота;
- утрата периферического зрения;
- тоннельное видение;
- нарушение возможности видеть в темноте.
Чтобы не допустить таких последствий, важно произвести комплексное лечение, полностью придерживаясь рекомендаций.
Профилактика, прогноз
Поскольку образование пигментной дистрофии характеризуется генетическими расстройствами, предотвратить болезнь не получится. Чтобы заметить недуг вначале его развития, нужно регулярно посещать окулиста, особенно когда в роду имеются близкие с данным отклонением.
Для упрочнения сетчатки, а также оснащения глазных яблок нужными компонентами, человек полноценно должен питаться, исключить вредные привычки. Поступление в организм полезных для здоровья веществ становятся гарантией правильной работы органа зрения. При выявлении запущенной формы дегенерации сетчатки прогноз неутешительный, высока вероятность потери зрения.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 16 марта 2018;
проверки требуют 13 правок.
Пигментный ретинит (RP) — наследственное, дегенеративное заболевание глаз, которое вызывает сильное ухудшение зрения и часто слепоту[1]. Прогрессирование RP не является последовательным. Некоторые люди могут иметь симптомы с детства, другие могут заметить симптомы позднее[2]. В общем, чем позже начало, тем быстрее ухудшение зрения. Те, кто не имеет RP, имеют 90-градусное периферийное зрение, в то время как люди, имеющие RP, имеют периферийное зрение менее 90 градусов.
Как форма дистрофии сетчатки, RP вызвана аномалиями фоторецепторов (палочек и колбочек) или пигментного эпителия сетчатки (ПЭС) , ведущими к прогрессирующей потере зрения. Пострадавшие люди могут испытывать дефектную адаптацию от светлого к тёмному, от тёмного к светлому или никталопию (ночную слепоту), в результате дегенерации периферического поля зрения (так называемое туннельное зрение). Иногда раньше теряется центральное зрение, вынуждая человека смотреть искоса на объекты.
Эффект RP лучше всего иллюстрируется сравнением с экраном телевизора или компьютера. Светящиеся пикселы, формирующие изображение на экране можно приравнять к миллионам световых рецепторов на сетчатке глаза. Чем меньше пикселей на экране, тем менее отчётливо будет отображаться изображение. Менее 10 процентов фоторецепторов в глазе способны воспринимать цвет, при высокой интенсивности света в условиях яркого освещения или дневного света. Эти рецепторы расположены в центре круга сетчатки. Остальные 90 процентов фоторецепторов получают серую шкалу при низкой интенсивности света, используются при низкой освещённости и ночном видении и расположены по периферии сетчатки. RP разрушает световые рецепторы снаружи внутрь, от центра к краю, или по спорадическим путям с соответствующим снижением эффективности зрения. Это вырождение является прогрессирующим и не имеет никакого известного лечения.
Признаки и симптомы[править | править код]
Тот же вид с туннельным зрением от пигментного ретинита. Чернота вокруг центра изображения указывает не на тьму, а на отсутствие визуальной информации.
RP характеризуется прогрессирующей потерей фоторецепторов и в конечном итоге может привести к слепоте[3]. У людей могут возникнуть один или несколько следующих симптомов:
- Ночная слепота или никталопия;
- Туннельное зрение (отсутствует периферийное зрение);
- Периферийное зрение (отсутствует центральное зрение);
- Сеточное зрение;
- Антипатия к яркому свету;
- Медленная регулировка от темного к светлому, и наоборот;
- Нечеткость зрения;
- Плохое различение цветов;
- Крайняя усталость.
Ассоциированные условия[править | править код]
RP может быть:
(1) несиндромальной, то есть, это происходит в одиночку, без каких-либо других клинических данных,
(2) Синдромный с другими нейросенсорными расстройствами, нарушениями развития или сложными клиническими данными, или
(3) Вторичным к другим системным заболевания[4].
- RP в сочетании с глухотой (врождённой или прогрессирующей) называется синдромом Ушера.
- RP в сочетании с офтальмоплегией, дисфагией, атаксией, и пороками сердца, видимыми как митихондриальным DNA нарушением — Синдром Барде — Бидля (также известный как рваная красная волоконная миопатия)
- RP в сочетании с отсталостью, периферической невропатией, акантозными (с шипами) эритроцитами, атаксией, стеатореей, указывает на недостаток ЛПОНП, видимо из-за абеталипопротеинемии.
- RP с клинически видимым сочетанием с рядом других редких генетических заболеваний (в том числе мышечной дистрофией и хронической гранулематозной болезнью) как часть синдрома Маклеода. Это X-хромосомный рецессивный фенотип характеризуется полным отсутствием поверхностных XK-клеточных белков, и поэтому указывает на снижение экспрессии всех красных кровяных клеток келл-антигенов. Для целей переливания эти пациенты считаются полностью несовместимы со всеми нормальными и К0 / К0 донорами.
- RP, связанные с гипогонадизмом, и задержкой развития с аутосомно-рецессивным типом наследования, по-видимому с синдромом Лоуренс-Луна-Барде-Biedl
Другие условия включают в себя нейросифилис, токсоплазмоз ( Emedicine «Retinitis Pigmentosa») и синдром Рефсума.
Генетика[править | править код]
Пигментный ретинит (RP) является одним из наиболее распространённых форм наследственной дегенерации сетчатки[5]. Существуют различные гены, которые, будучи мутированы, способны привести к фенотипу пигментного ретинита[6]. В 1989, мутаций в гене родопсина, пигмент, который играет существенную роль в визуальной фототрансдукции в условиях низкой освещённости, выявлено не было. С тех пор, более 100 мутаций были обнаружены в этом гене, что составляет 15% от всех видов дегенерации сетчатки. Большинство из этих мутаций миссенс-мутации и наследуются в основном в доминирующей манере.
Типы включают в себя:
| OMIM | Ген | Тип |
|---|---|---|
| 180100 | RP1 | Пигментный ретинит-1 |
| 312600 | RP2 | Пигментный ретинит-2 |
| 300029 | RPGR | Пигментный ретинит-3 |
| 608133 | PRPH2 | Пигментный ретинит-7 |
| 180104 | RP9 | Пигментный ретинит-9 |
| 180105 | IMPDH1 | Пигментный ретинит-10 |
| 600138 | PRPF31 | Пигментный ретинит-11 |
| 600105 | CRB1 | Пигментный ретинит-12, аутосомно-рецессивный |
| 600059 | PRPF8 | Пигментный ретинит-13 |
| 600132 | TULP1 | Пигментный ретинит-14 |
| 600852 | CA4 | Пигментный ретинит-17 |
| 601414 | HPRPF3 | Пигментный ретинит-18 |
| 601718 | ABCA4 | Пигментный ретинит-19 |
| 602772 | EYS | Пигментный ретинит-25 |
| 608380 | CERKL | Пигментный ретинит-26 |
| 607921 | FSCN2 | Пигментный ретинит-30 |
| 609923 | TOPORS | Пигментный ретинит-31 |
| 610359 | SNRNP200 | Пигментный ретинит 33 |
| 610282 | SEMA4A | Пигментный ретинит-35 |
| 610599 | PRCD | Пигментный ретинит-36 |
| 611131 | NR2E3 | Пигментный ретинит-37 |
| 268000 | MERTK | Пигментный ретинит-38 |
| 268000 | USH2A | Пигментный ретинит-39 |
| 612095 | PROM1 | Пигментный ретинит-41 |
| 612943 | KLHL7 | Пигментный ретинит-42 |
| 268000 | CNGB1 | Пигментный ретинит-45 |
| 613194 | BEST1 | Пигментный ретинит-50 |
| 613464 | TTC8 | Пигментный ретинит 51 |
| 613428 | C2orf71 | Пигментный ретинит 54 |
| 613575 | ARL6 | Пигментный ретинит 55 |
| 613617 | ZNF513 | Пигментный ретинит 58 |
| 613861 | DHDDS | Пигментный ретинит 59 |
| 613194 | BEST1 | Пигментный ретинит, концентрический |
| 608133 | PRPH2 | Пигментный ретинит, дигенический |
| 613341 | LRAT | Пигментный ретинит, ювенильный |
| 268000 | SPATA7 | Пигментный ретинит, ювенильный, аутосомно-рецессивный |
| 268000 | CRX | Пигментный ретинит, запоздалый доминирующий |
| 300455 | RPGR | Пигментный ретинит, X-хромосомный, с синореспираторной инфекцией, с глухотой или без неё |
Ген родопсина кодирует главный белок наружных сегментов фоторецепторов. Исследования показывают, что мутации в этом гене ответственны примерно за 25% аутосомно-доминантных форм RP[5][7].
Мутации в четырёх пре-мРНК факторах сплайсинга как известно, вызывают аутосомно-доминантный пигментный ретинит. Это PRPF3 (человек с PRPF3 является с HPRPF3, а также с PRP3), PRPF8 , PRPF31 и PAP1 . Эти факторы экспрессируются повсеместно, и предполагается, что дефекты в повсеместном факторе (белок, экспрессируемый повсеместно) должны вызывать заболевание только в сетчатке, так как клетки фоторецепторов сетчатки имеют гораздо большую потребность в обработке белка (родопсина), чем любой другой тип клеток.
О свыше 150 мутациях, зарегистрированных на сегодняшний день в гене опсина, связанного с RP мутацией Pro23His в интрадискальном домене белка впервые было сообщено в 1990 году. Эти мутации встречаются по всему гена опсина и распределяются по трём областям белка (внутридисковому, трансмембранному и цитоплазматическому доменам). Одной из основных биохимических причин RP в случае мутаций белка родопсина является фолдинг белка и молекулярные шапероны.[8] Было обнаружено, что мутация кодона 23 в гене родопсина, в котором пролин преобразуется в гистидин, приходится наибольшая доля мутаций родопсина в Соединённых Штатах. Ряд других исследований сообщили о других мутациях, которые также коррелируют с болезнью. Эти мутации включают Thr58Arg, Pro347Leu, Pro347Ser, а также удаление Ile-255[7][9][10][11][12]. В 2000 году сообщалось о редкой мутации в кодоне 23 вызывающей аутосомно-доминантный пигментный ретинит, в которой пролин изменялся на аланин. Тем не менее, это исследование показало, что дистрофии сетчатки, связанная с этой мутацией была характерна мягкая форма и течение. Кроме того, тем более сохранено в электроретинографии амплитуд, чем более преобладала мутация Pro23His[13].
Патофизиология[править | править код]
Опыты на животных показывают, что пигментный эпителий неудачно фагоцитирует потерянные палочки внешнего сегмента диска, что ведёт к накоплению мусора из палочек внешнего сегмента. У мышей с гомозиготно-рецессивной дегенеративной мутацией сетчатки палочки фоторецепторов прекращают развитие и подвергаются дегенерации до завершения созревания клеток. Также присутствует дефект цГМФ-фосфодиэстеразы; это приводит к токсичным уровням цГМФ.
Симптомы[править | править код]
Пигментный ретинит (как правило, называют «RP») является заболеванием, которое характеризуется потерей светочувствительных клеток фоторецепторов, расположенных в задней части глаза, как плёнка в камере. Обычно палочки фоторецепторов (ответственные за ночное зрение) поражаются первыми, поэтому потеря ночного зрения (никталопия), является как правило, первым симптомом. Дневное зрение (при посредничестве колбочек) обычно сохраняется до поздних стадий заболевания. Пятнистость пигментного эпителия сетчатки с чёрной боне-спикулярной пигментацией (или патогномоничный симптом, как правило, указывает из пигментный ретинит. Другие глазные функции включают в себя паллор головки зрительного нерва, ослабление (истончение) сосудов сетчатки, целлофановую макулопатию, кистозный макулярный отёк и заднюю субкапсулярную катаракту.
Диагностика[править | править код]
Диагноз пигментного ретинита опирается на документацию прогрессирующей потери функций клеток фоторецепторов посредством электроретинографии (ЭРГ) и визуального тестирования поля.
Режим наследования RP определяется историей семьи. По крайней мере, 35 различных генов или локусов, как известно, вызывают «несиндромальный RP» (RP, не являющийся результатом другого заболевания или частью более широкого синдрома).
ДНК-тестирование доступно на клинической основе для:
- RLBP1 (аутосомно-рецессивный, тип Bothnia RP)
- RP1 (аутосомно-доминантный, RP1)
- RHO (аутосомно-доминантный, RP4)
- RDS (аутосомно-доминантный, RP7)
- PRPF8 (аутосомно-доминантный, RP13)
- PRPF3 (аутосомно-доминантный, RP18)
- CRB1 (аутосомно-рецессивный, RP12)
- ABCA4 (аутосомно-рецессивный, RP19)
- RPE65 (аутосомно-рецессивный, RP20)
Для всех других генов (например, DHDDS), молекулярное генетическое тестирование доступно только на исследовательской основе.
RP может быть унаследован аутосомно-доминантным, аутосомно-рецессивным, или Х-хромосомым образом. Х-хромосомный RP может быть или рецессивный, затрагивающий в первую очередь только мужчин, или доминирующий, затрагивающие как мужчин, так и женщин, хотя на мужчин, как правило, более мягко влияет. Некоторые дигенические (контролируемые двумя генами) и митохондриальные формы были также описаны.
Генетическое консультирование зависит от точного диагноза, определения типа наследования в каждой семье, и результатов молекулярно-генетического тестирования.
Лечение[править | править код]
В настоящее время нет лекарств от пигментного ретинита, но лечение, теперь доступно в некоторых странах. Прогрессирование заболевания может быть снижено за счёт ежедневного потребления 15000 МЕ (соответствует 4,5 мг) витамина А пальмитата у некоторых пациентов[14]. Последние исследования показали, что правильные витаминные добавки могут отсрочить слепоту до 10 лет (за счёт снижение годовых потерь с 10% до 8,3%) у некоторых пациентов в определённых стадиях заболевания[15]., Получивший признание на рынке, в феврале 2011 года, протез сетчатки Argus стал первым одобренным средством для лечения этого заболевания, доступен в Германии, Франции, Италии и Великобритании. Операция протезирования здесь описана. Промежуточные результаты долгосрочных исследований 30 пациентов были опубликованы в 2012 году[16].
Имплантат сетчатки Argus II также получил разрешение для экспериментального использования в США.[17][18][19] Устройство может помочь взрослым с RP, которые потеряли способность воспринимать формы и движения, чтобы быть более мобильными и выполнять ежедневные мероприятия. В июне 2013 года 12 больниц в США объявили в ближайшее время начать консультации для пациентов с RP в рамках подготовки к запуску Argus II в том же году[20].
Исследования[править | править код]
Лечение в будущем может включать трансплантацию сетчатки, искусственные имплантаты сетчатки[21], генную терапию, стволовые клетки, пищевые добавки, и / или лекарственную терапию.
2006: Стволовые клетки: Исследователи Великобритании, работающие с мышами, пересаживали мышам стволовые клетки уже на продвинутой стадии развития, и уже программировали развитие клеток фоторецепторов мышей, которые были генетически индуцированны, чтобы имитировать человеческие условия пигментного ретинита и возрасто-зависимую дегенерацию жёлтого пятна. Эти фоторецепторы развились и сделали необходимые нервные связи в сетчатке глаза животного, ключевой шаг в восстановлении зрения. Ранее считалось, что зрелая сетчатка не имеет регенеративной способности. Это исследование может в будущем привести к использованию пересадки на людях, чтобы облегчить слепоту[22].
2008: Учёные Биологического научного института Осака выявили белок, названный Пикачурин, который, по их мнению, может привести к лечению пигментного ретинита [23][24]
2010: Доступная генная терапия, кажется, работает на мышах[1].
2010: R-Tech Ueno (японский медицинское производственное предприятие) завершает вторую фазу клинических исследований офтальмологического раствора UF-021 (название продукта Ocuseva (TM)) для пигментного ретинита.
2012: Учёные из Медицинского центра Колумбийского университета показали, на животной модели, что генная терапия и терапия индуцированных плюрипотентных стволовых клеток могут быть жизнеспособными вариантами для лечения пигментного ретинита в будущем[25].
2012: Учёные из Университета Майами института глаза Баском Палмер представили данные, показывающие защиту фоторецепторов в животной модели, когда в глаза были введены мезенцефалические астроциты нейротрофического фактора (MANF)[26].
2014: исследование