Бржеский лечение синдрома сухого глаза
Дата публикации 11 ноября 2019 г.Обновлено 11 ноября 2019 г.
Определение болезни. Причины заболевания
Синдром сухого глаза (сухой кератоконъюнктивит) — это воспалительное состояние глаза, при котором слёзная плёнка изменяется по своему химическому и количественному составу. Проявляется комплексом симптомов, таких как жжение, чувство рези и инородного тела в глазу.
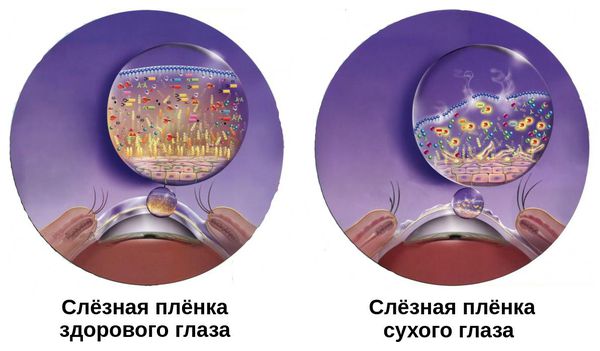
По данным различных авторов, сухость глаза встречается примерно у 15-17 % взрослых, проживающих в развитых странах. Этот показатель каждый год увеличивается. За последние 30 лет синдром сухого глаза стал встречаться в 4,5 раза чаще [1].
Одна из причин такого увеличения распространённости синдрома связана с развитием рефракционных хирургических вмешательств — лазерного кератомилёза, фоторефракционной кератэктомии, передней радиальной кератотомии и других. Во время этих операций нарушается иннервация роговицы.
На рост данной патологии также оказывают влияние:
- повсеместное использование смартфонов, планшетов, компьютеров, другого офисного оборудования, а также кондиционеров, так как они высушивают воздух;
- ношение мягких контактных линз;
- регулярный приём лекарств — мочегонных, противоаллергических препаратов, антидепрессантов, средств для снижения холестерина, бета-блокаторов, противозачаточных таблеток [1].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы синдрома сухого глаза
Часто встречаемые симптомы [11]:
- раздражение (покраснение) глаз;
- ощущение инородного тела в глазах;
- чувство жжения;
- слизистое отделяемое в виде нитей;
- периодические «затуманивание».
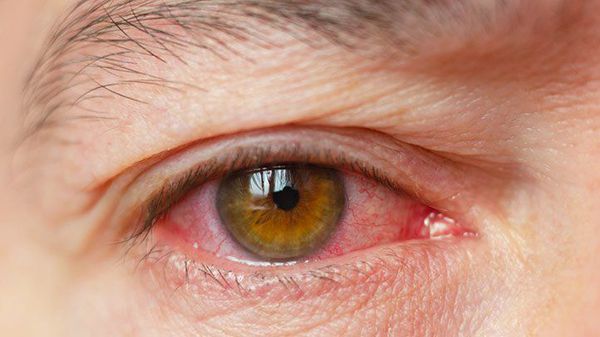
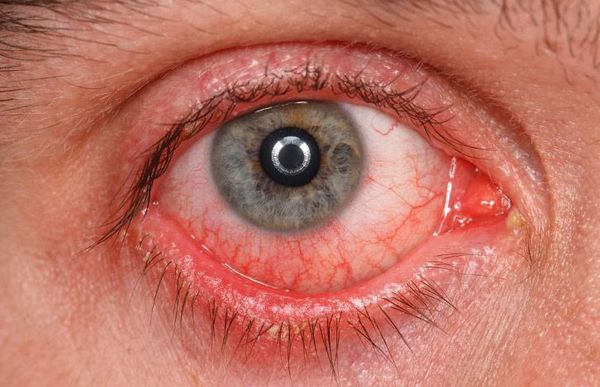
Реже наблюдается зуд в глазу, светобоязнь, утомление или чувство тяжести в глазах. При этом чувства стянутости и давления за глазами не возникают.
Как правило, все перечисленные симптомы проявляются на обоих глазах, но иногда они возникают только в одном глазном яблоке.
Любопытно, что пациенты с синдромом сухого глаза редко жалуются на сухость глаз, хотя иногда они отмечают нехватку эмоциональных слёз или отсутствие слезотечения в ответ на раздражитель, например, лук. В некоторых случаях пациентов беспокоит слезотечение, особенно на улице, так как там много раздражающих факторов — яркое солнце, ветер, холод. От возникающего слезотечения они испытывают дискомфорт.
Признаки сухого кератоконъюнктивита часто усиливаются из-за воздействия внешних факторов, связанных с повышенным испарением слезы от ветра, кондиционера, отопления или при длительном чтении, так как человек начинает реже моргать. При закрытых веках симптомы уменьшаются [5].
Патогенез синдрома сухого глаза
Патогенез сухого кератоконъюнктивита связан с нарушением стабильности слёзной плёнки. Она покрывает переднюю поверхность глаза. В норме её толщина составляет около 10 мкм. При развитии синдрома она становится тоньше.
Распределение слёзной плёнки поверхности глаза происходит благодаря рефлекторному морганию. Для её эффективного распределения должны сочетаться несколько факторов:
- нормальный моргательный рефлекс;
- контакт век и глазной поверхности;
- нормальный эпителий (внешний слой) роговицы.
Слёзная плёнка неоднородна. Она имеет три слоя:
- первый (внешний) слой — липидный — вырабатывается мейбомиевыми железами;
- второй слой — водный — вырабатывается слёзными железами;
- третий слой — муциновый — вырабатывается бокаловидными клетками роговицы.
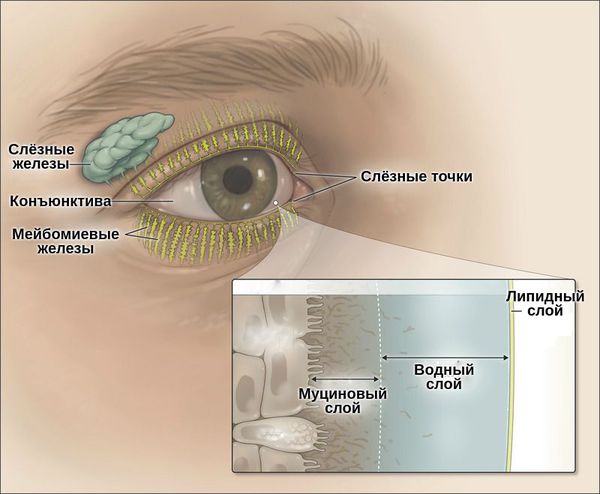
Липидный слой — самый тонкий. Его основная задача — задерживать испарения водного слоя и поддерживать слёзную плёнку. При его нехватке увеличивается испаряемость слезы, что приводит к «сухому глазу».
Водный слой является основой слёзной плёнки. Он состоит из воды, электролитов и белков. За счёт непрерывного обновления он выполняет своё предназначение — доставляет кислород к эпителию роговицы, защищает от бактерий, вымывает инородные тела, обеспечивает гладкость и ровность оптической поверхности.
Муциновый слой состоит из муцинов, которые помогают слёзной плёнке удерживаться на роговице. Он увлажняет и смазывает роговичный эпителий. Его дефицит может быть вызван как нехваткой водного слоя, так и высокой испаряемостью слёзной жидкости. Другой причиной нарушения муцинового слоя может стать повреждение бокаловидных клеток, которые его продуцируют. Это происходит при рубцующемся конъюнктивите, нехватке витамина А, химических ожогах, токсическом воздействии медикаментов [3].
Исходя из особенностей строения слёзной плёнки, патогенез сухого кератоконъюнктивита затрагивает несколько звеньев образования и функционирования слёзной плёнки [1]:
- выработка слезы, муцинов и липидов;
- скорость испарения слёзной плёнки;
- образование слёзной плёнки на поверхности эпителия роговицы.
Классификация и стадии развития синдрома сухого глаза
Единой классификации данного синдрома пока нет, но существует несколько авторских классификаций. Вот некоторые из них.
Национальный глазной институт Америки выделяет две основные категории синдрома:
- Снижение выработки слезы:
- синдром Шегрена — нарушение работы слюнных и слёзных желёз, которое приводит к развитию синдрома сухого глаза;
- снижение выработки слезы, не связанное с синдромом Шегрена.
- Увеличение испарения слезы:
- воспалительное заболевание мейбомиевой железы;
- атрофия мейбомиевых желёз.
Доктор B. Dohlman классифицирует синдром в зависимости от причин снижения слезопродукции слёзным железами:
- Дефицит слезопродукции — обычно связан со скоплением лимфоцитов в ткани слёзной железы:
- синдром Шегрена;
- коллагеноз (синдром Райли — Дея) — редкое наследственное заболевание, которое поражает периферическую нервную систему.
- Дефицит муцина:
- синдром Стивенса Джонсона — тяжёлая системная аллергия, которая снижает защитные свойства муцина;
- глазной пемфигоид — хроническое заболевание глаз аутоиммунного генеза, приводит к недостатку муцина;
- авитаминоз витамина А, который входит в состав муцина.
- Изменённая поверхность роговицы — наблюдается при трахоме (хроническом конъюнктивите, вызванном хламидиями), простом герпесе, роговичных дистрофиях. Повреждённые места уязвимы для инфекций и появления язв.
- Недостаточность увлажнения. Связана с нейропаралитическим кератитом — воспалительно-дистрофическим изменением роговицы на фоне поражения тройничного нерва. Проявляется снижением или отсутствием чувствительности роговицы, невралгическими болями, помутнением и язвой роговицы.
Азиатское общества сухих глаз (ADES) также классифицирует синдром по причинам его возникновения [2]:
- дефицит воды;
- снижение смачиваемости;
- увеличение испарения.
По клиническим проявлениям — жжению, зуду, рези, ощущению тяжести и инородного тела в глазах, слезотечению, светобоязни, уменьшению симптомов после закрытия глаз — синдром сухого глаза бывает:
- слабым — 1-2 симптома;
- умеренным — 3-5 симптомов;
- тяжёлым — более 5 симптомов.
Осложнения синдрома сухого глаза
В зависимости от стадии синдрома у человека может временно ухудшаться зрение, которое восстанавливается при моргании.
Сухость глаза повышает вероятность возникновения бактериального кератита и частого изъязвления, которые могут стать причиной появления перфорации роговицы [5]. Клинически бактериальный кератит проявляется:
- острой болью в глазу;
- отёком;
- корнеальным синдромом — светобоязнью, слезотечением, непроизвольным «зажмуриванием»;
- выраженной воспалительной инъекцией глазного яблока;
- слизисто-гнойными выделениями;
- помутнениями роговицы;
- поверхностными или глубокими изъязвлениями роговицы.
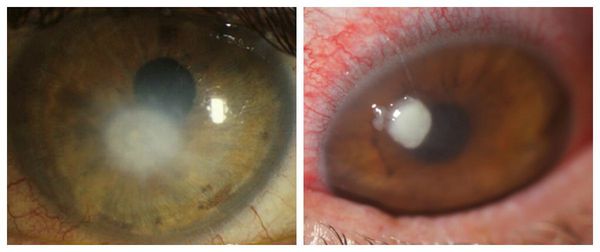
Перфорация роговицы опасна серьёзным снижением зрения, которое может потребовать пересадку роговицы.
Диагностика синдрома сухого глаза
При проведении биомикроскопии врач-офтальмолог может разглядеть признаки нарушения слёзной плёнки и роговицы.
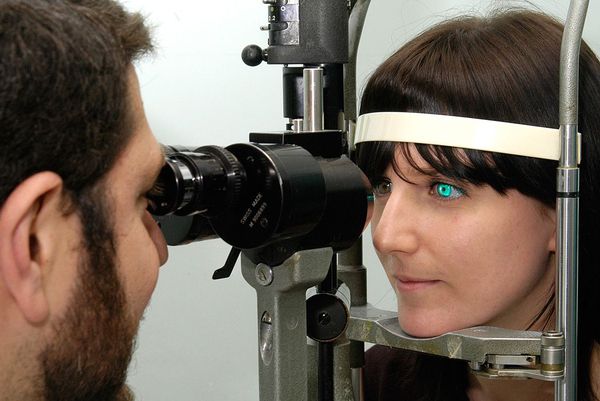
Нарушения слёзной плёнки:
- Появление нитей муцина — признак раннего сухого кератоконъюнктивита. В здоровом глазу после разрыва слёзной плёнки муциновый и липидный слои смешиваются и быстро смываются. При синдроме сухого глаза муцин также смешивается с липидным слоем, но не вымывается, а скапливается в слёзной плёнке и смещается при мигании.
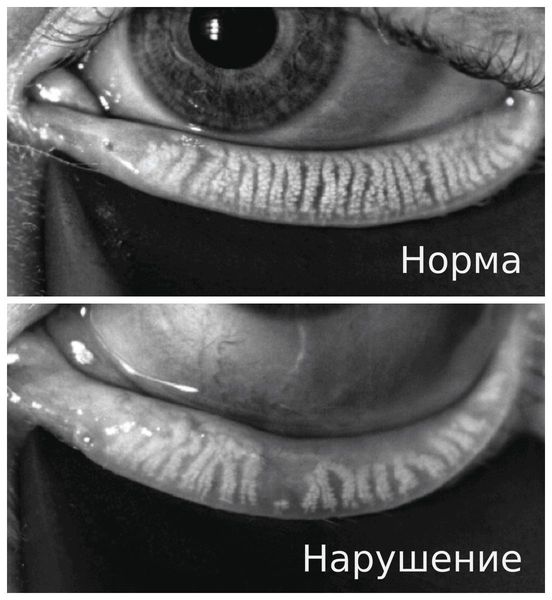
- Уменьшение слёзного мениска — объёма водного слоя слёзной плёнки. В норме он представляет собой выпуклую полосу с правильным верхним краем. При сухом кератоконъюнктивите слёзный мениск становится вогнутым, неравномерным, тонким, а иногда вовсе исчезает.
- Отделяемое в виде пены — возникает в слёзной плёнке или по краю века при нарушении работы мейбомиевых желёз.
Нарушения роговицы:
- Точечная эрозия роговицы — возникает в нижней половине роговицы.
- Появление роговичных нитей. Они состоят из небольших комочков слизи в форме запятой. Одни концы нитей прикрепляются к поверхности роговицы, другие свободно двигаются при мигании.
- Наличие нитчатых инфильтратов — полупрозрачные бело-серые немного выпуклые образования. Как правило, их обнаруживают одновременно с нитями слизи во время окрашивания бенгальским розовым красителем [5].
Для подтверждения и постановки диагноза сухости глаз также проводят различные тесты. Чем выраженнее синдром, тем они надёжнее. Во время тестов измеряют следующие параметры [3]:
- стабильность слёзной плёнки и время её разрыва;
- выработка слезы — тест ширмера, осмолярность слезы;
- заболевание глазной поверхности — окрашивание поверхности глаза.
Тест на время разрыва слёзной плёнки
Время разрыва слёзной пленки — показатель её стабильности. Его измеряют следующим образом:
- в нижний свод конъюнктивы закапывают флуоресцеин;
- просят пациента мигнуть несколько раз, а затем не моргать;
- через щелевую лампу с кобальтовым синим фильтром исследуют срез слёзной плёнки.
Через некоторое время в окрашенной плёнке возникают чёрные линии или пятна, которые указывают на появление сухих участков. Важно зафиксировать время между последним миганием и появлением первых сухих участков. Если данный промежуток длится менее 10 секунд, то это отклонение от нормы.
Тест Ширмера
Данный тест проводят для оценки слезопродукции. С его помощью измеряют увлажнённую часть специальными бумажными фильтрами. Тест проводят следующим образом:
- осторожно убирают имеющуюся слезу;
- согнутый бумажный фильтр помещают в полость конъюнктивы, не касаясь роговицы;
- просят пациента не закрывать глаз и моргать как обычно;
- через пять минут фильтры убирают и оценивают уровень увлажнения: 6-10 мм — это норма, диапазон менее 6 мм указывает на снижение выработки слезы.
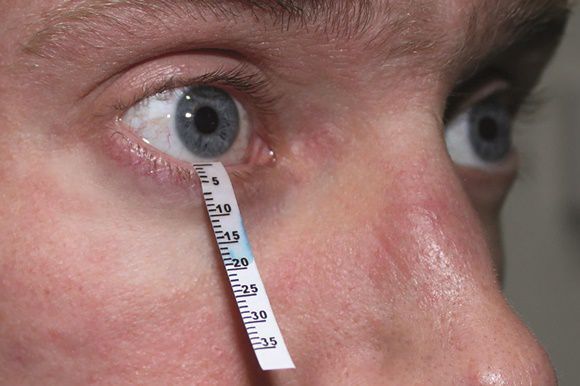
Тест с окрашиванием глазной поверхности
Специальные красители используют для окрашивания нежизнеспособных клеток муцина. Бенгальский розовый краситель прокрашивает изменённую поверхность роговицы в виде двух треугольников. Роговичные нити и инфильтраты также окрашиваются, но ещё интенсивнее. Минусом бенгальского розового в том, что он может вызвать гиперемию (покраснение) глаз, особенно при выраженном синдроме [5]. Тест с лиссаминовым зелёным вызывает меньше раздражения.
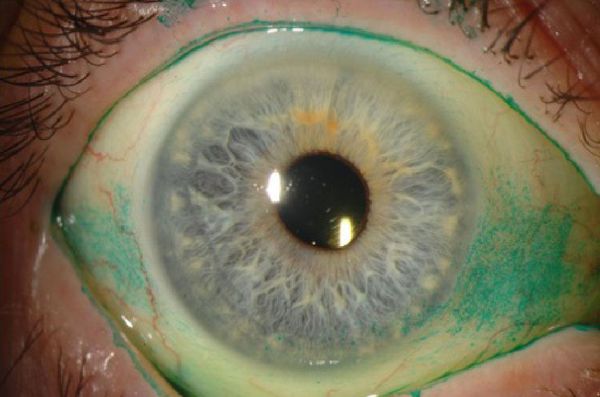
Другие способы диагностики
Помимо основных перечисленных методов диагностики иногда используют следующие тесты [3]:
- осмолярность слёзной плёнки;
- измерение состава слезы;
- слёзная менискометрия;
- импрессионная цитология;
- тест на лактоферрин;
- тест красной нити фенола;
- клиренс-флюоресцииновый тест.
Также применяется мейбография — бесконтактная визуальная оценка структуры мейбомиевых желёз. Она проводится независимо от возраста и пола пациента [9]. Данный метод диагностики используется редко, так как он достаточно новый и не везде есть нужное оборудование.
Лечение синдрома сухого глаза
Главная задача при лечении «сухого глаза» — уменьшить неприятные ощущения, сохранить оптическую поверхность роговицы и не допустить повреждения её структур. Одновременно можно применять сразу несколько способов лечения [5].
Сохранение вырабатываемой слезы:
- Уменьшение комнатной температуры — позволяет минимизировать испарения слёзной плёнки.
- В помещении можно использовать увлажнители воздуха, но чаще всего это не даёт результатов. Аппарат не способен значительно увеличить относительную влажность воздуха. Местно повысить влажность можно при помощи специальных очков. У них есть съёмная прокладка, которая защищает глаза от ветра и других раздражающих факторов.

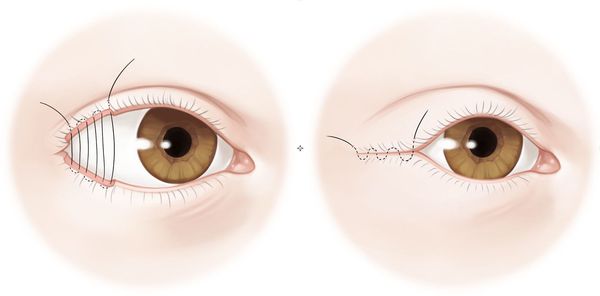
- Частичная боковая тарзорафия — операция, которая заключается в полном или частичном ушивании краёв век. Она уменьшает расстояние между веками глаза, чем может благотворно повлиять на состояние пациента.
Заместители слезы:
- Капли используются довольно часто. Их главный недостаток — короткий период действия и развитие чувствительности к консерванту.
- Гели состоят из карбомеров — заместителей слезы. Их приходится наносить не так часто, как капли, поэтому использование гелей предпочтительней.
- Также используют мази, которые содержат вазелин и минеральные липиды.
- Спреи для век обычно содержат средство на основе липосома. Они позволяют уменьшить испарение и стабилизировать слёзную плёнку.
Муколитические препараты
Ацетилцистеин 5 % в форме капель можно использовать для лечения пациентов с нитчатым кератитом и инфильтратами. Капли применяют четыре раза в день. Они могут вызвать покраснение после закапывания.
Уменьшение оттока слезы
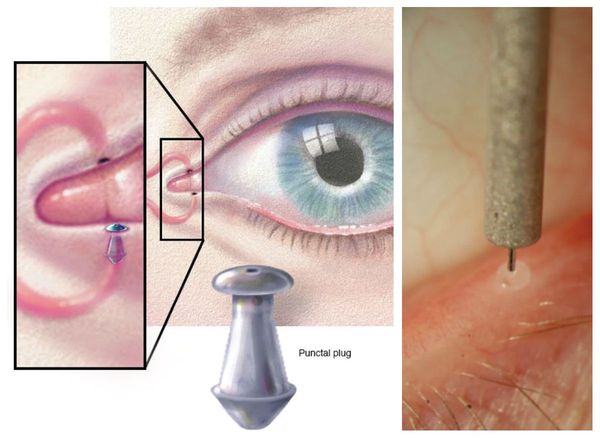
Окклюзия (закупорка) слёзной точки сохраняет отток слезы и продлевает эффект воздействия искусственных слёз. Это процедура показана пациентам с выраженным синдромом, особенно из-за токсичности консервантов.
Временная закупорка слёзной точки происходит при помещении коллагеновой заглушки в слёзные канальцы. Самая важная задача временной окклюзии — убедиться в том, что после неё не возникнет обильное слезотечение. Для временной окклюзии на несколько месяцев используются силиконовые заглушки. Постоянная окклюзия проводится пациентам с выраженным сухим кератоконъюнктивитом.
Другие варианты лечения:
- Местное использование циклоспорина 0,05 % или 0,1 % — безопасный, хорошо переносимый и эффективный препарат. Он позволяет уменьшить воспаление слёзной плёнки на уровне клеток.
- Системный приём холинергических препаратов типа пилокарпина — весьма эффективен в лечении ксеростомии — сухости во рту. У 40 % пациентов с сухим кератоконъюнктивитом наблюдается положительный эффект.
Лечение мейбомиевых желёз
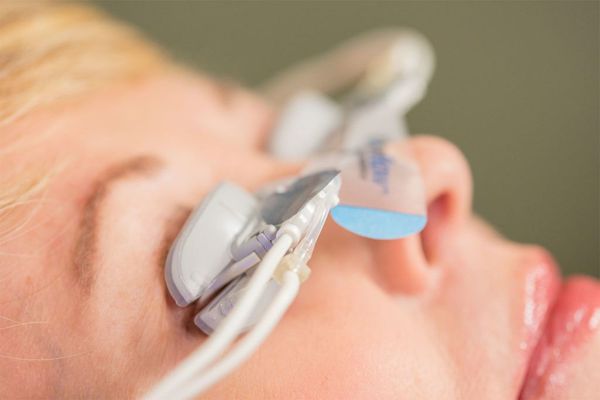
Нарушение работы данных желёз является основной причиной появления синдрома сухого глаза. Существует множество вариантов его лечения. Консервативные меры включают тёплые компрессы и гигиену век — наложение тёплых ватных дисков на пять минут, использование специальных гелей для век. Потенциальные медицинские методы лечения включают в себя антибиотики, нестероидные и стероидные противовоспалительные средства, добавки незаменимых жирных кислот, гормональную терапию и контроль инвазии демодекса — распространения клеща Demodex. Процедуры включают внутрипротоковое исследование мейбомиевых желёз, использование электронных нагревательных приборов, интенсивную импульсную световую терапию и интраназальную нейростимуляцию — электростимуляция нервных окончаний увеличивают производство слезы [7].
Прогноз. Профилактика
Причинные процессы, вызывающие сухость глаза, как правило, необратимы, поэтому лечение строится вокруг контроля симптомов и предотвращения повреждения поверхности.
Пациенту необходимо пересмотреть свой образа жизни:
- не носить контактные линзы дольше, чем рекомендует производитель;
- прекратить использование препаратов с потенциально токсическим воздействием (капли с консервантами);
- следить, чтобы уровень влажности в помещении был достаточным;
- чаще моргать во время чтения, просмотра телевизора или работы за компьютером;
- располагать экран так, чтобы он был ниже уровня глаз.
Интересно, что при ношении гарнитуры виртуальной реальности толщина липидного слоя и стабильность слёзной плёнки становится лучше, чем при использовании обычного настольного компьютера [8].
Выраженная сухость глаза у курильщиков электронных сигарет и вейперов указывают на потенциальный вред паров электронных сигарет и вейпов по отношению к глазам. Они ухудшают качество слёзной плёнки, из-за чего синдром сухого глаза становится умеренным или тяжёлым. Помимо пара на слёзную плёнку воздействуют опасные побочные продукты вейпа [4].
На качество слёз также влияет индекс массы тела. Как показало недавнее исследование, качество слезы у людей с высоким индексом массы тела было ниже, чем у людей с нормальным весом [10]. Поэтому правильно питание может снизить риск развития нарушений обмена веществ в организме, а следовательно и синдрома сухого глаза.
Хирургическое вмешательство является наиболее эффективным средством для повышения остроты зрения при катаракте. И хотя современные способы лечения катаракты безопасны и эффективны, после операции может развиться несколько осложнений, таких как кистозный макулярный отёк, а также сухость глаза. Причины послеоперационного «сухого глаза» пока не установлены. Поэтому если пациент планирует лазерную рефракционную операцию, то врач должен предупредить его, что эта процедура может привести к синдрому сухого глаза или усугубить его [3].
Препаратов, предназначенных для профилактики послеоперационного сухого глаза, пока не разработано. И хотя использование нестероидных противовоспалительных средств эффективно снижает частоту и степень послеоперационного кистозного макулярного отёка, они могут вызывать побочные эффекты, включая аномалии поверхности и сухость глаз. В связи с этим послеоперационные лекарства должны тщательно отбираться, чтобы улучшить результаты лечения и не допустить развитие сухого кератоконъюнктивита [6].
Источник
В статье представлены особенности патофизиологии и терапии синдрома «сухого глаза»

Введение
Согласно определению DEWSII 2017 г., синдром «сухого глаза» (ССГ) представляет собой мультифакториальное заболевание глазной поверхности, характеризующееся нарушением гомеостаза слезной пленки и сопровождающееся офтальмологическими симптомами, в развитии которых этиологическую роль играют нaрушение стабильности, гиперосмолярность слезной пленки, воспаление и повреждение глазной поверхности, а также нейросенсорные изменения [1]. У части больных это заболевание сопровождается осложнениями со стороны роговицы, которые могут привести не только к ухудшению зрительных функций, но и к потере глазного яблока. Общая распространенность ССГ в России у пациентов в возрасте до 40 лет составляет 12%, у пациентов старше 50 лет — более 67%. На офтальмологическом приеме диагноз ССГ ставится практически каждому второму пациенту [2–4].
Выделяют четыре степени тяжести ССГ: легкую, среднюю, тяжелую и особо тяжелую. Каждая из этих стадий характеризуется определенными субъективными симптомами и клиническими признаками ксеротических изменений поверхности глаза, сопровождаясь негативной динамикой показателей слезопродукции и времени разрыва слезной пленки (СП). Следует отметить, что при начальных проявлениях ССГ можно наблюдать компенсаторное увеличение рефлекторной слезопродукции, усиливающееся при воздействии на глаз неблагоприятных факторов внешней среды, что часто является причиной ошибочной диагностики.
К специфическим жалобам при ССГ относят болевую реакцию на инстилляции глазных капель, плохую переносимость ветра, дыма и кондиционированного воздуха, ощущение сухости в глазу. Кроме этого, пациенты часто описывают ощущение инородного тела, жжения и рези в глазу, светобоязнь, ухудшение зрительной работоспособности и колебания остроты зрения в течение рабочего дня.
К объективным признакам ССГ относятся уменьшение высоты слезных менисков, появление конъюнктивального отделяемого в виде слизистых и эпителиальных нитей, наличие параллельной краю века складки бульбарной конъюнктивы (тест LIPCOF). Также может наблюдаться наличие включений в СП и изменений эпителия роговицы дегенеративного характера.
Патогенез ССГ
При ССГ снижение секреции слезной жидкости приводит к воспалительной реакции в тканях глаза и поражению периферических нервов. Воспаление провоцирует сенситизацию нервных окончаний полимодальных и механоноцицепторов и аномальное повышение активности холодовых терморецепторов. Совокупность этих процессов ведет к появлению ощущения сухости и боли в глазу. Длительно присутствующее воспаление и повреждение нервных волокон изменяют экспрессию генов ионных каналов и рецепторов клеток тригеминального ганглия и нейронов клеток головного мозга, таким образом меняя их реакцию на раздражение и проведение нервного импульса. Также следует отметить, что пусковым механизмом может служить как воспаление, так и оксидативный стресс, который возникает при нарушении баланса между продукцией активных форм кислорода и факторов антиоксидантной защиты.
Нарушения на молекулярном, структурном и функциональном уровнях чувствительной иннервации глазного яблока вызывают дизестезию и нейропатические боли в глазу. Боль такого типа можно диагностировать с помощью специальных опросников, метода эстезиометрии и прижизненной конфокальной микроскопии [5–8]. Конфокальная микроскопия позволяет визуализировать нервные окончания и воспалительные клетки в тканях глазной поверхности. При ССГ могут определяться такие морфологические изменения, как повышенная извитость, рефлективность, однако без существенных изменений плотности нервных окончаний. В дополнение к указанному выше может наблюдаться увеличение плотности воспалительных клеток. При исследовании состава слезы выявляются повышение фактора роста нервов и снижение уровня кальцитонин ген-связанного пептида [9].
Лечение пациентов с ССГ
При подборе наиболее адекватной терапии ССГ руководствуются как стадией заболевания, так и особенностями симптоматических проявлений у конкретного пациента.
На первом этапе лечения ССГ в качестве базовых средств назначают различные заменители слезной жидкости (т. н. препараты «искусственной слезы»), отличающиеся в основном вязкостью и составом активных компонентов. Фармакологический эффект этих слезозаменителей в большинстве случаев обусловлен их действием на муциновый и водный слои прероговичной СП. Входящие в их состав полимеры (производные метилцеллюлозы и гиалуроновой кислоты, поливиниловый спирт, поливинилпирролидон и др.) смешиваются с нативной слезой и образуют собственную прероговичную пленку. Наиболее распространенным компонентом современных слезозаменителей является гиалуроновая кислота (ГК). ГК — естественный компонент слезы, способна связывать большое количество молекул воды и усиливать репаративные процессы в строме роговицы и бульбарной конъюнктиве, улучшая состояние эпителия роговицы и конъюнктивы [10–14].
Увлажняющие свойства ГК напрямую зависят от вязкости, которая определяется концентрацией ГК в составе слезозаменителя и ее молекулярным весом. Наиболее оптимальная концентрация ГК составляет от 0,1 до 0,3% [11]. При увеличении концентрации ГК более 0,3% также увеличивается и вязкость офтальмологического раствора, что может вызывать дискомфорт у пациентов при использовании слезозаместительного средства.
К средствам с низкой вязкостью, в частности, относятся Артелак Баланс и Артелак Баланс Уно (компания BauschandLomb), которые отличаются формой выпуска (мультидозы и монодозы). Эти слезозаменители включают ГК в виде натрия гиалуроната 0,15% и протектора (полиэтиленгликоль 8000). Протектор полиэтиленгликоль в составе Артелака Баланс способствует восстановлению муцинового слоя, действуя как временное защитное покрытие, позволяющее закрыть разрывы СП. Также есть данные о более выраженном увлажняющем действии ГК в присутствии полиэтиленгликоля. Исследование 2013 г. показало увеличение смачиваемости роговицы при добавлении полиэтиленгликоля к ГК. В то время как ГК повышала выживаемость клеток эпителия, дополнительное закапывание полиэтиленгликоля приводило к снижению поверхностного натяжения и повышению увлажнения поверхности глаза [15]. Таким образом, включение в состав полиэтиленгликоля позволяет увеличить степень и выраженность эффекта смачиваемости, который сохраняется даже после его удаления с поверхности глаза. Результаты этого исследования показывают, что концентрация ГК не является решающей для прогнозирования степени увлажняющего эффекта слезозаменителя. Следует принимать во внимание наличие дополнительных компонентов, усиливающих выраженность его действия. В состав Артелака Баланс и Артелака Баланс Уно входит также витамин В12, или цианокобаламин. Свойства цианокобаламина многообразны. Он участвует в процессах синтеза и конвертации активных веществ, а также в синтезе глутатиона — вещества с выраженными антиоксидантными свойствами [16, 17]. С учетом роли оксидативного стресса в развитии ССГ представляется патогенетически обоснованным назначение инстилляций препаратов с антиоксидантными свойствами [18, 19].
P. Versura et al. описывают результаты использования Артелака Баланс у пациентов со средней степенью выраженности симптомов ССГ в течение 2 мес., отмечая объективное уменьшение параметров воспаления глаз (показатели теста Ширмера, определение времени разрыва и осмолярности СП) и субъективное уменьшение выраженности симптомов дискомфорта [20].
Есть данные о результатах назначения Артелака Баланс у пациентов с ССГ средней степени тяжести на фоне вирусного гепатита С [21]. Отмечалось снижение выраженности симптомов ССГ, что можно объяснить защитным действием от повреждения свободными радикалами Артелака Баланс в отношении эпителия глазной поверхности и улучшением метаболических процессов в тканях глаза [21].
Наиболее показательным с точки зрения нейротрофических нарушений является состояние после перенесенных лазерных операций, в т. ч. LASIK. У данных пациентов наблюдаются проявления ССГ даже в отдаленном периоде после операции до 6 мес. за счет длительного восстановления иннервации роговицы. Этот период может увеличиваться до 1 года. Все это время пациентам необходимо назначение слезозаместительной терапии. Назначение Артелака Баланс, содержащего цианокобаламин, позволяет значительно сократить сроки реабилитации пациентов после лазерных операций за счет ускорения реиннервации роговицы.
В условиях эксперимента было показано положительное влияние цианокобаламина на реиннервацию роговицы у животных. На модели индуцированной эпителиальной эрозии результатом местного применения офтальмологического раствора, содержащего 0,05% цианокобаламин, 0,5% таурин и 0,5% натрия гиалуронат, в течение 10–30 дней было более раннее заживление эпителиальной раны, достигнуты более высокие темпы реиннервации роговицы по сравнению с результатами у животных, у которых применяли раствор, содержащий только 0,5% таурин и 0,5% натрия гиалуронат [22].
По результатам клинического исследования включение лубриканта с цианокобаламином в план предоперационной подготовки в виде 3-месячного курса и цианокобаламина в состав местной послеоперационной терапии у пациентов с высоким риском развития ССГ (длительное применение контактных линз) после LASIK снижает выраженность симптомов и жалоб, характерных для ССГ, а также потребность в длительном использовании лубрикантов в послеоперационном периоде через 1 мес. после выполнения операции [23].
Инстилляции цианокобаламина в составе глазных капель позволили снизить роль уже существующей нейропатии в развитии LASIK-ассоциированного вторичного ССГ. Положительный эффект слезозаменителя в отношении снижения выраженности и длительности симптомов ССГ был также обусловлен его назначением в рамках предоперационной подготовки.
Таким образом, Артелак Баланс и Артелак Баланс Уно способны оказывать комплексное действие на патогенетические звенья ССГ, что позволяет рекомендовать эти средства пациентам с различной выраженностью ССГ,
в т. ч. средней и тяжелой степенью.
Принимая во внимание, что у пациентов со средней тяжестью ССГ может потребоваться коррекция назначений, а эффект слезозаменителей низкой вязкости может быть недостаточным, врачу-офтальмологу следует переключить таких пациентов на инстилляции препаратов ГК средней и высокой вязкости. К таким средствам относятся слезозаменители Артелак Всплеск и Артелак Всплеск Уно (мульти- и монодозы). Артелак Всплеск включает натрия гиалуронат 0,24%, а монодозы — натрия гиалуронат в концентрации 0,2%. Преимуществом данных средств лечения ССГ является высокое содержание ГК. Кроме того, отсутствуют консерванты в обоих лекарственных формах. В Артелаке Всплеск стерильность раствора достигается за счет оригинальной конструкции флакона, которая предотвращает контаминацию. Артелак Всплеск Уно выпускается в монодозах по 0,5 мл, что позволяет четко рассчитать режим инстилляций, не хранить открытым тюбик-капельницу и не подвергать раствор инфицированию. Отсутствие консервантов снижает риск развития токсических и токсико-аллергических реакций при его применении. Таким образом, Артелак Всплеск можно назначать пациентам с аллергическими реакциями на консервант в среднетяжелой стадии ССГ.
При выраженном ССГ при симптомах кератопатии, особенно дегенеративных изменениях роговицы и конъюнктивы, терапию необходимо дополнять средствами, стимулирующими регенерацию тканей. К таким средствам относят Корнерегель (декспантенол 5%). Данный препарат сочетает в себе декспантенол в высокой концентрации и карбомер, который увлажняет поверхность глаза. Декспантенол стимулирует миграцию эпителиальных клеток в область поврежденного участка роговицы от периферии к центру и ускоряет их пролиферацию, а также влияет на образование нормальной структуры фибробластов в строме роговицы, что способствует восстановлению правильной многослойной структуры коллагеновых волокон в регенерированных участках и предотвращает образование рубцов в строме роговицы [24, 25].
Карбомер в составе Корнерегеля позволяет активному веществу дольше удерживаться на поверхности поврежденной роговицы, что обеспечивает также мягкий заживляющий эффект. Благодаря такому сочетанию компонентов Корнерегель не имеет аналогов по составу на российском рынке.
Заключение
Индивидуальный подбор средств слезозаместительной терапии в зависимости от вязкости раствора позволяет наиболее эффективно купировать симптомы ССГ у пациентов с различными стадиями заболевания. При наличии признаков кератопатии с дегенеративными изменениями рекомендуется дополнительное назначение средств из группы репарантов.
Учитывая, что ключевую роль в патогенезе ССГ у пациентов с системными инфекционными и неинфекционными заболеваниями играет оксидативный стресс, развивающийся вследствие воспаления на местном уровне, следует использовать не только слезозаместительные препараты для купирования симптомов ксерофтальмии, но и антиоксидантные препараты.
Сведения об авторе: Егоров Евгений Алексеевич —
д.м.н., профессор. ФГБОУ ВО РНИМУ им. Н. И. Пирогова Минздрава России. 117997, Российская Федерация, ъг. Москва, ул. Островитянова, д. 1. Контактная информация: Егоров Евгений Алексеевич, e-mail: egorov_ea@rsmu.ru. Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 06.08.2018.
About the author: Eugene A. Egorov — professor. Pirogov
Russian National Research Medical University. 1, Ostrovityanova str., Moscow, 117997, Russian Federation. Contact information: Eugene A. Egorov, e-mail: egorov_ea@rsmu.ru. Financial Disclosure: author hasn’t any financial or property interest in any material or method mentioned. There is no conflict of interests. Received 06.08.2018.
Источник


