Адгезия сетчатки что это
Стебнев В.С., Малов В.М.
Симптоматическая витреомакулярная адгезия (ВМА) представляет собой локальное прикрепление заднего гиалоида к поверхности сетчатки на фоне полного отслоения его от остальной поверхности сетчатки [Sebag J. et al., 2012]. При этом нарастающая витреомакулярная тракция вызывает анатомические нарушения в сетчатке, что приводит к развитию витреомакулярного тракционного синдрома [Carpineto P. et al., 2011]. В последние годы появилось мнение, что в зависимости от протяженности ВМА, от направленности и мощности витреомакулярной тракции поражение самой макулярной области может быть представлено различными симптомо-комплексами и клиническими формами: идиопатическое макулярное отверстие, эпимакулярный фиброз, тракционный макулярный отек при диабетической и посттромботической ретинопатии, фовеошизис, экссудативная возрастная макулодистрофия [Gandorfer A. et al., 2009; Witkin A. et al., 2012].
Цель — изучить динамику симптоматической витреомакулярной адгезии у пациентов, не получивших по разным причинам хирургическое пособие.
Материал и методы
Нами изучено безоперационное течение симптоматической витреомакулярной адгезии у 110 пациентов. Возраст пациентов — от 51 года до 74 лет (средний — 61,5±4,4 года). Женщин было 86 (78%), мужчин — 24 (22%). Средняя корригированная острота зрения составляла 0,17±0,02. При первичном обращении все пациенты предъявляли характерные для макулярной патологии специфические жалобы: затуманивание и снижение центрального зрения (93%), метаморфопсии (70%), нарушение бинокулярного зрения (53%) и диплопию (37%). После проведения общеклинических и ОКТ-исследований пациентам поставлен диагноз «Витреомакулярный тракционный синдром». Было предложено хирургическое лечение, от которого пациенты отказались по разным причинам. За этими больными было установлено динамическое наблюдение. Сроки наблюдения за пациентами составили от 3 мес. до 2 лет.
Результаты
Динамическое клиническое наблюдение и ОКТ-контроль за пациентами выявили различную динамику течения у них ВМА.
Самостоятельное отслоение задней гиалоидной мембраны диагностировано у 4 (3,6%) пациентов с локальной ВМА, что привело к устранению витреомакулярной тракции и улучшению витреомакулярного интерфейса: исчез ретинальный отек и деформация сетчатки, нормализовался макулярный и фовеолярный профили сетчатки. Клинически пациенты отмечали улучшение остроты зрения, исчезновение затуманивания и метаморфопсий в проекции зрения. Средняя корригированная острота зрения у пациентов этой группы повысилась с 0,23±0,02 до 0,54±0,02. Никаких хирургических вмешательств пациентам этой группы не понадобилось.
У остальных 106 пациентов наблюдалась отрицательная динамика витреомакулярного интерфейса с постепенным снижением остроты зрения.
В группе пациентов с локальной плотной ВМА (51 (46%) пациент) отмечалась нарастающая витреомакулярная тракция, которая привела к формированию кистозных полостей в толще сетчатки, увеличению конусовидного выпячивания сетчатки и, в конечном счете, к ее дефекту с формированием сквозного (38) или ламеллярного (13) макулярных разрывов. Пациентам было предложено витреоретинальное хирургическое лечение.
У пациентов с широкой разлитой ВМА (55, 50% пациентов) отмечалась также отрицательная динамика, но она носила более медленный и затяжной характер. Пациенты отмечали постепенное снижение остроты зрения, усиление затуманивания остроты зрения, нарастающие искажения в поле зрения. На ОКТ выявилось разлитое утолщение сетчатки, формирование мелких кистозных полостей, нарастание ретинального отека, сглаживание макулярного профиля, а позже — и его возвышение. Практически у всех пациентов на поверхности сетчатки отчетливо контурировалась эпимакулярная фиброзная ткань в виде рефлексирующей полосы, которая деформировала поверхность сетчатки. Пациентам было предложено витреоретинальное хирургическое лечение.
Выводы
1. Симптоматическая витреомакулярная адгезия связана с неполным отслоением заднего гиалоида и формированием витреомакулярного тракционного синдрома.
2. При локальной ВМА возможно самостоятельное отслоение прикрепленного заднего гиалоида, восстановление макулярного профиля сетчатки и клиническое выздоровление, что наблюдалось у 3,6% наших пациентов.
3. Неразрешившаяся локальная плотная витреомакулярная адгезия у 46% пациентов имела отрицательную динамику и приводила к формированию сквозных и ламеллярных разрывов макулы, что требовало хирургического лечения.
4. Широкая разлитая витреомакулярная адгезия, диагностированная у 50% пациентов, имела также отрицательную динамику с постепенной деформацией сетчатки и формированием хронических макулярных отеков и эпимакулярного фиброза, требовавших витреоретинального вмешательства.
Источник
| адгезия витреомакулярного | |
|---|---|
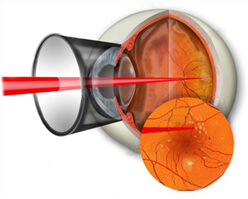
| Принципиальная электрическая схема человеческого глаза. |
Витреомакулярная адгезия (ВМА) представляет собой человеческое состояние здоровья , где стекловидное тело гель (или просто стекловидное тело) из человеческого глаза прилипает к сетчатке в аномально сильной манере. Как глаза возрасты, он является общим для стекловидного тела отделяется от сетчатки. Но если это разделение не является полным, т.е. есть еще адгезия , это может создать силы тяги на сетчатке , которые могут привести к последующей потере или искажению зрения. Адгезии в самом по себе не опасно, но в результате патологические витреомакулярные тяги (ВМТ) могут привести к серьезному повреждению глазного.
Тока стандартом лечения для лечения этих спаек является Парс Plana витрэктомии (ППВ), который включает в себя хирургическое удаление стекловидного тела из глаза. Биологическое средство для неинвазивного лечения спаек называемых ocriplasmin был одобрен FDA 17 октября 2012 года .
Симптом / знаки
Тяговый вызванное VMA является основной патологии болезни глаз называется симптоматической ВМА. Существует доказательство того, что симптоматическое VMA может внести свой вклад в развитие ряда хорошо известных заболеваний глаз, таких как макулярной отверстие и макулярной морщиться, что может привести к ухудшению зрения, включая слепоту. Он также может быть связано с возрастной макулярной дегенерации (AMD), диабетический макулярный отек (DME), окклюзии вены сетчатки и диабетической ретинопатии (DR).
патология
Со времени, он является общим для стекловидного тела внутри человеческого глаза сжиженного и сворачивать в процессах , известные как синерезис и synchisis соответственно. Это создает заполненную жидкость области , которые могут объединяться с образованием карманов стекловидного геля , которые в основном жидкостями с очень малыми концентрациями коллагена . Если эти жидкие карманы достаточно близко к границе раздела между стекловидным гелем и сетчатками, они могут вызвать полное отделение стекловидного тела от сетчатки в процессе , как правило , происходящем в пожилых люди называются задним стекловидный отрядом (PVD). PVD в само по себе не опасно и естественный процесс.
Если отделение стекловидного тела от сетчатки не является полным, области фокальной привязанности или спаек могут происходить, т.е. VMA. Тянущие силы тяги или от этой адгезии на поверхности сетчатки иногда могут вызвать отек внутри сетчатки, повреждение кровеносных сосудов сетчатки вызывает кровотечение или повреждение зрительного нерва вызывает нарушение в нервных сигналах , направленных в мозг для визуальной обработки . Важно отметить , что в то время как сам VMA не опасен, в результате вытягивать на сетчатке называется витреомакулярные тяги (ВМТ) вызывает вышеупомянутое повреждение. Размер и прочность VMA определяют разнообразие в результате патологии или симптомов.
VMA также может привести к развитию VMT / тяга , связанным с осложнениями , такими как макулярные морщат и макулярное отверстие , ведущих к искаженному видению или метаморфопсии ; Epiretinal мембрана ; тяговый макулярный отек ; близорукая макулярная ретиношизис ; нарушение зрения; слепота. Заболеваемость VMA сообщаются выше , чем 84% пациенты с макулярным отверстием , 100% для пациентов с витреомакулярными тяговым синдромом , а также 56% в идиопатической epimacular мембраны .
диагностика
Тщательное обследование глаз с помощью офтальмолога или окулиста имеет решающее значение для диагностики симптоматической VMA. Визуализации технологии , такие как оптической когерентной томографии (OCT) значительно улучшили точность диагностики симптоматической VMA.
лечение
Новый FDA одобрило препарат был выпущен на рынок в конце 2013 г. Jetrea (Брэнд) или Ocriplasmin (общее название) является первым препаратом такого типа используется для лечения витреомакулярного adhension. Механизм действия: Ocriplasmin представляет собой усеченный человеческий плазмин с протеолитической активностью против белковых компонентов стекловидного тела и vitreretinal интерфейса. Он растворяет матрицу белка , ответственную за витреомакулярную адгезию. Побочные реакции на лекарства: Снижение зрения, потенциал для линз sublaxation, dyschromatopsia (желтый) зрение, боль в глазах, поплавки, затуманенное зрение. Новое сравнение Drug рейтинг дал Jetea в 5 указывает на важный шаг вперед. Раньше не рекомендуется лечение не было доступно для пациента с умеренной симптоматической ВМА. В симптоматических пациентов VMA с более значительной потерей зрения, стандартом лечения является Парс Plana витрэктомии (ППВ), который включает в себя хирургическое удаление стекловидного тела из глаза, тем самым высвобождая хирургическим симптоматическое VMA. Другими словами, витрэктомии индуцирует PVD , чтобы освободить тяги / адгезии на сетчатке. По оценкам 850000 процедуры витрэктомии проводится во всем мире ежегодно с 250,000 в Соединенных Штатах.
Стандартная процедура П может привести к серьезным осложнениям , включая малый калибр PPV. Осложнения могут включать отслойки сетчатки , слезы сетчатки , эндофтальмят и послеоперационный катаракта образование. Кроме того, П могут привести к неполному разделению, и она потенциально может оставить очаг для вазоактивных и вазопролиферативных веществ, или это может вызвать развитие сосудисто — волокнистых мембраны . Как и с любой инвазивной процедурой, PPV вводит травму в стекловидное тело и окружающие ткани.
Есть данные , показывающие , что нехирургическая индукция PVD с использованием ocriplasmin (а рекомбинантный протеазы с активностью против фибронектина и ламининой ) может предложить преимущества успешного PVD, устраняя риски , связанные с хирургической процедурой, т.е. витрэктомии. Фармакологический витреолизис является улучшением по сравнению с инвазивной хирургией , как это вызывает полное разделение, создает более физиологическое состояние интерфейса витреомакулярного, предотвращает развитие сосудисто — волокнистых мембран, является менее травматичным стекловидным телом, и является потенциально профилактическим . По состоянию на 2012 год , ThromboGenics продолжает разрабатывать ocriplasmin биологического агента. Ocriplasmin утвержден недавно под названием Jetrea для использования в Соединенных Штатах по FDA .view.
Экспериментальная проверка инъекций перфторпропана (C 3 F 8 ) на 15 симптоматических глазах 14 пациентов показала , что витреомакулярные тяговые решена в 6 глаз в течение 1 месяца и решили более 3 глаз в течение 6 месяцев.
Рекомендации
- ^ Паоло Carpineto, Лука ди Антонио, Agbeanda Aharrh-Gnama, Винченцо Ciciarelli, Леонардо Mastropasqua. Диагностика и лечение витреомакулярной адгезии. Европейский офтальмологический обзор, 2011,5 (1): 69-73
- ^ Кернер F, Garweg Дж [Болезнь vitreo-макулярного интерфейс]. Клин Monbl Augenheilkd. 1999; 214 (5): 305-310.
- ^ Mojana Р, Ченг л, Барч DU,др. Роль аномальной витреомакулярной адгезии в возрастной макулярной дегенерации: спектральная оптической когерентной томографии и хирургических результатах. Am J Ophthalmol. 2008; 146 (2): 218-227.
- ^ Doft ВН, Вишниевски SR, Келси SF, Groer-Фицджеральд S; Endophthalmitis Витрэктомия Study Group. Диабет и postcataract эндофтальмит экстракции. Curr ОПИН Ophthalmol. 2002; 13 (3): 147-151.
- ^ Doft БМ, Келси SF, Вишниевски SR. Отслойка в исследовании эндофтальмиты витрэктомии. Arch Ophthalmol. 2000; 118 (12): 1661-1665.
- ^ Вишниевски СР, Капоне А, Келси SF,др. Характеристики после экстракции катаракты или вторичной имплантации линзы среди пациентовобследованных на эндофтальмиту витрэктомии исследования. Офтальмология. 2000; 107 (7): 1274-1282.
- ^ Гупта OP, ED Weichel, Regillo CD и др. Послеоперационные осложнениясвязанные с 25-калибра рагз PLANA витрэктомии. Офтальмологическая SURG Лазеры визуализация. 2007; 38 (4): 270-275.
- ^
Лю DT, Чан CK, Вентилятор DS, Lam SW, Lam DS, Chan WM. Хориоидеи складок после25 калибра трансконъюктивальных бесшовной витрэктомии. Eye. 2005; 19 (7): 825-827. - ^
Scott IU, Флинн HWмладший, Dev S и др. Эндофтальмит после 25 калибра и 20 калибра рагз PLANA витрэктомии: заболеваемость и исходы. Сетчатка. 2008; 28 (1): 138-142. - ^
Kunimoto DY, Kaiser RS; Wills Eye Retina Service. Заболеваемость эндофтальмита после 20- и 25- калибра витрэктомии. Офтальмология. 2007; 114 (12): 2133-2137. - ^
Kaiser RS. Осложнения бесшовной витрэктомии и выводы Micro-хирургическую Целевой группыбезопасности. Документпредставленный на: Retina субспециальностей день, ежегодной встрече Американской академии офтальмологии; 7-8 ноября 2008; Атланта, штат Джорджия. - ^ Де Смет MD, Гандорфер A, Stalmans P и др. Микроплазмина введениестекловидном теле у больных с витреомакулярной тягой запланированном на витрэктомию: суд MIVI I. Офтальмология. 2009; 116 (7): 1349-1355.
- ^
Гольденберг DT, Trese MT. Фармакологическое vitreodynamics и молекулярный поток. Dev Ophthalmol. 2009; 44: 31-36. - ^ Stalmans Р, МСBenz, Гандорфер А, Kampik А, Girach А, Pakola S, Галлер JA; MIVI-TRUST Study Group. Ферментативный витреолизис с ocriplasmin для витреомакулярнога тяги и макулярного отверстия. N Engl J Med. 2012 16 августа, 367 (7): 606-15.
- ^ Де Смет MD, Гандорфер A, Stalmans P и др. Микроплазмина введениестекловидном теле у больных с витреомакулярной тягой запланированном на витрэктомию: суд MIVI I. Офтальмология. 2009; 116 (7): 1349-1355.
- ^
Гольденберг DT, Trese MT. Фармакологическое vitreodynamics и молекулярный поток. Dev Ophthalmol. 2009; 44: 31-36. - ^ https://bmctoday.net/retinatoday/2012/05/supplement/article.asp?f=symptomatic-vitreomacular-adhesion
- ^ Rodrigues IA; Stangos; McHugh DA; Джексон TL (2013). «Интравитреальная инъекция expansile перфторпропан (С 3 F 8 ) для лечения витреомакулярной тяги». Американский журнал офтальмологии . 155 (2)): 270-276. DOI : 10.1016 / j.ajo.2012.08.018 .
внешняя ссылка
Источник
Клиническая картина
Симптомы регматогенной отслойки сетчатки: у 60% пациентов отмечаются вспышки света, флоатеры в стекловидное тело (вызванные острой отслойкой ЗГМ с коллапсом). Через некоторое время пациент замечает дефект поля зрения, который может затрагивать центральное зрение. У 40% больных сразу возникает дефект поля зрения.
Фотопсии связаны с тракцией в участках витреоретинальной адгезии. При этом либо адгезия разрушается, либо отрывается «крышечкой» участок сетчатки. В глазах с отслойкой ЗГМ фотопсии могут вызываться движением глаз; чаще проецируются темпорально.
Флоатеры — движущиеся тени в стекловидном теле, они бывают 3 типов:
- солитарная, большая кольцеобразная тень — кольцо Вайсса по краям диска зрительного нерва;
- нитевидная — конденсация коллагеновых волокон в коре стекловидного тела;
- внезапные тени, темные или красноватые пятна — свидетельствуют о витреальном кровоизлиянии при разрыве периферического сосуда.
Дефект поля зрения вызывается распространением субретинальной жидкости к экватору. Дефект прогрессирует, иногда может развиться отслойка сетчатки с утра за счет спонтанной абсорбции жидкости за ночь. Дефект внизу замечается больным раньше, чем вверху.
Потеря центрального зрения является результатом вовлечения фовеа или закрытия зрительной оси большим куполом отслойки сетчатки.
Клинические признаки:
- относительный афферентный зрачковый дефект (при больших отслойках сетчатки);
- внутриглазное давление снижено на 5 мм рт. ст. по сравнению с другим глазом;
- легкие явления переднего увеита;
- разрывы в сетчатке, обычно красного цвета;
- отслоенная сетчатка имеет выгнутую поверхность, она несколько матовая на вид, сосуды выглядят темнее, чем в нормальной сетчатке, и меньше заметен контраст а:b. Субретинальная жидкость распространяется к ora serrata; отслоенная сетчатка мобильна, подвижна. При отслойке в заднем полюсе определяется псевдоразрыв в макулярной области (ML);
- в стекловидном теле — отслойка ЗГМ, «табачная пыль» в переднем гиалоиде. Иногда может присутствовать кровь.
Без лечения отслойка сетчатки приводит к вторичной катаракте, хроническому увеиту, гипотонии, фтизису глаза. Редко бывает спонтанное ограничение отслойки. Крайне редко, если больной находится на постельном режиме, отслойка прилегает сама.
Для старых отслоек сетчатки характерно:
- истончение (следует не путать с ретиношизисом);
- вторичные кисты возникают через год, исчезают после успешного прилегания;
- субретинальные демаркационные линии (на границе между отслойкой и нормальной сетчаткой). Они не всегда отграничивают отслойку сетчатки; обычно они содержат сначала пигмент, а потом его теряют.
Пролиферативная ретинопатия вызвана пролиферацией мембран эпиретинально, на задней поверхности отслоенного стекловидного тела и даже субретинально. Слабая пролиферативная ретинопатия обнаружена в 5% случаев с отслойкой сетчатки. Иногда сокращения фиброзного компонента эпи- и субретинальной мембран вызывает тракцию и смещение сетчатки. Выраженная постоперативная пролиферативная ретинопатия является причиной неуспешной хирургии отслоек. Стадии пролиферативной ретинопатии перечислены в международной классификации (А-С).
При тракционной отслойке сетчатки отсутствуют фотопсии и флоатеры. Отслойка развивается медленно, дефект поля зрения возникает постепенно, годами он может быть стационарным. Разрывов нет, пока не разовьется вторичный регматогенный компонент. Отслоенная сетчатка имеет вогнутое направление и неподвижна. Количество субретинальной жидкости тут меньше, редко доходит до от serrata. Вторичные изменения отсутствуют.
При экссудативной отслойке сетчатки фотопсии отсутствуют, так как нет тракции, флоатеры могут быть. Дефект поля зрения возникает внезапно, быстро. При синдроме Харада оба глаза могут поражаться одновременно. Разрывы сетчатки отсутствуют. Отслоенная сетчатка может быть видна в щелевую лампу без линзы, доходя до хрусталика. При перемене положения тела при экссудативной отслойке субретинальная жидкость смещается, сетчатка временно прилегает.
Т. Бирич, Л. Марченко, А. Чекина
«Симптомы отслойки сетчатки» статья из раздела Офтальмология
Дополнительная информация:
- Травма глаза и отслойка сетчатки
- Профилактика отслойки сетчатки
Источник
Периферические дистрофии сетчатки находятся в ракурсе постоянного внимания офтальмологов в связи с риском развития отслойки сетчатки, возникновение которой связывают с тракционным воздействием со стороны СТ [48,50,83].
Русецкая Н.С. (1976), изучавшая факторы риска развития первичной отслойки сетчатки, в том числе у пожилых лиц, большую роль в развитии регматогенной отслойки сетчатки придает периферическим витреоретинальным дегенерациям [68].
В настоящее время существует несколько видов классификаций периферических дистрофий сетчатки. В соответствии с локализацией различают экваториальные, параоральные (у зубчатой линии) и смешанные формы периферических витреохориоретинальных дистрофий [50].
Иванишко Ю.А. с соав. (2003), подчеркивая важность вовлечения стекловидного тела в патологический процесс, отмечает наличие периферических хориоретинальных дистрофий (ПХРД) и периферических витреохориоретинальных дистрофий (ПВХРД) [38]. К ПХРД относят: друзы, параоральные кисты, дистрофию по типу «булыжной мостовой», микрокистозную дегенерацию, дегенеративный и врожденный ретиношизис. К ПВХРД — инееподобная дегенерация, «решетчатая», «след улитки». Дистрофиями, очень редко приводящими к разрывам и отслойке сетчатки, по мнению авторов, являются друзы и параоральные кисты; к «условно» предотслоечным относят «булыжную мостовую», микрокистозную дегенерацию, дегенеративный и врожденный ретиношизис, инееподобную дегенерацию. «Облигатно» предотслоечными дистрофиями, по мнению авторов, являются «решетчатая» дегенерация и дистрофия по типу «следа улитки» [54].
Периферическая кистозная дистрофия характеризуется небольшими кистами на крайней периферии сетчатки, которые находятся в наружном плексиформном и внутреннем ядерном слоях сетчатки и часто встречаются в глазах недоношенных детей и людей пожилого возраста. С возрастом микрокисты могут сливаться, формируя более крупные кисты. Возможны разрывы как внутренней, так и наружной стенки кисты.
Spensоr W.H. [1985] утверждает, что периферическая кистозная дегенерация обнаруживается в 86.8% аутопсированных глаз у лиц старше 70 лет (Рис.7). По мнению автора, кистозная дегенерация редко может распространяться к экватору, но из нее может развиваться типичный периферический дегенеративный ретиношизис [205].
По мнению ряда авторов, кистозная дегенерация очень редко может приводить к развитию отслойки сетчатки (Рис.7) [38,114,123].
Пантелеева О.А., (1996) дает определение ретиношизиса, как дегенеративное изменение сетчатки, сопровождающееся ее кистозным перерождением, складчатостью, разрывами, отслойкой сетчатки и изменением СТ [59].
Ретиношизис согласно классификации Луковской Н.Г. (2008) имеет три разновидности:
1) врожденный, Х-сцепленный ювенильный ретиношизис, при котором помимо периферических изменений сетчатки отмечается патология макулярной области;
2) приобретенный ретиношизис, к нему относятся миопический и сенильный;
3) вторичный ретиношизис, который встречается после травмы и при различных заболеваниях глаз [7,59].
Частота встречаемости ретиношизиса по данным разных авторов варьирует от 3-х до 22-х % от общей популяции [69]. Сочетание разрывов во внутреннем и наружном листках ретиношизиса может привести в 3.7-11-ти % случаев к отслойке сетчатки [59,123,205].
По данным Луковской Н.Г. (2008) миопический ретиношизис развивается из кистозной дегенерации при прогрессировании миопии, местом его локализации являются параоральная, экваториальная и центральная зоны сетчатки. Чаще всего ретиношизис наблюдался у пациентов молодого возраста со степенью миопии от 1-й до 6-ти Д.
Известно, что сенильный ретиношизис (СР) — это расщепление сетчатки, возникающее у лиц старше 50-ти лет вследствие дегенеративных ее изменений, как правило, двухстороннее, симметричное по расположению и начинающееся с периферии [59,69,123].
Саксонова Е.О. с соавторами (1975) полагают, что сенильный ретиношизис обусловлен периферической кистозной дегенерацией сетчатки и реже всего выявлялся у лиц старше 60-ти лет с миопической рефракцией. Данные Луковской Н.Г (2008) указывают на преобладание гиперметропической и эмметропической рефракции у больных с сенильным ретиношизисом, однако частота выявления данной патологии была выше в группе старше 60-ти лет.
При офтальмоскопии периферического ретиношизиса на поверхности внутреннего слоя сетчатки можно видеть белые отложения, множественные маленькие, округлые отверстия (Рис. 9, 10). Сосуды сетчатки часто окружены белым футляром. Наружный слой ретиношизиса толще, чем внутренний, и тесно прилежит к пигментному эпителию сетчатки [123].
Периферическая хориоретинальная дистрофия по типу «булыжной мостовой» имеет вид атрофических фокусов с пигментированной каймой (Рис.11). Эти участки размером от одного до нескольких дисков располагаются между ora serrata и экватором. Частым местом локализации являются нижние назальный и темпоральный квадранты. Светлая окраска «булыжной мостовой» обусловлена просвечиванием склеры сквозь атрофичные сетчатку и хориоидею, с отсутствием пигментного эпителия, наружного ядерного и плексиформного слоев. Поверхность дефекта ровная, края часто пигментированы (Рис.12). Множественные дефекты могут сливаться, образуя при этом атрофический пояс на периферии сетчатки. Хориоретинальные дистрофии по типу «булыжной мостовой» наблюдаются в пожилом возрасте одинаково часто у мужчин и женщин и имеют двустороннюю локализацию. Данный вид дистрофии не провоцирует развитие отслойки сетчатки и в действительности может защищать от прогрессирования отслойки сетчатки [2,50, 123,205].
Решетчатая дистрофия и дистрофия по типу «следа улитки» специфические и очень важные дегенерации сетчатки, которые могут располагаться рядом с экватором во всех меридианах, но наиболее часто в нижнем и верхнем сегментах, участки дегенерации параллельны ora serrata (Рис.13).
«Решетчатую дегенерацию считают наиболее прогностически неблагоприятной формой ПВХРД, при которой отслойка сетчатки имеет место в 40-60% случаев [114,154,217].
Термин «решетчатая дегенерация» (РД) происходит из-за белых линий, которые представлены истонченными и заключенными в футляр ретинальными сосудами.
Стекловидное тело над участком решетчатой дегенерации выглядит разжиженным, по краям дефекта существует сильная витреоретинальная адгезия, которая может привести к отслойке сетчатки (Рис. 14) [205].
Решетчатая дистрофия встречается в 8 % случаев из общей популяции, становится видимой на втором десятилетии жизни и прогрессирует с возрастом. В 50% случаев решетчатая дистрофия сетчатки симметрична и характерна для миопии средней и высокой степени [50,63,123,205].
Дистрофия по типу «следа улитки» (СУ) характеризуется истончением сетчатки с потерей внутренних слоев и наличием маленьких округлых дефектов внутри участка дегенерации сетчатки, которые могут быть частичными или сквозными. СТ, прилежащее к СУ, прозрачное и разжиженное, по краям также плотно фиксировано к сетчатке [123].
Дефекты в сетчатке внутри участка данной дегенерации могут быть стационарными в течение многих лет, но спонтанная отслойка СТ или экстракция катаракты могут спровоцировать отслойку сетчатки [63,123].
Spenser (1986) считает, что дистрофия по типу «следа улитки», инеевидная и решетчатая дистрофии имеют схожую гистологическую структуру, для которой характерно: истончение сетчатки, разжиженное СТ над участками дегенерации, по краям дефектов существование сильной витреоретинальной адгезии [205].
Ряд авторов указывают на наличие в параоральной зоне измененных волокон СТ в виде полупрозрачных «тяжей» (tufts), которые имеют выраженную фиксацию к сетчатке и зачастую не диагностируются даже в условиях выраженного мидриаза и прозрачности оптических сред, данные структуры образованы за счет разрастания глиальных клеток и расцениваются как зоны возможной пролиферации при развитии патологических процессов в глазу [118,205] (Рис 16).
В современной классификации пролиферативного процесса чрезвычайная роль отводится передней пролиферативной витреоретинопатии, которая не сопутствует отслойке сетчатки, а предшествует ей, вызывая ее развитие [27,91]. Длительное время данные структуры могут существовать бессимптомно, однако в условиях травмы, воспаления эти структуры могут вызывать активацию пролиферативного процесса [118].
Основное внимание до настоящего времени уделялось возникновению периферических хориоретинальных дистрофий сетчатки у лиц с миопией высокой степени [15,36,63]. Патогенетическим обоснованием возникновения периферических дистрофий сетчатки у данной категории больных служит растяжение склеральной капсулы и возникающие при этом трофические нарушения в сетчатке [15]. Установлена четкая зависимость частоты дистрофических изменений периферии сетчатки с величиной осевой длины глаза (Табл. 1) [114]. С увеличением степени близорукости возрастает и частота дистрофий, в 90% случаев они диагностированы при увеличении передне-задней оси глаза более 27 мм [154].
Недавние исследования ряда авторов опровергнули зависимость периферических дистрофий сетчатки от вида рефракции лиц в возрасте от 16-ти до 45-ти лет. Авторы доказали, что периферические хориоретинальные дистрофии часто не коррелируют со степенью близорукости, возрастом и длинной передне-задней оси глаза.
Таким образом, суммируя все вышесказанное, можно сделать выводы, что периферические хориоретинальные и витреохориоретинальные дистрофии сетчатки — это часто встречающая патология, которая не зависит от возраста и степени рефракции. В течение многих лет дистрофии могут протекать стационарно, но при возникновении сопутствующей патологии глаза (травмы, воспаления, деструкции СТ, ЗОСТ, экстракции катаракты и т.д.) могут вызвать активацию пролиферативного процесса с последующим развитием отслойки сетчатки. Наличие миоза и непрозрачности оптических сред не позволяют использовать традиционные методы диагностики патологии периферии сетчатки, такие как: биомикроскопия с линзой Гольдмана и офтальмоскопия.
Источник